解答题-原理综合题 较难0.4 引用1 组卷40
研究氮氧化物污染的治理是环保的一项重要工作.合理应用和处理氨氧化物,在生产生活中有重要意义.
(1)已知:① ;
;
② .
.
则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为_______________________ .
(2)利用测压法在恒容刚性反应器中研究反应 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
① 时,反应物的转化率
时,反应物的转化率
_____________ .若降低反应温度,则平衡后体系总压强小于 ,主要原因是
,主要原因是________________________ .
②T℃时反应 的平衡常数
的平衡常数
______ ( 为以分压表示的平衡常数).
为以分压表示的平衡常数).
(3)一定条件下,在体积为2L的密闭容器中充入 发生反应:
发生反应:  .实验测得
.实验测得 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.
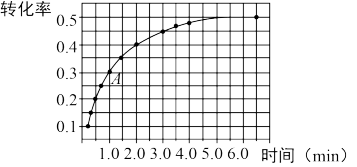
①要提高 的转化率,可采取的措施是
的转化率,可采取的措施是_____________ 、____________ (写两条).
②计算A点处
_____________ (保留一位小数).
(1)已知:①
②
则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为
(2)利用测压法在恒容刚性反应器中研究反应
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
②T℃时反应
(3)一定条件下,在体积为2L的密闭容器中充入
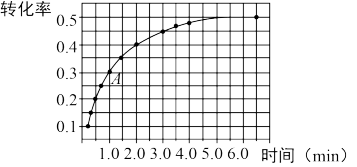
①要提高
②计算A点处
23-24高二下·云南保山·开学考试
类题推荐
Ⅰ.利用测压法在刚性反应器中研究 T℃ 时:
3NO2(g) 3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:
3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:
(1)该反应达到平衡后的熵值较平衡前______________ (填“增大”“减小”“不变”)。
(2)若降低反应温度,则平衡后体系压强 p____ 24.00 MPa(填“大于”“等于”“小于”),原因是_____________________________________________________________________ 。15min 时,反应物的转化率 α=__________ %
Ⅱ.一定条件下,在体积为 2 L 的密闭容器中发生反应:2NO2(g) 2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。
2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。

(1)要提高 NO2转化率,可采取的措施是________________ 、__________________ 。
(2)前2min内,以NO2表示该反应的化学反应速率为___________________ 。
(3)计算 A 点处v正/ v逆=_________________ (保留一位小数)。
3NO2(g)
 3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:
3NO(g)+O3(g) ΔH=+317.3kJ·mol-1的分解反应,体系的总压强 p随时间 t 的变化如下表所示:| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
(2)若降低反应温度,则平衡后体系压强 p
Ⅱ.一定条件下,在体积为 2 L 的密闭容器中发生反应:2NO2(g)
 2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。
2NO(g)+O2(g) ΔH>0。投入 2 mol NO2发生反应。实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为 T℃ 时 NO2的转化率随时间变化的结果如图所示。
(1)要提高 NO2转化率,可采取的措施是
(2)前2min内,以NO2表示该反应的化学反应速率为
(3)计算 A 点处v正/ v逆=
烟气(主要污染物SO2、NOX)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中的SO2、NOx 的含量。
(1) O3氧化烟气中 SO2、NOx 的主要反应的热化学方程式为: NO(g)+O3(g) NO2(g)+ O2(g) ΔH=-200.9 kJ·mol-13NO(g)+O3(g)⇌3NO2(g) ΔH=-317.3kJ·mol-1。则2NO2(g)⇌2NO(g)+O2(g)的ΔH=
NO2(g)+ O2(g) ΔH=-200.9 kJ·mol-13NO(g)+O3(g)⇌3NO2(g) ΔH=-317.3kJ·mol-1。则2NO2(g)⇌2NO(g)+O2(g)的ΔH=_____________ kJ·mol-1
(2)T℃时,利用测压法在刚性反应器中,投入一定量的NO2发生反应3NO2(g) 3NO(g)+O3(g),体系的总压强 p随时间 t的变化如下表所示:
3NO(g)+O3(g),体系的总压强 p随时间 t的变化如下表所示:
①若降低反应温度,则平衡后体系压强 p______ 24.00 MPa(填“>”、“<”或“=”),原因是____________ 。
②15min 时,反应物的转化率 α=______ 。
③T℃时反应3NO2(g) ⇌ 3NO(g)+O3(g)的平衡常数Kp=____________ (Kp 为以分压表示的平衡常数,分压等于总压乘以该气体的物质的量分数)
(3)T℃时,在体积为2L的密闭刚性容器中,投入2 mol NO2发生反应2NO2(g) 2NO(g)+O2(g) ,实验测得:v正=k正 c2(NO2),v逆=k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时 NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):
2NO(g)+O2(g) ,实验测得:v正=k正 c2(NO2),v逆=k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时 NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):

①在体积不变的刚性容器中,投入固定量的NO2发生反应,要提高 NO2转化率,可采取的措施是______________ 、___________ 。
②由图中数据,求出该反应的平衡常数为_________ 。
③计算 A 点处 v正/v逆=_________________________ (保留1位小数)。
(1) O3氧化烟气中 SO2、NOx 的主要反应的热化学方程式为: NO(g)+O3(g)
(2)T℃时,利用测压法在刚性反应器中,投入一定量的NO2发生反应3NO2(g)
 3NO(g)+O3(g),体系的总压强 p随时间 t的变化如下表所示:
3NO(g)+O3(g),体系的总压强 p随时间 t的变化如下表所示: | 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
②15min 时,反应物的转化率 α=
③T℃时反应3NO2(g) ⇌ 3NO(g)+O3(g)的平衡常数Kp=
(3)T℃时,在体积为2L的密闭刚性容器中,投入2 mol NO2发生反应2NO2(g)
 2NO(g)+O2(g) ,实验测得:v正=k正 c2(NO2),v逆=k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时 NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):
2NO(g)+O2(g) ,实验测得:v正=k正 c2(NO2),v逆=k逆 c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时 NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡): 
①在体积不变的刚性容器中,投入固定量的NO2发生反应,要提高 NO2转化率,可采取的措施是
②由图中数据,求出该反应的平衡常数为
③计算 A 点处 v正/v逆=
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中的SO2、NOx的含量。
(1)O3氧化姻气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g) NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO2(g)+O2(g) △H=-200.9kJ·mol-1
3NO(g)+O3(g) 3NO2(g) △H=-317kJ·mol-1。
3NO2(g) △H=-317kJ·mol-1。
则2NO2(g) 2NO(g)+O2(g)的△H=
2NO(g)+O2(g)的△H=____ kJ·mol-1。
(2)T℃时,利用测压法在刚性反应器中,投入一定量的NO2发生反应3NO2(g) 3NO(g)+O3(g),体系的总压强p随时间t的变化如表所示:
3NO(g)+O3(g),体系的总压强p随时间t的变化如表所示:
①15min时,反应物的转化率α=____ 。
②T℃时反应3NO2(g) 3NO(g)+O3(g)的平衡常数Kp=
3NO(g)+O3(g)的平衡常数Kp=____ (Kp为以分压表示的平衡常数分压等于总压乘以该气体的物质的量分数)
(3)T℃时,在体积为2L的密闭刚性容器中,投入2molNO2发生反应2NO2(g) 2NO(g)+O2(g),实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):
2NO(g)+O2(g),实验测得:v正=k正c2(NO2),v逆=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。在温度为T℃时NO2的转化率随时间变化的结果如图所示(反应在5.5min时达到平衡):
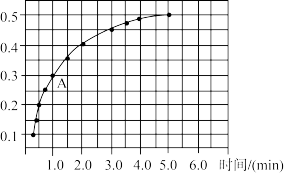
①在体积不变的刚性容器中,投入固定量的NO2发生反应,要提高NO2转化率,可采取的措施是____ 、____ 。
②由图中数据,求出该反应的平衡常数为____ 。
③计算A点处 =
=____ (保留1位小数)。
(1)O3氧化姻气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)
3NO(g)+O3(g)
则2NO2(g)
(2)T℃时,利用测压法在刚性反应器中,投入一定量的NO2发生反应3NO2(g)
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
①15min时,反应物的转化率α=
②T℃时反应3NO2(g)
(3)T℃时,在体积为2L的密闭刚性容器中,投入2molNO2发生反应2NO2(g)

①在体积不变的刚性容器中,投入固定量的NO2发生反应,要提高NO2转化率,可采取的措施是
②由图中数据,求出该反应的平衡常数为
③计算A点处
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


