解答题-工业流程题 适中0.65 引用2 组卷208
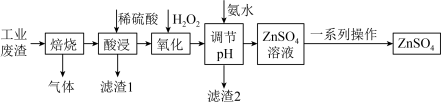
硫酸锌是制造锌钡白和锌盐的主要原料,也可用作印染媒染剂、木材和皮革的保存剂。现从工业废渣中(主要成分ZnS,含有 等杂质)制取
等杂质)制取 流程如图所示;
流程如图所示;
(1)“酸浸”时为了提高浸出效率可采取的措施有___________ 。
(2)“滤渣1”的主要成分是___________ 。
(3)“氧化”中发生反应的离子方程式是___________ 。
(4)加入氨水“调节 ”的作用是
”的作用是___________ ,调节过程中加热有利于反应但温度不宜过高,原理是___________ 。
(5)“一系列操作”中包括___________ ,冷却结晶、___________ 、洗涤、干燥。
(1)“酸浸”时为了提高浸出效率可采取的措施有
(2)“滤渣1”的主要成分是
(3)“氧化”中发生反应的离子方程式是
(4)加入氨水“调节
(5)“一系列操作”中包括
23-24高三下·海南省直辖县级单位·开学考试
类题推荐
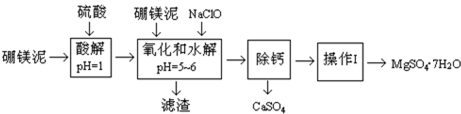
硼镁泥是一种工业废料,主要成分是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的流程如图:
根据题意回答下列问题:
(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施________ 、________ ;
(2)滤渣的主要成分除含有Fe(OH)3、Al(OH)3、MnO2外,还有________ ;
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是________ ,在调节pH、发生水解之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为________ ;
(4)如何检验滤液中Fe3+是否被除尽,简述检验操作________ ;
(5)已知MgSO4、CaSO4的溶解度如下表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤________ 、________ 。
根据题意回答下列问题:

(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施
(2)滤渣的主要成分除含有Fe(OH)3、Al(OH)3、MnO2外,还有
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是
(4)如何检验滤液中Fe3+是否被除尽,简述检验操作
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网