解答题-原理综合题 较难0.4 引用3 组卷579
丁二烯是生产丁苯橡胶、聚二烯橡胶等的基本原料.丁烯 氧化脱氢制丁二烯
氧化脱氢制丁二烯 的生产工艺涉及反应如下:
的生产工艺涉及反应如下:
反应Ⅰ

反应Ⅱ

回答下列问题:
(1)判断反应Ⅱ的自发性并说明理由__________ .
(2)在常压、催化剂作用下,投料按 ,并用水蒸气稀释;不同温度下反应相同时间后,测得丁烯的转化率与丁二烯、二氧化碳的选择性随温度变化情况如图1所示(选择性:转化的
,并用水蒸气稀释;不同温度下反应相同时间后,测得丁烯的转化率与丁二烯、二氧化碳的选择性随温度变化情况如图1所示(选择性:转化的 中,生成
中,生成 或
或 的
的 的百分比).
的百分比).___________ .
A.随温度的升高, 平衡转化率逐渐增大
平衡转化率逐渐增大
B.水蒸气可调节一定温度下反应物与产物的分压,提高丁烯的平衡转化率
C.较低温度条件下,反应Ⅰ速率大于反应Ⅱ的速率
D.320~580℃范围内,升温, 的产率下降,
的产率下降, 产率升高
产率升高
②温度高于440℃时,丁烯转化率随温度变化不明显的可能原因是_____________ .
(3)文献显示,丁烯与 反应也可制丁二烯,可分两步实现:
反应也可制丁二烯,可分两步实现:
反应Ⅲ
反应Ⅳ
600℃时,恒定总压0.10MPa、以起始物质的量均为1mol的 、
、 投料,达平衡时,测得
投料,达平衡时,测得 和
和 的转化率分别为80%、10%.600℃时,反应Ⅳ的平衡常数
的转化率分别为80%、10%.600℃时,反应Ⅳ的平衡常数
_________ .
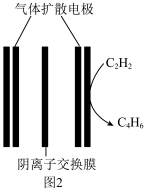
(4)有人设计一种电解装置,用乙炔合成二丁烯 的装置如图2.电解质溶液为
的装置如图2.电解质溶液为 溶液.
溶液. 的电极的电极反应式:
的电极的电极反应式:____________ 。
②用 溶液吸收阳极逸出的气体再生电解质溶液。不考虑气体溶解残留.当电路中转移
溶液吸收阳极逸出的气体再生电解质溶液。不考虑气体溶解残留.当电路中转移 时,计算再生液的
时,计算再生液的
____________ 。(已知 的电离常数
的电离常数 ,
, )
)
反应Ⅰ
反应Ⅱ
回答下列问题:
(1)判断反应Ⅱ的自发性并说明理由
(2)在常压、催化剂作用下,投料按
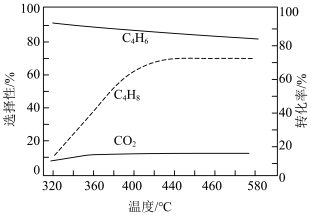
图1
①根据图1的相关信息,下列说法正确的是A.随温度的升高,
B.水蒸气可调节一定温度下反应物与产物的分压,提高丁烯的平衡转化率
C.较低温度条件下,反应Ⅰ速率大于反应Ⅱ的速率
D.320~580℃范围内,升温,
②温度高于440℃时,丁烯转化率随温度变化不明显的可能原因是
(3)文献显示,丁烯与
反应Ⅲ
反应Ⅳ
600℃时,恒定总压0.10MPa、以起始物质的量均为1mol的
(4)有人设计一种电解装置,用乙炔合成二丁烯
②用
23-24高三下·浙江·开学考试
类题推荐
甲醇是一种可再生能源,用 和
和 合成甲醇的过程主要有以下反应:
合成甲醇的过程主要有以下反应:
反应I:

反应II:

反应III:

请回答:
(1)反应III自发进行的条件是___________ 。
(2)恒温恒容条件下,若仅发生反应II,反应达到平衡的标志是___________。
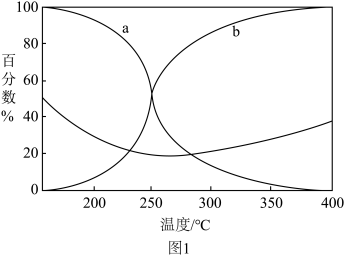
(3)在5.0MPa恒定压强和催化剂作用下,以 的投入量进行反应,体系到达平衡后的CO与
的投入量进行反应,体系到达平衡后的CO与 在含碳产物中的物质的量百分数、
在含碳产物中的物质的量百分数、 转化率随温度的变化如图1所示。
转化率随温度的变化如图1所示。 在含碳产物中物质的量百分数的曲线是
在含碳产物中物质的量百分数的曲线是___________ (填a或b)。
② 平衡转化率随温度的升高先减小后增大,增大的原因可能是
平衡转化率随温度的升高先减小后增大,增大的原因可能是___________ 。
(4)反应I、III的逆过程又称为甲醇水蒸气重整,是电动汽车常见的氢源。在常压、CaO催化下, 和
和 以体积比1:1.2混合,总物质的量为2.2mol,反应至
以体积比1:1.2混合,总物质的量为2.2mol,反应至 时刻测得
时刻测得 转化率及CO、
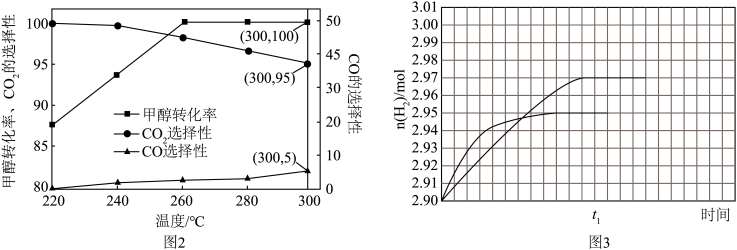
转化率及CO、 选择性随温度变化分别如图2所示,260℃时
选择性随温度变化分别如图2所示,260℃时 的物质的量随时间的变化曲线如图3所示。
的物质的量随时间的变化曲线如图3所示。___________ 。
A.反应适宜温度为300℃
B.工业生产通常在高压条件下进行甲醇水蒸气重整
C.CaO催化剂具有更高催化活性,可以提高甲醇平衡转化率
D.其他条件不变,适当升高温度有利于提高 的产率
的产率
②通过计算在图3中画出300℃时,反应至 时刻
时刻 物质的量随时间变化的曲线。
物质的量随时间变化的曲线。___________
反应I:
反应II:
反应III:
请回答:
(1)反应III自发进行的条件是
(2)恒温恒容条件下,若仅发生反应II,反应达到平衡的标志是___________。
| A.CO的分压不再发生变化 | B.气体平均相对分子质量不再发生变化 |
| C.气体密度不再发生变化 | D. |
(3)在5.0MPa恒定压强和催化剂作用下,以
②
(4)反应I、III的逆过程又称为甲醇水蒸气重整,是电动汽车常见的氢源。在常压、CaO催化下,
A.反应适宜温度为300℃
B.工业生产通常在高压条件下进行甲醇水蒸气重整
C.CaO催化剂具有更高催化活性,可以提高甲醇平衡转化率
D.其他条件不变,适当升高温度有利于提高
②通过计算在图3中画出300℃时,反应至
丙烯是一种重要的化工原料,在催化剂作用下,可以由丙烷直接脱氢或氧化脱氢制备。
反应Ⅰ(直接脱氢):

反应Ⅱ(氧化脱氢):

反应Ⅲ(氢气燃烧):

(1)
_____ kJ/mol。
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
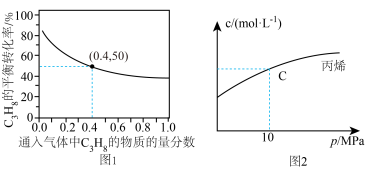
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1
①结合图1,从平衡移动的角度分析,“通入Ar”的作用是_____ 。
②若要将 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
_____ 。
(3)恒温条件下,测得反应Ⅰ平衡时 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线_____ 。(在图中C点平衡总压为10Mpa时,丙烷和丙烯的物质的浓度相等)。
(4)①关于反应Ⅲ,下列说法正确的是_____ 。
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高 的转化率
的转化率
②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是_____ 。
(5)研究表明, 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
下列说法不正确的是_____。
反应Ⅰ(直接脱氢):
反应Ⅱ(氧化脱氢):
反应Ⅲ(氢气燃烧):
(1)
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入
①结合图1,从平衡移动的角度分析,“通入Ar”的作用是
②若要将
(3)恒温条件下,测得反应Ⅰ平衡时
(4)①关于反应Ⅲ,下列说法正确的是
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高
②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是
(5)研究表明,
| t℃ | 丙烷转化率 | 产物的选择性 | ||
| CO | ||||
| 400 | 4.06 | 93.12 | 2.20 | 4.68 |
| 500 | 12.32 | 91.23 | 3.16 | 5.61 |
| 600 | 35.22 | 85.44 | 7.73 | 6.83 |
| A.在较高温度下,催化剂X可提高产生丙烯反应的速率 |
| B. |
| C.相同条件下,使用不同的催化剂,丙烷的平衡转化率相同 |
| D.温度升高,催化剂X的活性下降,丙烯的产率降低 |
丙烯是一种重要的化工原料,其主要产品聚丙烯是生产口罩喷溶布的原料。铬基催化剂下丙烷生产丙烯相关主要反应有:
Ⅰ.
Ⅱ.
Ⅲ.
请回答:
(1)已知键能: ,
, 。C=C的键能与C-C的键能相差约
。C=C的键能与C-C的键能相差约___________ kJ/mol。
(2)600℃时,容器压强恒为P,铬基催化剂下两个密闭容器中分别按下表投料发生反应:
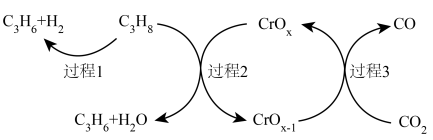
①容器B生成C3H6的反应流程如下:________ 。
A.原料气中通入N2可提高C3H8的平衡转化率
B.升高温度,一定能提高的C3H6平衡产率
C.过程1产生C3H6的量大于过程2和过程3产生的C3H6
D.在铬基催化剂中适当加入CaO可促进过程2平衡正移而提高C3H8的平衡转化率
②若容器A中只发生反应Ⅰ和反应Ⅱ,C3H8的平衡转化率为 ,C3H6的选择性(选择性
,C3H6的选择性(选择性 )为w,计算反应Ⅰ的平衡常数
)为w,计算反应Ⅰ的平衡常数
________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③按照容器A和容器B的气体组分比,将两组气体按相同流速分别通过催化剂固定床反应器,C3H8的转化率和C3H6的选择性随时间变化如图所示:________ ,B组中CO2的作用是________ (用化学方程式和必要的文字说明)。
(3)恒温恒容的密闭容器中通入气体分压比为 的混合气体,
的混合气体, ,已知某反应条件下只发生反应Ⅳ和反应Ⅴ(
,已知某反应条件下只发生反应Ⅳ和反应Ⅴ( ,
, 为速率常数,只与温度有关且
为速率常数,只与温度有关且 ):
):
反应Ⅳ:
反应Ⅴ:
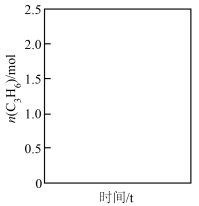
实验测得丙烯的净生成速率方程为 ,请在下图中画出丙烯的物质的量随时间的变化趋势
,请在下图中画出丙烯的物质的量随时间的变化趋势____________ 。
Ⅰ.
Ⅱ.
Ⅲ.
请回答:
(1)已知键能:
(2)600℃时,容器压强恒为P,铬基催化剂下两个密闭容器中分别按下表投料发生反应:
| 容器 | C3H8/mol | CO2/mol | N2/mol |
| A | 1 | 0 | 10 |
| B | 1 | 2 | 8 |
A.原料气中通入N2可提高C3H8的平衡转化率
B.升高温度,一定能提高的C3H6平衡产率
C.过程1产生C3H6的量大于过程2和过程3产生的C3H6
D.在铬基催化剂中适当加入CaO可促进过程2平衡正移而提高C3H8的平衡转化率
②若容器A中只发生反应Ⅰ和反应Ⅱ,C3H8的平衡转化率为
③按照容器A和容器B的气体组分比,将两组气体按相同流速分别通过催化剂固定床反应器,C3H8的转化率和C3H6的选择性随时间变化如图所示:

(3)恒温恒容的密闭容器中通入气体分压比为
反应Ⅳ:
反应Ⅴ:
实验测得丙烯的净生成速率方程为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


