解答题-原理综合题 适中0.65 引用1 组卷57
回答下列问题:
(1)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。
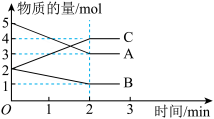
①该反应的化学方程式为_______ 。
②反应开始至2min时,B的平均反应速率为_______ 。
(2)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
①请完成此实验设计:其中
_______ ,
_______ 。
②该同学最后得出的结论为当加入少量 溶液时,生成氢气的速率会大大提高,但当加入的
溶液时,生成氢气的速率会大大提高,但当加入的 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:_______ 。
(3)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO: 。已知该反应的
。已知该反应的 ,该设想能否实现?
,该设想能否实现?_______ (填“能”或“否”),依据是:_______ 。
(1)某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。

①该反应的化学方程式为
②反应开始至2min时,B的平均反应速率为
(2)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积气体所需的时间。
实验 混合溶液 | A | B | C | D | E | F |
| 4 mol·L | 30 | |||||
| 饱和 | 0 | 0.5 | 2.5 | 5 | 20 | |
| 10 | 0 |
②该同学最后得出的结论为当加入少量
(3)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
23-24高二下·甘肃武威·开学考试
类题推荐
某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如图所示(已知A、B、C均为气体)。
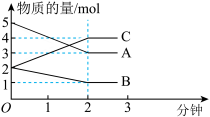
(1)该反应的化学方程式为_______ 。
(2)反应开始至2分钟时,B的平均反应速率为_______ 。
(3)由图求得平衡时A的转化率为_______ 。
(4)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
请完成此实验设计,其中:V1=_______ ,V6=_______ 。

(1)该反应的化学方程式为
(2)反应开始至2分钟时,B的平均反应速率为
(3)由图求得平衡时A的转化率为
(4)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验混合溶液 | A | B | C | D | E | F |
| 4mol/L H2SO4(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
请完成此实验设计,其中:V1=
研究化学反应速率与限度,有利于人类的生产。
Ⅰ.在T℃时,某反应在体积为2L的恒容密闭的容器中进行,各物质的量随时间的变化情况如图所示 已知A、B、C均为气体
已知A、B、C均为气体 .
.
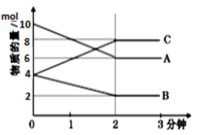
(1)该反应的化学方程式为_______________
(2)反应开始至2分钟时,C的平均反应速率为_____ mol·L-1·min-1
(3)能说明该反应已达到平衡状态的是________
A. B.
B. C.容器内气体密度不变 D.各组分的物质的量相等 E.容器内气体压强不变
C.容器内气体密度不变 D.各组分的物质的量相等 E.容器内气体压强不变
(4)由图求得平衡时B的物质的量分数为_______________
Ⅱ.某学生探究加入硫酸铜的量对锌与硫酸反应生成H2速率的影响,设计实验如下:
将表中所给的混合溶液分别加入到5个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。(忽略混合时溶液体积变化)
(5)请完成此实验设计,其中:
______ ,
______
(6)该同学最后得出的结论为:当加入少量 溶液时,生成氢气的速率会大大提高,请分析氢气生成速率提高的主要原因
溶液时,生成氢气的速率会大大提高,请分析氢气生成速率提高的主要原因_____________________
Ⅰ.在T℃时,某反应在体积为2L的恒容密闭的容器中进行,各物质的量随时间的变化情况如图所示

(1)该反应的化学方程式为
(2)反应开始至2分钟时,C的平均反应速率为
(3)能说明该反应已达到平衡状态的是
A.
(4)由图求得平衡时B的物质的量分数为
Ⅱ.某学生探究加入硫酸铜的量对锌与硫酸反应生成H2速率的影响,设计实验如下:
将表中所给的混合溶液分别加入到5个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。(忽略混合时溶液体积变化)
| 实验混合溶液 | A | B | C | D | E |
| 40 | |||||
| 饱和 | 0 | 10 | |||
| 0 |
(5)请完成此实验设计,其中:
(6)该同学最后得出的结论为:当加入少量
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有__ 。
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=__ ,V6=__ ,V9=__ ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因__ 。
(1)上述实验中发生反应的化学方程式有
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需时间。
| A | B | C | D | E | F | |
| 4mol·L-1H2SO4溶液/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


