解答题-原理综合题 较难0.4 引用1 组卷55
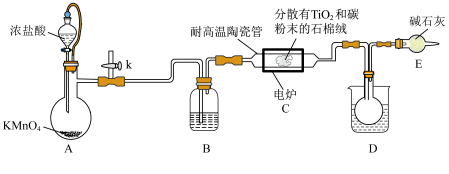
钛在医疗领域的应用非常广泛,如制人造关节、头盖、主动心瓣等, 是制备金属钛的重要中间体,某小组同学利用如图所示的装置在实验室制备
是制备金属钛的重要中间体,某小组同学利用如图所示的装置在实验室制备 (夹持装置略去).
(夹持装置略去). 易挥发,高温时能与
易挥发,高温时能与 反应,不与
反应,不与 反应,其他相关信息如表所示(
反应,其他相关信息如表所示( 为副产物):
为副产物):
回答下列问题:
(1)装置B中所盛试剂为___________ .
(2)组装好仪器后,部分实验步骤如下:
a.装入药品 b.打开分液漏斗活塞
c.检查装置气密性 d.关闭分液漏斗活塞
e.停止加热,充分冷却 f.加热装置C中陶瓷管
从上述选项中选择合适操作(不重复使用)并排序:___________ .
(3)若在反应前,先打开开关 ,从侧管持续通入一段时间的
,从侧管持续通入一段时间的 ,其目的是
,其目的是___________ ;装置C中除生成 外,还生成一种气态不成盐氧化物,该反应的化学方程式为
外,还生成一种气态不成盐氧化物,该反应的化学方程式为___________ ,判断该制备反应结束的实验现象是___________ .
(4)下列说法错误的是___________(填选项字母).
(5) 可用于制备纳米
可用于制备纳米 :以
:以 为载体,用
为载体,用 和水蒸气反应生成
和水蒸气反应生成 ,再控制温度生成纳米
,再控制温度生成纳米 .测定产物
.测定产物 组成的方法如下:
组成的方法如下:
步骤一:取样品 ,用稀硫酸充分溶解得到
,用稀硫酸充分溶解得到 ,再用足量铝将
,再用足量铝将 还原为
还原为 ,过滤并洗涤,将所得滤液和洗涤液合并注入
,过滤并洗涤,将所得滤液和洗涤液合并注入 容量瓶,定容得到待测液.
容量瓶,定容得到待测液.
步骤二:取待测液 于锥形瓶中,加几滴
于锥形瓶中,加几滴 溶液作指示剂,用
溶液作指示剂,用 的
的 标准溶液滴定,将
标准溶液滴定,将 氧化为
氧化为 ,三次滴定消耗标准溶液体积的平均值为
,三次滴定消耗标准溶液体积的平均值为 .通过分析、计算,该样品中
.通过分析、计算,该样品中
___________ .
| 熔点/℃ | 沸点/℃ | 密度 | 水溶性 | |
| 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 | ||
| 76.8 | 1.6 | 难溶于水 |
(1)装置B中所盛试剂为
(2)组装好仪器后,部分实验步骤如下:
a.装入药品 b.打开分液漏斗活塞
c.检查装置气密性 d.关闭分液漏斗活塞
e.停止加热,充分冷却 f.加热装置C中陶瓷管
从上述选项中选择合适操作(不重复使用)并排序:
(3)若在反应前,先打开开关
(4)下列说法错误的是___________(填选项字母).
| A.该装置有缺陷,通过装置 |
| B.石棉线载体是为了增大气体与 |
| C.装置D的烧杯中可加入冰水,便于收集到纯的液态 |
| D.装置 |
(5)
步骤一:取样品
步骤二:取待测液
23-24高三下·山东·开学考试
类题推荐
钛在医疗领域的应用非常广泛,如制人造关节、头盖、主动心瓣等。TiCl4是制备金属钛的重要中间体。某小组同学利用如下装置在实验室制备TiCl4 (夹持装置略去)。

资料表明:室温下,TiCl4为无色液体,易挥发,高温时能与 反应,与HCl不发生反应。其他相关信息如下表所示:
反应,与HCl不发生反应。其他相关信息如下表所示:
请回答下列问题:
(1)A装置中仪器b的名称是_______ ,B装置中的试剂是_______ ,E装置的作用是_______ 。
(2)组装好仪器后,部分实验操作步骤如下:①装入药品 ②打开分液漏斗活塞 ③检查装置气密性 ④关闭分液漏斗活塞 ⑤停止加热,充分冷却 ⑥加热装置C中陶瓷管。符合题意的操作顺序依次为:③①_______ 。(填操作序号)
(3)装置C中除生成TiCl4外,同时还生成一种常见气态不成盐氧化物,该反应的化学方程式为_______ 。
(4)下列说法不正确的是_______ (填序号)。
A.通入氯气之前,必须先从k处通入氮气,否则实验会失败
B.石棉绒载体是为了增大气体与 、炭粉的接触面积,以加快反应速率
、炭粉的接触面积,以加快反应速率
C.装置D的锥形瓶中可能会有少量 ,可用蒸馏的方法分离除去
,可用蒸馏的方法分离除去
D.装置D中的冷却水应从d口通入
E.该实验装置还有缺陷,通过装置F后的气体不可直接排放到空气中
(5)利用下图装置测定所得TiCl4的纯度:取wg产品TiCl4加入烧瓶,向安全漏斗中加入适量蒸馏水,待TiCl4充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴 溶液作指示剂(
溶液作指示剂( 呈砖红色),用
呈砖红色),用 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 。
。

[已知:常温下, ,
, ;
; ]根据上述数据计算该产品纯度为
]根据上述数据计算该产品纯度为_______ (用含w、c和V的代数式表示)。

资料表明:室温下,TiCl4为无色液体,易挥发,高温时能与
| 物质 | 熔点/℃ | 沸点/℃ | 水溶性 |
| TiCl4 | -25 | 136.4 | 易水解生成白色沉淀,能溶于有机溶剂 |
| -23 | 76.8 | 难溶于水 |
(1)A装置中仪器b的名称是
(2)组装好仪器后,部分实验操作步骤如下:①装入药品 ②打开分液漏斗活塞 ③检查装置气密性 ④关闭分液漏斗活塞 ⑤停止加热,充分冷却 ⑥加热装置C中陶瓷管。符合题意的操作顺序依次为:③①
(3)装置C中除生成TiCl4外,同时还生成一种常见气态不成盐氧化物,该反应的化学方程式为
(4)下列说法不正确的是
A.通入氯气之前,必须先从k处通入氮气,否则实验会失败
B.石棉绒载体是为了增大气体与
C.装置D的锥形瓶中可能会有少量
D.装置D中的冷却水应从d口通入
E.该实验装置还有缺陷,通过装置F后的气体不可直接排放到空气中
(5)利用下图装置测定所得TiCl4的纯度:取wg产品TiCl4加入烧瓶,向安全漏斗中加入适量蒸馏水,待TiCl4充分反应后,将烧瓶和漏斗中的液体一并转入锥形瓶中,滴加几滴

[已知:常温下,
金属钛在医疗领域的使用非常广泛,可以应用在人体骨骼、组织移植和再造,如制人造髋关节、膝关节、头盖骨。主动心瓣等。TiCl4是制备金属钛的重要中间体,某小组同学利用如下装置在实验室制备TiCl4(夹持装置略去)。

相关信息如下表所示:
请回答下列问题:
(1)仪器b的名称为_______ ,装置A中导管a的作用为_______ 。装置B中所装试剂为_______ ,装置A中发生反应的离子方程式为_______ 。
(2)装置C中除生成TiCl4外,同时还生成一种气态不成盐氧化物,该反应的化学方程式为_______ 。制得的TiCl4中常含有少量CCl4,从混合液体中分离出TiCl4的操作名称为_______ 。
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;_______ (按正确的顺序填入下列操作的序号)。
①打开分液漏斗活塞
②关闭分液漏斗活塞
③停止加热,充分冷却
④加热装置C中陶瓷管
(4)设计实验证明装置D中收集到的液体中含有TiCl4:_______ 。
(5)TiCl4可制备纳米TiO2:以N2为载体,用TiCl4和水蒸气反应生成Ti(OH)4。再控制温度生成纳米xTiO2∙yH2O。测定产物xTiO2∙yH2O组成的方法如下:
步骤一:取样品2.100g,在酸性条件下充分溶解,并用适量铝将TiO2+还原为Ti3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液。
步骤二:取待测液25.00mL于锥形瓶中,加几淌KSCN溶液作指示剂,用0.1000mol·L-1的NH4Fe(SO4)2标准溶液滴定,将Ti3+氧化为TiO2+。重复滴定2次。滴定所得的相关数据如下表:
①步骤一中用稀硫酸而不用水定容的原因是_______ 。
②通过计算确定该样品的组成为_______ 。

相关信息如下表所示:
| 熔点/℃ | 沸点/℃ | 密度/(g∙cm-3) | 水溶性 | |
| TiCl4 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
| CCl4 | -23 | 76.8 | 1.6 | 难溶于水 |
(1)仪器b的名称为
(2)装置C中除生成TiCl4外,同时还生成一种气态不成盐氧化物,该反应的化学方程式为
(3)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;
①打开分液漏斗活塞
②关闭分液漏斗活塞
③停止加热,充分冷却
④加热装置C中陶瓷管
(4)设计实验证明装置D中收集到的液体中含有TiCl4:
(5)TiCl4可制备纳米TiO2:以N2为载体,用TiCl4和水蒸气反应生成Ti(OH)4。再控制温度生成纳米xTiO2∙yH2O。测定产物xTiO2∙yH2O组成的方法如下:
步骤一:取样品2.100g,在酸性条件下充分溶解,并用适量铝将TiO2+还原为Ti3+,过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,并用稀硫酸定容,得待测液。
步骤二:取待测液25.00mL于锥形瓶中,加几淌KSCN溶液作指示剂,用0.1000mol·L-1的NH4Fe(SO4)2标准溶液滴定,将Ti3+氧化为TiO2+。重复滴定2次。滴定所得的相关数据如下表:
| 滴定序号 | 待测液体积/mL | NH4Fe(SO4)2标准溶液滴定管起点读数/mL | NH4Fe(SO4)2标准溶液滴定管终点读数/mL |
| 1 | 25.00 | 0.02 | 24.02 |
| 2 | 25.00 | 0.08 | 24.06 |
| 3 | 25.00 | 0.12 | 24.14 |
②通过计算确定该样品的组成为
钛在医疗领域的应用非常广泛,如制造人造关节、头盖骨、心脏瓣膜等。 是制备金属钛的重要中间体。某小组同学利用如图所示装置在实验室制备
是制备金属钛的重要中间体。某小组同学利用如图所示装置在实验室制备 (夹持装置略去)。
(夹持装置略去)。
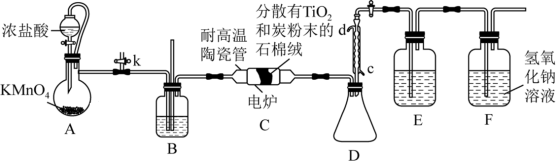
资料表明:室温下, 为无色液体,易挥发高温时能与
为无色液体,易挥发高温时能与 反应,与HCl不发生反应。其他相关信息如表所示:
反应,与HCl不发生反应。其他相关信息如表所示:
注释:①指题目难度星级,满星级为5颗,下同。
请回答下列问题:
(1)装置A中发生反应的化学方程式是___________ ,装置B的作用是___________ 。
(2)组装好仪器后,部分实验操作步骤如下:①装入药品;②打开分液漏斗活塞;③检查装置气密性;④关闭分液漏斗活塞;⑤停止加热,充分冷却;⑥加热装置C中陶瓷管。符合题意的操作顺序依次为③①___________ (填操作序号)。
(3)装置C中石棉绒载体的作用为___________ 。装置C中除生成 外,同时还生成一种常见气态不成盐氧化物,该反应的化学方程式为
外,同时还生成一种常见气态不成盐氧化物,该反应的化学方程式为___________ 。
(4)装置E中试剂为___________ ,作用是___________ 。
(5)下列说法不正确的是___________(填标号)。

资料表明:室温下,
注释:①指题目难度星级,满星级为5颗,下同。
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
| -25 | 136.4 | 易水解生成白色沉淀,能溶于有机溶剂 | |
| -23 | 76.8 | 难溶于水 |
(1)装置A中发生反应的化学方程式是
(2)组装好仪器后,部分实验操作步骤如下:①装入药品;②打开分液漏斗活塞;③检查装置气密性;④关闭分液漏斗活塞;⑤停止加热,充分冷却;⑥加热装置C中陶瓷管。符合题意的操作顺序依次为③①
(3)装置C中石棉绒载体的作用为
(4)装置E中试剂为
(5)下列说法不正确的是___________(填标号)。
| A.通入氯气之前,必须先从k处通入氮气,否则实验会失败 |
| B.装置D的锥形瓶中可能会有少量 |
| C.装置D中的冷却水应从d口通入 |
| D.该实验装置还有缺陷,通过装置F后的气体不可直接排放到空气中 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


