填空题 较难0.4 引用1 组卷281
2024高三下·全国·专题练习
类题推荐
Ⅰ.为了研究化学反应 的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到
的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到 形管中左侧液面下降,右侧液面上升:
形管中左侧液面下降,右侧液面上升:___________ (填“高”或“低”)。
Ⅱ.同素异形体相互转化的反应热相当小,而且转化速率较慢,有时还转化不完全,测定反应热很困难。现在可根据盖斯定律来计算反应热。
已知:①
②
(2)白磷转化为红磷的热化学方程式为___________ 。
(3)相同状况下,白磷的稳定性比红磷___________ (填“强”或“弱”)。
Ⅲ. 为空间四面体构型的分子,可看做是
为空间四面体构型的分子,可看做是 分子中的两个
分子中的两个 原子被
原子被 原子取代的物质;
原子取代的物质;
已知:①
②
相关化学键的键能数据如下:
(4)用 表示
表示 :
:___________ 。
(5)用 、
、 表示
表示 的
的 :
:___________ 。

Ⅱ.同素异形体相互转化的反应热相当小,而且转化速率较慢,有时还转化不完全,测定反应热很困难。现在可根据盖斯定律来计算反应热。
已知:①
②
(2)白磷转化为红磷的热化学方程式为
(3)相同状况下,白磷的稳定性比红磷
Ⅲ.
已知:①
②
相关化学键的键能数据如下:
| 化学键 | ||||
| 键能 |
(4)用
(5)用
氮的化合物广泛应用于工业、航天、医药等领域。
(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g)+4NH3(g) 5N2(g)+6H2O(g)。该反应已达到平衡状态的标志是
5N2(g)+6H2O(g)。该反应已达到平衡状态的标志是____ 。
a.反应速率v(NO)=v(H2O) b.容器内压强不再变化
c.容器内N2的物质的量分数不再变化 d.混合气体的密度不变
e.12molN-H键断裂的同时生成5molN≡N键 f.混合气体的平均相对分子质量不再改变
(2)肼(N2H4)是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键的键能如表:
则1molN2H4(g)在氧气中完全燃烧的热化学方程式___ 。
(3)一定条件下,在5L密闭容器内,反应2NO2(g) N2O4(g),NO2的物质的量随时间变化如表:
N2O4(g),NO2的物质的量随时间变化如表:
①用N2O4表示0~2s内该反应的平均速率为___ mol·L−1·s−1.达平衡时,该反应的平衡常数K=___ 。
②为加快反应速率,可以采取的措施是____ 。
a.升高温度 b.恒容时充入He(g) c.恒压时充入He(g) d.恒容时充入NO2
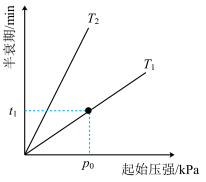
(4)已知:2N2O=2N2+O2,不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1_____ T2(填“>”、“=”或“<”)。当温度为T1、起始压强为p0,反应至t1min时,此时体系压强p=____ (用p0表示)。
(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3,在一定条件下发生反应:6NO(g)+4NH3(g)
a.反应速率v(NO)=v(H2O) b.容器内压强不再变化
c.容器内N2的物质的量分数不再变化 d.混合气体的密度不变
e.12molN-H键断裂的同时生成5molN≡N键 f.混合气体的平均相对分子质量不再改变
(2)肼(N2H4)是火箭的高能燃料,该物质燃烧时生成水蒸气和氮气,已知某些化学键的键能如表:
| 化学键 | O-H | N-N | N-H | O=O | N≡N |
| 键能kJ·mol-1 | 467 | 160 | 391 | 498 | 945 |
(3)一定条件下,在5L密闭容器内,反应2NO2(g)
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
②为加快反应速率,可以采取的措施是
a.升高温度 b.恒容时充入He(g) c.恒压时充入He(g) d.恒容时充入NO2
(4)已知:2N2O=2N2+O2,不同温度(T)下,N2O分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度N2O消耗一半时所需的相应时间),则T1
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网



