解答题-结构与性质 较难0.4 引用1 组卷241
卤素在高分子材料及电子电气等领域都有广泛应用。
(1)卤族元素位于元素周期表的___________ 区,基态溴原子的价层电子排布式为___________ 。
(2)比较键角大小:NH3___________ NF3(填“>”“<”或“=”)。
(3)已知下列5种羧酸:①CF3COOH②CH3COOH③CH2FCOOH④CH2ClCOOH⑤CH3CH2COOH,其酸性由强到弱的顺序为①___________ (填序号)。
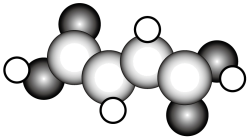
(4)已知:由于 中甲基的推电子诱导效应,π电子离1号碳更近,H+倾向于与电子密度更高的1号碳结合,丙烯与HCl加成的主产物为CH3CHClCH3.,CF3CH=CH2与HCl加成反应主产物的结构简式为
中甲基的推电子诱导效应,π电子离1号碳更近,H+倾向于与电子密度更高的1号碳结合,丙烯与HCl加成的主产物为CH3CHClCH3.,CF3CH=CH2与HCl加成反应主产物的结构简式为___________ 。
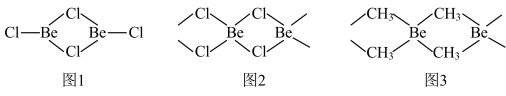
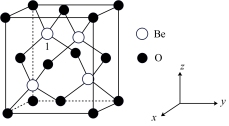
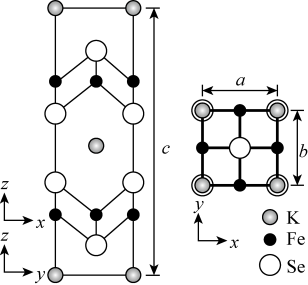
(5)图1为气态氯化铍,图2为固态氯化铍。
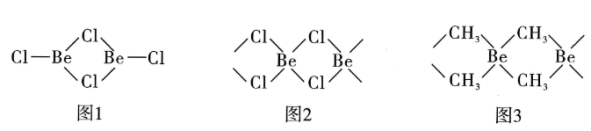
①气态氯化铍为___________ (填“极性”或“非极性”)分子。氯化铍由气态转化为固态,Be的杂化方式由___________ 转化为___________ 。
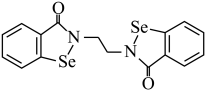
②若将固态氯化铍中的Cl原子替换为甲基,可形成如图3化合物。1个甲基与2个Be原子形成共价键时所提供的电子数为___________ 。
(1)卤族元素位于元素周期表的
(2)比较键角大小:NH3
(3)已知下列5种羧酸:①CF3COOH②CH3COOH③CH2FCOOH④CH2ClCOOH⑤CH3CH2COOH,其酸性由强到弱的顺序为①
(4)已知:由于
(5)图1为气态氯化铍,图2为固态氯化铍。

①气态氯化铍为
②若将固态氯化铍中的Cl原子替换为甲基,可形成如图3化合物。1个甲基与2个Be原子形成共价键时所提供的电子数为
23-24高二上·陕西·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网