解答题-实验探究题 适中0.65 引用1 组卷56
某小组将浓盐酸和 混合加热生成氯气,发现氯气不再逸出时,固液混合物A中仍存在盐酸和
混合加热生成氯气,发现氯气不再逸出时,固液混合物A中仍存在盐酸和 ,回答下列问题。
,回答下列问题。
(1)写出反应中生成氯气的离子方程式___________ 。
(2)一个氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应),第(1)题中的离子方程式可分为下面两个反应式:
i.氧化反应:
ii.还原反应:_______
 ___________
___________ ___________
___________
(3)根据两个半反应的反应式,分析A中仍存在盐酸和 的原因。
的原因。
i.随 降低,
降低, 还原性减弱
还原性减弱
ii.随 降低或
降低或 浓度升高,
浓度升高,___________ 。
(4)补充实验证实了(3)中的分析。
a是___________ ,b是___________ 。
(5)利用 浓度对
浓度对 氧化性的影响,探究同周期非金属元素阴离子的还原性。相同浓度的NaCl和
氧化性的影响,探究同周期非金属元素阴离子的还原性。相同浓度的NaCl和 溶液,能与
溶液,能与 反应所需
反应所需 较小的是
较小的是___________ 。
(6)该小组查资料得知:氧化还原反应电位传感器可以测量不同溶液的电位值。根据电位值大小可比较物质的氧化性或者还原性强弱:数值越大,氧化性越强;数值越小,还原性越强。由此推知 的以下物质溶液的电位值大小(填“<”“>”或“=”)
的以下物质溶液的电位值大小(填“<”“>”或“=”)
①KI___________ KBr
②
___________  (酸化)
(酸化)
(1)写出反应中生成氯气的离子方程式
(2)一个氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应),第(1)题中的离子方程式可分为下面两个反应式:
i.氧化反应:
ii.还原反应:
(3)根据两个半反应的反应式,分析A中仍存在盐酸和
i.随
ii.随
(4)补充实验证实了(3)中的分析。
| 实验操作 | 试剂 | 产物 | |
| I | 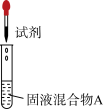 | 较浓 | 有氯气 |
| Ⅱ | a | 有氯气 | |
| Ⅲ | a和b | 无氯气 |
(5)利用
(6)该小组查资料得知:氧化还原反应电位传感器可以测量不同溶液的电位值。根据电位值大小可比较物质的氧化性或者还原性强弱:数值越大,氧化性越强;数值越小,还原性越强。由此推知
①KI
②
23-24高一上·广东茂名·期末
类题推荐
某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是___________ 。
②电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:___________ 。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。
ii.随c(Cl-)降低,___________ 。
④补充实验证实了③中的分析。
a是___________ ,b是___________ 。
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是___________ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是___________ 。
(4)总结:物质氧化性和还原性变化的一般规律是___________ 。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是
②电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。
ii.随c(Cl-)降低,
④补充实验证实了③中的分析。
| 实验操作 | 试剂 | 产物 | |
| I |  | 较浓H2SO4 | 有氯气 |
| II | a | 有氯气 | |
| III | a+b | 无氯气 |
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)由大到小的顺序是
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是
(4)总结:物质氧化性和还原性变化的一般规律是
氧化还原反应包括氧化反应和还原反应两个过程(即两个半反应)。化学兴趣小组同学探究卤素参与的氧化还原反应,从半反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO2混合加热生成氯气。当氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式为___________ 。
②上述氧化还原反应方程式可分为两个半反应式。
I.还原反应: MnO2+2e- +4H+= Mn2+ +2H2O
II.氧化反应:___________ 。
③根据半反应式,分析A中仍存在盐酸和MnO2的原因。
I.随c(H+)降低或c(Mn2+)浓度升高,MnO2的氧化性减弱。
II.随c(Cl-)降低,Cl-的还原性___________ (选填 “增强”或“减弱”)。
④补充实验证实了③中的分析。
a是 ___________ 浓溶液,b是 ___________ 浓溶液(选择下列合适选项,填写对应序号)。
A. NaCl B. MnSO4 C. Na2SO4
(2)利用c(H+)浓度对MnO2氧化性的影响,探究同周期元素氢化物的还原性。相同浓度的HCl和H2S溶液,能与MnO2反应所需c(H+)较小的是___________ 。
(3)酸性条件下,反应Mn2+ + Br2+2H2O= MnO2↓+2Br- +4H+进行程度很小,加入AgNO3溶液后,该反应的进行程度明显增大。
①反应中氧化产物为___________ (填化学式) 。
②加入AgNO3溶液后该反应的进行程度明显增大的原因是___________ 。
(1)浓盐酸与MnO2混合加热生成氯气。当氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式为
②上述氧化还原反应方程式可分为两个半反应式。
I.还原反应: MnO2+2e- +4H+= Mn2+ +2H2O
II.氧化反应:
③根据半反应式,分析A中仍存在盐酸和MnO2的原因。
I.随c(H+)降低或c(Mn2+)浓度升高,MnO2的氧化性减弱。
II.随c(Cl-)降低,Cl-的还原性
④补充实验证实了③中的分析。
| 实验操作 | 试剂X | 产物 | |
| I | 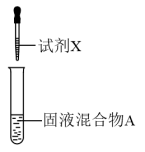 | 较浓硫酸 | 有氯气 |
| II | a | 有氯气 | |
| III | a+b | 无氯气 |
A. NaCl B. MnSO4 C. Na2SO4
(2)利用c(H+)浓度对MnO2氧化性的影响,探究同周期元素氢化物的还原性。相同浓度的HCl和H2S溶液,能与MnO2反应所需c(H+)较小的是
(3)酸性条件下,反应Mn2+ + Br2+2H2O= MnO2↓+2Br- +4H+进行程度很小,加入AgNO3溶液后,该反应的进行程度明显增大。
①反应中氧化产物为
②加入AgNO3溶液后该反应的进行程度明显增大的原因是
某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是__ 。
②电极反应式:i.还原反应:MnO2+2e-+4H+=Mn2++2H2O;ii.氧化反应:__ 。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。ii.随c(Cl-)降低,__ 。
④补充实验证实了③中的分析。
a是__ ,b是__ 。
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)最小的是__ ,从原子结构角度说明理由__ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高Br2的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是__ 。
(4)总结:物质氧化性和还原性随反应物和生成物浓度变化的一般规律是:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越___ (选填“强”或“弱”,下同),还原产物(氧化产物)的浓度越大,对应的氧化剂(还原剂)的氧化性(还原性)越___ 。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是
②电极反应式:i.还原反应:MnO2+2e-+4H+=Mn2++2H2O;ii.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。ii.随c(Cl-)降低,
④补充实验证实了③中的分析。
| 实验操作 | 试剂 | 产物检测 | |
| I | 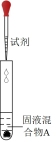 | 较浓H2SO4 | 有Cl2 |
| II | a | 有Cl2 | |
| III | a+b | 无Cl2 |
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)最小的是
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高Br2的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是
(4)总结:物质氧化性和还原性随反应物和生成物浓度变化的一般规律是:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


