填空题 适中0.65 引用1 组卷63
用含有  和少量
和少量  的铝灰制备
的铝灰制备  ,工艺流程如下(部分操作和条件略):
,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀 ,过滤;
,过滤;
Ⅱ.向滤液中加入过量 溶液,调节溶液的
溶液,调节溶液的  约为3,生成红褐色沉淀;
约为3,生成红褐色沉淀;
Ⅲ.静置,上层溶液呈紫红色;
Ⅳ.加入 至紫红色消失,过滤;
至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
资料: 是酸性氧化物,能与碱反应,不与酸反应。
是酸性氧化物,能与碱反应,不与酸反应。
(1) 溶解铝灰涉及的离子反应方程式有
溶解铝灰涉及的离子反应方程式有_________________ 、_________________ 。
(2)将 氧化
氧化  离子方程式补充完整:
离子方程式补充完整:_________________
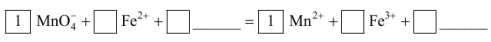
(3)已知:一定条件下, 可与
可与  反应生成
反应生成  。
。
①向Ⅲ的沉淀中加入浓 并加热,能说明沉淀中存在
并加热,能说明沉淀中存在  的现象是
的现象是_____________________________________ 。
②Ⅳ中加入 的目的是
的目的是_____________________________________ 。
Ⅰ.向铝灰中加入过量稀
Ⅱ.向滤液中加入过量
Ⅲ.静置,上层溶液呈紫红色;
Ⅳ.加入
Ⅴ.浓缩、结晶、分离,得到产品。
资料:
(1)
(2)将
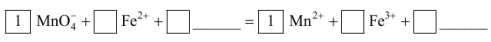
(3)已知:一定条件下,
①向Ⅲ的沉淀中加入浓
②Ⅳ中加入
23-24高一上·北京·期末
类题推荐
用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解Al2O3的离子方程式是_________________________________________ 。
(2)将MnO4-氧化Fe2+的离子方程式补充完整:MnO4-+_______ Fe2++_______ =Mn2++_______ Fe3++________ 。
(3)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释步骤Ⅱ的目的:____________________________________________ 。
(4)已知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是_____________ 。
②Ⅳ中加入MnSO4的目的是___________________________________________ 。
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解Al2O3的离子方程式是
(2)将MnO4-氧化Fe2+的离子方程式补充完整:MnO4-+
(3)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释步骤Ⅱ的目的:
(4)已知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是
②Ⅳ中加入MnSO4的目的是
用含有 和少量
和少量 的铝灰制备
的铝灰制备 ,工艺流程如下(部分操作和条件略)。
,工艺流程如下(部分操作和条件略)。
Ⅰ.向铝灰中加入过量稀 ,过滤;
,过滤;
Ⅱ.向滤液中加入过量 溶液,充分反应;
溶液,充分反应;
Ⅲ.调节溶液的 约为3,加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
约为3,加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入 至紫红色消失,过滤、浓缩、结晶、分离,得到产品。
至紫红色消失,过滤、浓缩、结晶、分离,得到产品。
已知:
①生成氢氧化物沉淀的
②一定条件下, 可与
可与 反应生成
反应生成
下列说法不正确 的是
Ⅰ.向铝灰中加入过量稀
Ⅱ.向滤液中加入过量
Ⅲ.调节溶液的
Ⅳ.加入
已知:
①生成氢氧化物沉淀的
开始沉淀时 | |||
完全沉淀时 |
下列说法
| A.Ⅰ中溶液中的阳离子有 |
| B.Ⅱ的目的是将 |
| C.Ⅲ中棕色沉淀含有 |
| D.Ⅳ中发生了反应: |
用含有A1203、SiO2和少量FeO·xFe2O3的铝灰制备A12(SO4)3·18H2O。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是_______________ 1;
(2)KMnO4-氧化Fe2+的离子方程式补充完整:______
 1MnO
1MnO +
+ Fe2++
Fe2++ ______=
______= Mn2++
Mn2++ Fe3++
Fe3++ ______
______
(3)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol·L-1
根据表中数据解释步骤Ⅱ的目的:._________________ ;
(4)已知:一定条件下,MnO 可与Mn2+反应生成MnO2,
可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是_____________ ;
②Ⅳ中加入MnSO4的目的是:______________ ;
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解A12O3的离子方程式是
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:.
(4)已知:一定条件下,MnO
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是
②Ⅳ中加入MnSO4的目的是:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


