解答题-原理综合题 适中0.65 引用1 组卷81
人类利用化学反应不仅可以创造新物质,还可以获取能量或实现不同形式能量之间的转化。回答下列问题:
(1)氨气是重要的化工原料,工业合成氨反应:N2 (g)+ 3H2(g) 2NH3(g)。已知在25℃、
2NH3(g)。已知在25℃、 时,拆开
时,拆开 键、
键、 键和
键和 键所需能量分别为946kJ、436kJ、和391kJ。
键所需能量分别为946kJ、436kJ、和391kJ。
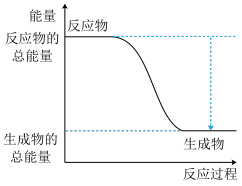
①根据上述数据判断,合成氨的反应是___________ 反应(填“吸热”或“放热”)。
②每消耗0.3molN2,反应放出或吸收的热量Q1=___________ kJ。
③将0.5molN2和4.5molH2充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为Q2kJ,则Q2___________ Q1 (填“>”“<”或“=”),理由是___________ 。
(2)科学家利用生物燃料电池原理研究室温下氨的合成并取得初步成果,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。
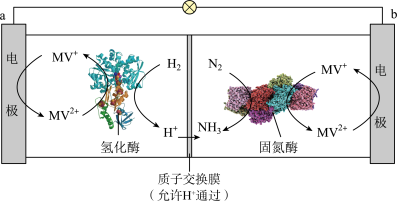
①b电极为___________ (填“正极”或“负极”),电极反应式为___________ 。
②电池工作时在固氮酶表面发生的反应为___________ 。
(1)氨气是重要的化工原料,工业合成氨反应:N2 (g)+ 3H2(g)
①根据上述数据判断,合成氨的反应是
②每消耗0.3molN2,反应放出或吸收的热量Q1=
③将0.5molN2和4.5molH2充入密闭容器中,在相同条件下发生该反应,达平衡时,放出或吸收的热量为Q2kJ,则Q2
(2)科学家利用生物燃料电池原理研究室温下氨的合成并取得初步成果,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。

①b电极为
②电池工作时在固氮酶表面发生的反应为
22-23高一下·山东淄博·阶段练习
类题推荐
工业上利用反应:N2(g) + 3H2(g)⇌2NH3(g)合成氨气。已知在1×105Pa和25℃时,拆开1mol N≡N键和1mol H-H键所需能量分别为946 kJ和436 kJ,生成1molN-H键放出的能量为391kJ。回答下列问题:
(1)根据上述数据判断,在1×105 Pa和25 ℃时,工业合成氨的反应是_______ 反应(填“吸热”或“放热”);每消耗1 molN2,反应放出或吸收的热量Q1为_______ kJ;1 molN2和3 molH2在该条件下反应,达平衡时,放出或吸收的热量为Q2 kJ,则Q2_______ Q1(填“>”“<”或“=”)。
(2)①合成氨反应在恒容密闭容器中进行,达到平衡后,只改变某一条件,下列说法正确的是_______ (填序号)。
a.升高温度,V(正)、V(逆)均增大 b.升高温度,V(正)增大,V(逆)减小
c.充入一定量的氮气,V(正)、V(逆)均增大 d.充入一定量的氩气,V(正)、V(逆)均增大
②下列叙述能说明上述反应已达化学平衡状态的是_______ (填序号)。
a.V正(N2)=V逆(NH3) b.n(N2)∶n(H2)∶n(NH3)=1∶3∶2
c.容器中气体的密度不随时间而变化 d.容器中气体的平均相对分子质量不随时间而变化
(3)一定温度下,将1 mol N2和3 mol H2置于1L的恒容密闭容器中反应,测得不同温度(T)、不同时间段内,容器中NH3的物质的量数据如下:
表中x、y的大小关系为x_______ y。(填“>”“<”“=”“≥”或“≤”)。
(1)根据上述数据判断,在1×105 Pa和25 ℃时,工业合成氨的反应是
(2)①合成氨反应在恒容密闭容器中进行,达到平衡后,只改变某一条件,下列说法正确的是
a.升高温度,V(正)、V(逆)均增大 b.升高温度,V(正)增大,V(逆)减小
c.充入一定量的氮气,V(正)、V(逆)均增大 d.充入一定量的氩气,V(正)、V(逆)均增大
②下列叙述能说明上述反应已达化学平衡状态的是
a.V正(N2)=V逆(NH3) b.n(N2)∶n(H2)∶n(NH3)=1∶3∶2
c.容器中气体的密度不随时间而变化 d.容器中气体的平均相对分子质量不随时间而变化
(3)一定温度下,将1 mol N2和3 mol H2置于1L的恒容密闭容器中反应,测得不同温度(T)、不同时间段内,容器中NH3的物质的量数据如下:
| 1小时 | 2小时 | 3小时 | 4小时 | |
| T3 | 0.38 mol | 0.49 mol | 0.56 mol | 0.56 mol |
| T4 | 0.42 mol | 0.51 mol | x mol | y mol |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网