解答题-工业流程题 适中0.65 引用1 组卷95
以硫铁矿(主要成分为 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下:
)的工艺流程如下:
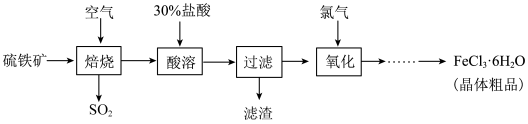
(1)焙烧产生的 可以继续制备硫酸,以下有关接触法制硫酸的论述错误的是___________。
可以继续制备硫酸,以下有关接触法制硫酸的论述错误的是___________。
(2)转化器是接触法制硫酸的核心场所,写出该场所发生的化学方程式:___________ 。
(3)热交换器是转化器中发挥着至关重要的作用,其中包括___________。
(4)酸溶时,不能用硫酸代替盐酸,原因:___________ 。
(5)“氧化”后,测得室温下溶液的pH=3,若忽略溶液中HCl的影响,相较于纯水,此时水的电离程度被___________ (填“促进”或“抑制”)了___________ 倍;若将溶液中HCl的影响考虑在内,则此时水的电离___________ 。
A.被促进 B.被抑制 C.无法直接判断

(1)焙烧产生的
| A.为提高反应速率和原料利用率,硫铁矿要在“沸腾”状态下燃烧 |
| B.为防止催化剂中毒,气体在进转化器前要先净化 |
| C.为提高 |
| D.吸收塔中 |
(2)转化器是接触法制硫酸的核心场所,写出该场所发生的化学方程式:
(3)热交换器是转化器中发挥着至关重要的作用,其中包括___________。
| A.预热未反应的气体,充分利用热能 |
| B.降低产物的温度,便于液化分离 |
| C.减小已达平衡的混合气体的压强,进一步提高产率 |
| D.降低已达平衡的混合气体温度,进一步提高转化率 |
(4)酸溶时,不能用硫酸代替盐酸,原因:
(5)“氧化”后,测得室温下溶液的pH=3,若忽略溶液中HCl的影响,相较于纯水,此时水的电离程度被
A.被促进 B.被抑制 C.无法直接判断
23-24高二上·上海·期末
类题推荐
硫酸在国民经济中占有极其重要的地位,工业上常用黄铁矿为原料接触法制硫酸。
(1)写出黄铁矿 在沸腾炉中与氧气发生反应的化学方程式
在沸腾炉中与氧气发生反应的化学方程式______ 。
(2)硫酸的生产中,下列说法不正确 的是______ 。
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400~500℃,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆流的形式, 从下而上,水从上而喷下
从下而上,水从上而喷下
(3)分别将1 mol的 、1.45 mol的
、1.45 mol的 通入
通入 、
、 和
和 恒压容器中发生反应:
恒压容器中发生反应:
 ,相同时间内测得
,相同时间内测得 的转化率
的转化率 随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强
随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强 )代替物质的量浓度
)代替物质的量浓度 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如 ,p为平衡总压强,
,p为平衡总压强, 为平衡系统中B的物质的量分数)。
为平衡系统中B的物质的量分数)。
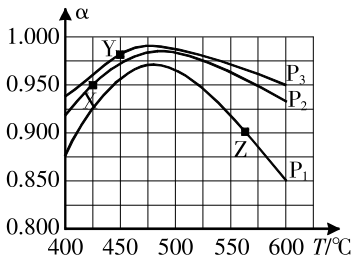
请回答:
①据图判断 、
、 、
、 的大小关系
的大小关系______ 。
②判断X、Y、Z中属于平衡点的是______ (填“X”、“Y”、“Z”),并计算该温度下平衡的
______ 。(用含 或
或 或
或 的式子表示)。
的式子表示)。
(4)为减少 的排放,工业上常将
的排放,工业上常将 转化为
转化为 固定,但存在CO又会同时发生以下两个反应:
固定,但存在CO又会同时发生以下两个反应:
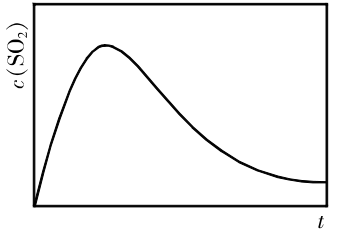
①恒容、恒温 条件下,反应体系中
条件下,反应体系中 随时间t变化的总趋势如图。
随时间t变化的总趋势如图。结合已知信 息分析 浓度随时间t变化的原因
浓度随时间t变化的原因______ 。
②恒容、恒温( ,
, )条件下,请在图中画出
)条件下,请在图中画出 条件下
条件下 浓度随时间t变化图
浓度随时间t变化图______ 。
(1)写出黄铁矿
(2)硫酸的生产中,下列说法
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400~500℃,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆流的形式,
(3)分别将1 mol的

请回答:
①据图判断
②判断X、Y、Z中属于平衡点的是
(4)为减少
| 反应 | 活化能 | 平衡常数 | |
| Ⅰ | |||
| Ⅱ |
①恒容、恒温

②恒容、恒温(
硫酸在国民经济中占有极其重要的地位,工业上常用黄铁矿为原料接触法制硫酸。
(1)写出黄铁矿(FeS2)在沸腾炉中与氧气发生反应的化学方程式_______ 。
(2)硫酸的生产中,下列说法不正确的是_______ 。
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400-500°C,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆的形式,SO3从下而上,水从上而喷下
(3)分别将1mol的SO2(g)、1.45mol的O2(g)通入p1、p2和p3恒压容器中发生反应: ,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
,相同时间内测得SO2的转化率α随温度的变化如图所示。(对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp如p(B)=px(B),p为平衡总压强,x(B为平衡系统中B的物质的量分数)。
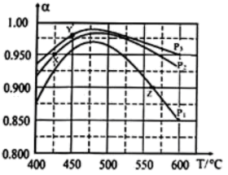
请回答:
①据图判断p1、p2、p3的大小关系_______ 。
②判断X、Y、Z中属于平衡点的是_______ (填“X”、 “Y”、 “Z”),并计算该温度下平衡的Kp=_______ 。(用含p1或p2或p3的式子表示)。
(4)为减少SO2的排放,工业上常将SO2转化为CaSO4固定,但存在CO又会同时发生以下两个反应:
①恒容、恒温(T1)条件下,反应体系中c(SO2)随时间t变化的总趋势如图。结合已知信息分析c(SO2)浓度随时间t变化的原因_______ 。
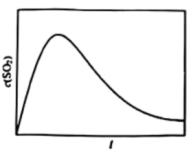
②恒容、恒温(T2,T2>T1)条件下,请在图中画出T2条件下c(SO2)浓度随时间t变化图_______ 。
(1)写出黄铁矿(FeS2)在沸腾炉中与氧气发生反应的化学方程式
(2)硫酸的生产中,下列说法不正确的是
A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高原料的利用率
B.气体在进接触室前要先净化,可防止催化剂中毒
C.接触室中反应采用400-500°C,主要是因为提高原料的平衡转化率
D.吸收塔中操作采取逆的形式,SO3从下而上,水从上而喷下
(3)分别将1mol的SO2(g)、1.45mol的O2(g)通入p1、p2和p3恒压容器中发生反应:

请回答:
①据图判断p1、p2、p3的大小关系
②判断X、Y、Z中属于平衡点的是
(4)为减少SO2的排放,工业上常将SO2转化为CaSO4固定,但存在CO又会同时发生以下两个反应:
| 反应 | 活化能 | 平衡常数 | |
| I | EaI | KI | |
| II | EaII(EaII>EaI) | KII(KI>KII) |

②恒容、恒温(T2,T2>T1)条件下,请在图中画出T2条件下c(SO2)浓度随时间t变化图
硫酸在国民经济中占有极其重要的地位,工业上常以黄铁矿为原料用接触法制硫酸。
(1)接触室中发生的反应:
 。
。
①若测得2h后 的浓度为0.6
的浓度为0.6 ,此时间内
,此时间内 的消耗速率为0.2
的消耗速率为0.2 ,则开始时
,则开始时 的浓度为
的浓度为_________  。
。
②将0.050mol (g)和0.030mol
(g)和0.030mol  (g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测
(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测 。计算该条件下反应的平衡常数K=
。计算该条件下反应的平衡常数K=_________ , 的平衡转化率为
的平衡转化率为_________ 。
③ 可作为该反应的催化剂,其过程如图。c步的化学方程式可表示为
可作为该反应的催化剂,其过程如图。c步的化学方程式可表示为_________ 。
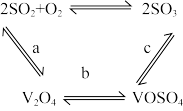
(2)硫酸的生产中,下列说法不正确的是_________(填字母)。
(3)为减少 的排放,工业上将
的排放,工业上将 转化为
转化为 固定,但存在C0会同时发生以下两个反应:
固定,但存在C0会同时发生以下两个反应:
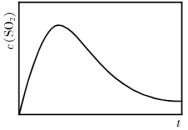
恒容、恒温( )条件下,反应体系中
)条件下,反应体系中 随时间t变化的总趋势如图。结合已知信息分析
随时间t变化的总趋势如图。结合已知信息分析 随时间t变化的原因:
随时间t变化的原因:_________ 。
(1)接触室中发生的反应:
①若测得2h后
②将0.050mol
③
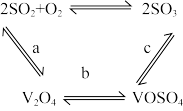
(2)硫酸的生产中,下列说法不正确的是_________(填字母)。
| A.把黄铁矿磨成细粉末在“沸腾”状态下燃烧,可以提高反应速率和原料的利用率 |
| B.气体在进接触室前要先净化,可防止催化剂中毒 |
| C.接触室中反应温度采用400~500℃,主要是为了提高原料的平衡转化率 |
| D.吸收塔中操作采取逆流的形式, |
| 反应 | 活化能 | 平衡常数 | |
| Ⅰ | |||
| Ⅱ |
恒容、恒温(

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


