解答题-实验探究题 较难0.4 引用3 组卷144
二氯六氨合铜 是一种重要的化工产品。某小组拟制备
是一种重要的化工产品。某小组拟制备 并测定其纯度。制备原理是强冷条件下:
并测定其纯度。制备原理是强冷条件下: 。
。
(一)制备产品,实验装置如图所示。
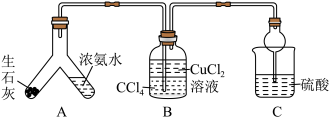
(1)装置B中添加四氯化碳的目的是_______ 。
(2)启动装置A中反应的操作是_______ ;用平衡移动原理解释制备氨气的原理:_______ 。
(3)实验完毕后,向装置B中加入适量乙醇,析出蓝色晶体,经过_______ 、洗涤、晾干得到产品。
(二)测定产品纯度,实验装置如图所示。
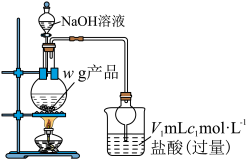
向烧瓶中加入足量 溶液,产生蓝色沉淀,逸出的氨气被过量的盐酸吸收;完全反应后,取下烧杯并用蒸馏水冲洗干燥管,将洗涤液和烧杯中的溶液合并。稀释溶液至
溶液,产生蓝色沉淀,逸出的氨气被过量的盐酸吸收;完全反应后,取下烧杯并用蒸馏水冲洗干燥管,将洗涤液和烧杯中的溶液合并。稀释溶液至 ,准确量取该溶液
,准确量取该溶液 于锥形瓶中,滴几滴指示剂
于锥形瓶中,滴几滴指示剂 ,用
,用 标准溶液滴定至终点,消耗滴定液
标准溶液滴定至终点,消耗滴定液 (假设杂质不参与反应)。
(假设杂质不参与反应)。
(4)指示剂X应选择_______ 。
(5)该产品的纯度为_______ (用含 的代数式表示)。如果碱式滴定管没有润洗,测得的结果
的代数式表示)。如果碱式滴定管没有润洗,测得的结果_______ (填“偏高”“偏低”或“无影响”)。
(一)制备产品,实验装置如图所示。

(1)装置B中添加四氯化碳的目的是
(2)启动装置A中反应的操作是
(3)实验完毕后,向装置B中加入适量乙醇,析出蓝色晶体,经过
(二)测定产品纯度,实验装置如图所示。

向烧瓶中加入足量
(4)指示剂X应选择
(5)该产品的纯度为
23-24高二上·河南南阳·期末
类题推荐
碘化亚铜(CuI)是重要的有机催化剂。某学习小组用如图装置制备CuI,并设计实验探究其性质。已知:碘化亚铜(CuI)是白色固体,难溶于水,易与KI形成 ,实验装置如图所示。
,实验装置如图所示。
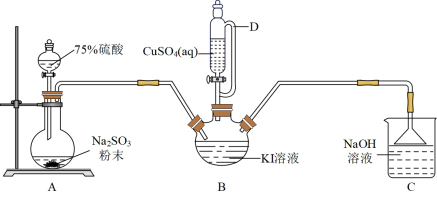
(1)仪器D的名称是___________ 。
(2)实验完毕后,用如图所示装置分离CuI的突出优点是___________ 。
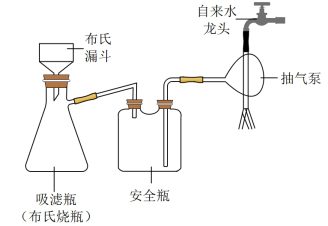
(3)装置B中发生反应的离子方程式是___________ 。
(4)小组同学设计下表方案对CuI的性质进行探究:
①在实验I中“加水,又生成白色沉淀”的原理是___________ 。
②根据实验Ⅱ,CuI与NaOH溶液反应的化学方程式是___________ 。
(5)测定CuI样品纯度:取agCuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液体积为VmL[已知:滴定反应为
溶液体积为VmL[已知:滴定反应为 ]。该样品纯度为
]。该样品纯度为___________ (用含a、b、V的代数式表示)。如果其他操作均正确,仅滴定前盛标准液的滴定管用蒸馏水洗净后没有用标准液润洗,测得结果___________ (填“偏高”“偏低”或“无影响”)。

(1)仪器D的名称是
(2)实验完毕后,用如图所示装置分离CuI的突出优点是

(3)装置B中发生反应的离子方程式是
(4)小组同学设计下表方案对CuI的性质进行探究:
| 实验 | 实验操作及现象 |
| I | 取少量CuI放入试管中,加入KI溶液,白色固体溶解得到无色溶液;加水,又生成白色沉淀 |
| Ⅱ | 取少量CuI放入试管中,加入NaOH溶液,振荡,产生砖红色沉淀。过滤,向所得上层清液中滴加淀粉溶液,无明显变化;将砖红色沉淀溶于稀硫酸,产生红色固体和蓝色溶液 |
②根据实验Ⅱ,CuI与NaOH溶液反应的化学方程式是
(5)测定CuI样品纯度:取agCuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用
某学习小组利用二氧化氯 制备消毒剂、漂白剂亚氯酸钠
制备消毒剂、漂白剂亚氯酸钠 ,有关反应原理:
,有关反应原理: 放热反应
放热反应
实验一、制备 晶体
晶体
选择如图所示装置设计实验制备亚氯酸钠晶体
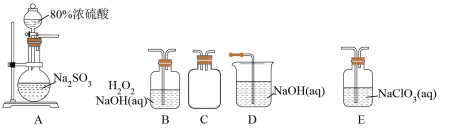
已知:饱和 溶液析出晶体与度关系如下表所示:
溶液析出晶体与度关系如下表所示:
⑴装置连接顺序:
______
⑵C装置的作用是______ D装置作用是______
⑶A装置中选择 浓硫酸的理由是
浓硫酸的理由是______
⑷写出E装置中发生反应的离子方程式______
⑸对B装置中溶液采用结晶法提取无水亚氯酸钠晶体,操作分别为蒸发结晶、趁热过滤、用 左右热水洗涤、低于
左右热水洗涤、低于 条件下干燥,得到成品,蒸发结晶时控制温度为
条件下干燥,得到成品,蒸发结晶时控制温度为______
实验二、测定产品纯度
⑹准确称量ag产品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应: ,将所得混合溶液稀释成250mL待测液。取
,将所得混合溶液稀释成250mL待测液。取 待测液于锥形瓶,加入淀粉溶液作指示剂,用
待测液于锥形瓶,加入淀粉溶液作指示剂,用 标准
标准 溶液滴定至终点,测得消耗
溶液滴定至终点,测得消耗 标准溶液的体积为
标准溶液的体积为 (已知:
(已知: )
)
 该产品纯度为
该产品纯度为______ (只要求列出计算式)
 若滴定前滴定管尖嘴有气泡,滴定终点时尖嘴气泡消失,则测得结果
若滴定前滴定管尖嘴有气泡,滴定终点时尖嘴气泡消失,则测得结果______ (填“偏高偏低”或“无影响”)
实验一、制备
选择如图所示装置设计实验制备亚氯酸钠晶体

已知:饱和
| 温度 | |||
| 晶体成分 |
⑴装置连接顺序:
⑵C装置的作用是
⑶A装置中选择
⑷写出E装置中发生反应的离子方程式
⑸对B装置中溶液采用结晶法提取无水亚氯酸钠晶体,操作分别为蒸发结晶、趁热过滤、用
实验二、测定产品纯度
⑹准确称量ag产品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生反应:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网




