解答题-原理综合题 适中0.65 引用1 组卷37
CO和NO都是有毒气体,但新的研究表明,它们都是生命体系气体信号分子,在人体内具有重要的生理作用,H2是高中阶段常见的气体。回答下列问题:
(1)反应2NO(g)+2H2(g)⇌N2(g)+2H2O(g) △H=-664kJ/mol是联合硝酸工业减少污染物排放的重要反应。该反应分为三步完成(都是双分子反应,即反应物都只有两种分子),前两步反应如下:
第1步:2NO(g)⇌N2O2(g)△H=-103kJ/mol
第2步:N2O2(g)+H2(g)⇌N2O(g)+H2O(g)△H=-17kJ/mol
①写出第3步反应的热化学方程式:_______ 。
②基元反应mA(g)+nB(g)⇌pC(g)+qD(g),正反应速率υ正=κcm(A)•cn(B)。
2NO(g)+2H2(g)⇌N2(g)+2H2O(g)的正反应速率υ正=k1c2(NO),总反应速率 ,α是平衡转化率,α′是瞬时转化率,k、k1、k2均为速率常数,受温度影响,温度升高,速率常数增大。
,α是平衡转化率,α′是瞬时转化率,k、k1、k2均为速率常数,受温度影响,温度升高,速率常数增大。
Ⅰ.复杂反应分为多步进行时,决定反应速率的是最_______ (填“快”或“慢”)的一步,3步基元反应中,活化能最高的一步是第_______ 步。
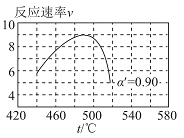
Ⅱ.温度升高,α_______ (填“变大”、“变小”或“不变”),在α′=0.90时,一系列温度下的总反应速率—时间(υ-t)曲线如图所示,分析图中曲线先升后降的原因:_______ 。
(2)用FeO冶炼Fe的过程涉及如下反应:
反应Ⅰ:FeO(s)+CO(g)⇌Fe(s)+CO2(g)
反应Ⅱ:FeO(s)+C(s)⇌Fe(s)+CO(g)
①将FeO和CO放入恒容密闭容器中,下列事实能说明反应Ⅰ和Ⅱ均已达到平衡状态的是_______ (填选项字母)。
A.容器内气体的密度不再发生变化 B. CO的生成速率等于消耗速率。
C.容器内气体总压强不再发生变化 D. 容器内CO和CO2的物质的量相等
②在一个体积可变的容器中,维持温度1200K不变(此时反应Ⅰ的分压平衡常数KP1=1.00)。压缩容器体积,达到新平衡时,CO的分压_______ (填“变大”、“变小”或“不变”)。
(1)反应2NO(g)+2H2(g)⇌N2(g)+2H2O(g) △H=-664kJ/mol是联合硝酸工业减少污染物排放的重要反应。该反应分为三步完成(都是双分子反应,即反应物都只有两种分子),前两步反应如下:
第1步:2NO(g)⇌N2O2(g)△H=-103kJ/mol
第2步:N2O2(g)+H2(g)⇌N2O(g)+H2O(g)△H=-17kJ/mol
①写出第3步反应的热化学方程式:
②基元反应mA(g)+nB(g)⇌pC(g)+qD(g),正反应速率υ正=κcm(A)•cn(B)。
2NO(g)+2H2(g)⇌N2(g)+2H2O(g)的正反应速率υ正=k1c2(NO),总反应速率
Ⅰ.复杂反应分为多步进行时,决定反应速率的是最
Ⅱ.温度升高,α

(2)用FeO冶炼Fe的过程涉及如下反应:
反应Ⅰ:FeO(s)+CO(g)⇌Fe(s)+CO2(g)
反应Ⅱ:FeO(s)+C(s)⇌Fe(s)+CO(g)
①将FeO和CO放入恒容密闭容器中,下列事实能说明反应Ⅰ和Ⅱ均已达到平衡状态的是
A.容器内气体的密度不再发生变化 B. CO的生成速率等于消耗速率。
C.容器内气体总压强不再发生变化 D. 容器内CO和CO2的物质的量相等
②在一个体积可变的容器中,维持温度1200K不变(此时反应Ⅰ的分压平衡常数KP1=1.00)。压缩容器体积,达到新平衡时,CO的分压
23-24高二上·广东江门·期中
类题推荐
氮氧化物在工农业生产中有着重要作用,但也会对大气及水体产生污染,治理和减少污染是环境学家研究的热点之一。请回答下列问题:
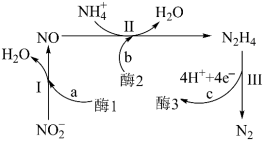
(1)NH3还原法研究发现NH3还原NO的反应历程如图。
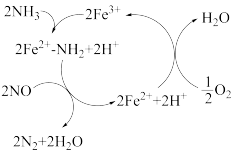
①该反应的催化剂是____ 。
②总反应化学方程式为____ 。
(2)H2还原法
反应2NO(g)+2H2(g) N2(g)+2H2O(g) △H=-664kJ•mol-1
N2(g)+2H2O(g) △H=-664kJ•mol-1
是联合硝酸工业减少污染物排放的重要反应。该反应分为三步基元反应完成:
第一步(慢反应):2NO(g) N2O2(g) △H1=-103kJ•mol-1
N2O2(g) △H1=-103kJ•mol-1
第二步(快反应):
第三步(快反应):N2O(g)+H2(g) N2(g)+H2O(g) △H2=-544kJ•mol-1
N2(g)+H2O(g) △H2=-544kJ•mol-1
①写出第二步反应的热化学方程式:_____ 。
②三步基元反应中,活化能最高的一步是第_____ 步。
(3)CO还原法
向一恒温恒容的密闭容器中充入1molNO(g)和1molCO(g)发生反应:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H<0。 时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态II,正反应速率随时间变化如图所示。下列说法正确的是
时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态II,正反应速率随时间变化如图所示。下列说法正确的是____ (填标号)
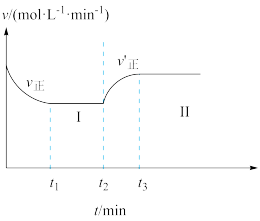
a. 容器内压强不变,说明反应体系已达到平衡
b. t2时可能改变的条件是向容器中充入N2
c. 平衡时向容器中充入惰性气体,反应I的平衡逆向移动
d. 平衡常数K:K(II)<K(I)
(4)CH4还原法
一定温度下,在2.0L刚性密闭容器中充入1molCH4和2molNO2,发生反应:CH4(g)+2NO2(g) CO2(g)+N2(g)+2H2O(g)。测得反应时间(t)与容器内气体总压强(p)的变化如表所示。
CO2(g)+N2(g)+2H2O(g)。测得反应时间(t)与容器内气体总压强(p)的变化如表所示。
①用CH4表示0~4min内的反应速率v(CH4)=____ kPa•min-1。
②达到平衡时,该温度下的压强平衡常数Kp=____ kPa(以分压表示的平衡常数为Kp,分压=总压×物质的量分数)。
(1)NH3还原法研究发现NH3还原NO的反应历程如图。
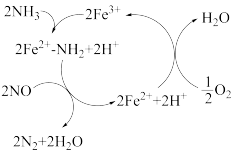
①该反应的催化剂是
②总反应化学方程式为
(2)H2还原法
反应2NO(g)+2H2(g)
是联合硝酸工业减少污染物排放的重要反应。该反应分为三步基元反应完成:
第一步(慢反应):2NO(g)
第二步(快反应):
第三步(快反应):N2O(g)+H2(g)
①写出第二步反应的热化学方程式:
②三步基元反应中,活化能最高的一步是第
(3)CO还原法
向一恒温恒容的密闭容器中充入1molNO(g)和1molCO(g)发生反应:2NO(g)+2CO(g)=N2(g)+2CO2(g) △H<0。

a. 容器内压强不变,说明反应体系已达到平衡
b. t2时可能改变的条件是向容器中充入N2
c. 平衡时向容器中充入惰性气体,反应I的平衡逆向移动
d. 平衡常数K:K(II)<K(I)
(4)CH4还原法
一定温度下,在2.0L刚性密闭容器中充入1molCH4和2molNO2,发生反应:CH4(g)+2NO2(g)
| 反应时间(t)/min | 0 | 2 | 4 | 6 | 8 | 10 |
| p/(100kPa) | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
②达到平衡时,该温度下的压强平衡常数Kp=
消除城市中汽车尾气的污染是一个很重要的课题。回答下列问题
(1) 下列不属于汽车尾气中的污染物的是___________
A. CO、CxHy B. NOx、细颗粒物 C. CO、NOx D. CO2、H2S
(2)已知:① 2NO(g) + 2CO(g) N2(g) + 2CO2(g) ∆H1=-746.5 kJ• mol-1,据此可在一定条件下反应消除NO和CO的污染;② CO2(g)+C(s)=2CO(g) △H2=+172.5 kJ•mol-1;碳(石墨)的燃烧热为-393.5kJ•mol-1.写出石墨完全燃烧的热化学方程式
N2(g) + 2CO2(g) ∆H1=-746.5 kJ• mol-1,据此可在一定条件下反应消除NO和CO的污染;② CO2(g)+C(s)=2CO(g) △H2=+172.5 kJ•mol-1;碳(石墨)的燃烧热为-393.5kJ•mol-1.写出石墨完全燃烧的热化学方程式___________ 。2NO(g)= N2(g)+O2(g) △H3=___________ kJ•mol-1
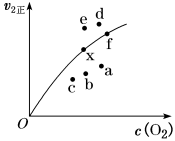
(3)某研究小组在三个容积均为VL的恒容密闭容器中,分别充入1.0molNO和1.0molCO,在三种不同实验条件(见下表)下进行上述反应,反应体系的总压强(P)随时间变化情况如图所示:

①曲线III对应的实验编号是___________ ,曲线I中压强降低的原因是___________ 。
②由曲线II数据计算出对应条件下的压强平衡常数Kp=___________ ; 若在曲线III对应条件下,NO、CO、N2、 CO2的分压依次是10kPa、20kPa、 40kPa、 40kPa,则此时反应的速率v正___________ v逆(填 “<”、=’或“>”)。
(4)反应物分子一步直接转化为产物的反应称为基元反应,一个化学反应往往是由多个基元反应分步进行的,这个分步过程称为反应机理,机理中的快反应对整个反应速率的影响可以忽略不计。一定温度下,基元反应的化学反应速率与反应物浓度以其化学计量数的幂的连乘积成正比,如基元反应mA(g)+nB(g) pC(g)的 “速率方程”可表示为v= kcm(A)•cn(B) (k为速率常数)。实验测得低温时某反应的速率方程为v=kc2(NO2),其反应机理有如下两种可能。则该反应的化学方程式可表示为
pC(g)的 “速率方程”可表示为v= kcm(A)•cn(B) (k为速率常数)。实验测得低温时某反应的速率方程为v=kc2(NO2),其反应机理有如下两种可能。则该反应的化学方程式可表示为___________ ,以 下机理中与其速率方程符合的是___________ ( 填编号)。
(1) 下列不属于汽车尾气中的污染物的是
A. CO、CxHy B. NOx、细颗粒物 C. CO、NOx D. CO2、H2S
(2)已知:① 2NO(g) + 2CO(g)
(3)某研究小组在三个容积均为VL的恒容密闭容器中,分别充入1.0molNO和1.0molCO,在三种不同实验条件(见下表)下进行上述反应,反应体系的总压强(P)随时间变化情况如图所示:

| 实验编号 | a | b | c |
| 温度/K | 500 | 500 | 600 |
| 催化剂的比表面积/m2.g-1 | 82 | 124 | 124 |
②由曲线II数据计算出对应条件下的压强平衡常数Kp=
(4)反应物分子一步直接转化为产物的反应称为基元反应,一个化学反应往往是由多个基元反应分步进行的,这个分步过程称为反应机理,机理中的快反应对整个反应速率的影响可以忽略不计。一定温度下,基元反应的化学反应速率与反应物浓度以其化学计量数的幂的连乘积成正比,如基元反应mA(g)+nB(g)
| 反应机理 | 第一步反应 | 第二步反应 |
| ① | 2NO | N2O4+2CO= 2NO+2CO2 (慢反应) |
| ② | 2NO2=NO3+NO (慢反应) | NO3+CO=NO2+CO2 (快反应) |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网