解答题-原理综合题 适中0.65 引用1 组卷52
硫及其化合物在生产生活中具有广泛的应用,根据所学知识,回答下列问题:
(1) 溶液显
溶液显_______________ 性,判断的理由是_______________ (用离子方程式表示),若将该溶液蒸干,最终所得固体为_______________ (填化学式)。
(2) 的
的 溶液中,各离子浓度由大到小的关系为
溶液中,各离子浓度由大到小的关系为_______________ 。
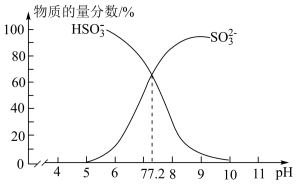
(3)常温下,在某 混合溶液中,部分含硫微粒的物质的量分数随
混合溶液中,部分含硫微粒的物质的量分数随 的变化曲线如图所示,根据图示,
的变化曲线如图所示,根据图示, 的水解平衡常数
的水解平衡常数
_______________ 。
(4)常温下,某浓度的 溶液中:
溶液中:
① 为
为_______________ (填“强”或“弱”)电解质。
②往 溶液中滴加少量的
溶液中滴加少量的 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为_______________ ,此时所得溶液的
_______________ (填“变大”、“变小”或“不变”)。
(5)在 的
的 溶液中加入等体积
溶液中加入等体积 溶液,有黑色
溶液,有黑色 沉淀生成,反应后溶液中
沉淀生成,反应后溶液中
_______________ [已知: ](忽略溶液混合时体积的变化)。
](忽略溶液混合时体积的变化)。
(1)
(2)
(3)常温下,在某

(4)常温下,某浓度的
①
②往
(5)在
23-24高二上·广东江门·期末
类题推荐
硫及其化合物在生产、生活中具有广泛的应用,根据所学知识,回答下列问题:
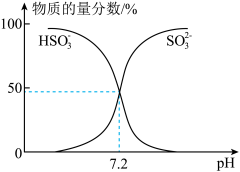
(1)室温下,在某NaHSO3、Na2SO3混合溶液中, 、
、 物质的量分数随pH的变化曲线如图所示,根据图示,
物质的量分数随pH的变化曲线如图所示,根据图示, 的水解平衡常数Kh=
的水解平衡常数Kh=_______

(2)室温下,某浓度的(NH4)2SO3溶液中:
①往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为_______ 。
②此时所得溶液的pH_______ (“变大”、“变小”或“不变”)。
(3)亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,向一定体积的亚磷酸溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
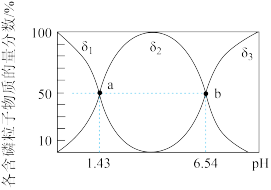
①NaH2PO3为_______ (填“正盐”或“酸式盐”),其溶液显_______ (填“酸性”、“中性”、“碱性”或“无法判断”)。
②写出NaH2PO3水解的离子方程式_______ ;
(4)现有浓度为0.02 mol/L的HCN与0.01 mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_______(填字母编号)。
(1)室温下,在某NaHSO3、Na2SO3混合溶液中,

(2)室温下,某浓度的(NH4)2SO3溶液中:
①往(NH4)2SO3溶液中滴加少量的HClO溶液,发生反应的离子方程式为
②此时所得溶液的pH
(3)亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,向一定体积的亚磷酸溶液中滴加等物质的量浓度的NaOH溶液,混合液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①NaH2PO3为
②写出NaH2PO3水解的离子方程式
(4)现有浓度为0.02 mol/L的HCN与0.01 mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是_______(填字母编号)。
| A.c(H+)>c(OH-) | B.c(H+)<c(OH-) |
| C.c(H+)+c(HCN)=c(OH-) | D.c(HCN)+c(CN-)=0.01 mol/L |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网