解答题-原理综合题 适中0.65 引用1 组卷99
甲醇是一种理想的储氢载体,我国科学家研发的全球首套千吨级太阳能燃料舍成项目被形象地称为“液态阳光”计划。该计划利用太阳能电解水产生氢气,然后将二氧化碳与氢气转化为甲醇,以实现碳中和的目的。生产甲醇过程主要发生以下反应:
①
②
③
(1)反应③活化能 (正)
(正)___________  (逆)(填“>”、“<”或“=”),该反应在
(逆)(填“>”、“<”或“=”),该反应在___________ (填“高温”或“低温”)条件下自发进行。
(2)当只发生以上反应时,单位时间内反应物投料与 转化率、
转化率、 产率之间关系如下表:
产率之间关系如下表:
根据资料,氢气12000元/吨,二氧化碳1200元/吨,甲醇的选择率=甲醇的产率/二氧化碳转化率。若单纯从选择率角度看,上表中氢气与二氧化碳的最佳投料比应为___________ (填字母);若从碳中和的目的及原料成本因素考虑,实际生产中氢气与二氧化碳的最佳投料比应接近___________ (填字母)。
A.2∶1 B.3∶1 C.5∶1 D.7∶1
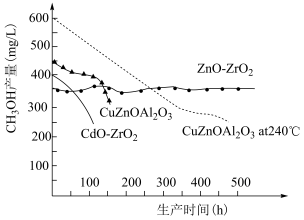
(3)工业生产对催化剂进行选择的时候,除了要考虑催化剂的效率以外,催化剂的稳定性也是很重要的参考条件,一般工业生产所用催化剂更换间隔为半年到一年,请根据下图信息,选出最适合的催化剂___________。
(4)在恒温密闭容器中,往容器中注入一定量 和
和 发生以上反应,若反应达到平衡时
发生以上反应,若反应达到平衡时 和
和 浓度相等,则平衡时的
浓度相等,则平衡时的 的浓度=
的浓度=___________  。
。
(5)通过设计燃料电池(图1),可以将甲醇中蕴藏的能量释放出来,酸性电解质溶液中,甲醇在电极上反应,产生碳氧化物 。
。
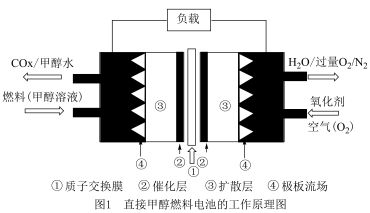
请写出燃料电池负极反应方程式___________ 。
①
②
③
(1)反应③活化能
(2)当只发生以上反应时,单位时间内反应物投料与
| 11.6 | 13.7 | 15.9 | 18.7 | |
| 3.0 | 4.1 | 5.3 | 6.9 |
A.2∶1 B.3∶1 C.5∶1 D.7∶1
(3)工业生产对催化剂进行选择的时候,除了要考虑催化剂的效率以外,催化剂的稳定性也是很重要的参考条件,一般工业生产所用催化剂更换间隔为半年到一年,请根据下图信息,选出最适合的催化剂___________。
| A. | B. | C. | D. |

(4)在恒温密闭容器中,往容器中注入一定量
(5)通过设计燃料电池(图1),可以将甲醇中蕴藏的能量释放出来,酸性电解质溶液中,甲醇在电极上反应,产生碳氧化物

请写出燃料电池负极反应方程式
23-24高三上·福建福州·阶段练习
类题推荐
中国科学家在国际知名杂质《焦耳》上发表文章,首次在国际上提出“液态阳光”一词,并被国际社会广泛认可。把太阳能装进瓶子里,随处携带,随时取用,是人类一直以来的美好梦想。近年来,人类终于找到了太阳能的最佳载体——甲醇。“液态阳光”,即“清洁甲醇”和“绿色甲醇”,是指生产过程中碳排放极低或为零时制得的甲醇。人们利用太阳能电解水产生氢气,然后将二氧化碳与氢气转化为甲醇,以实现碳中和的目的。生产甲醇过程主要发生以下反应(温度恒为 ):
):
①


②


③

回答下列问题:
(1)反应③活化能E(正)_____ E(逆)(填“>”、“<”或“=”),该反应在_____ (填“高温”或“低温”)条件下自发进行。
(2)当只发生以上反应时,单位时间内反应物投料与 转化率、
转化率、 产率之间关系如下表:
产率之间关系如下表:
根据资料,氢气12000元/吨,二氧化碳1200元/吨,甲醇的选择率=甲醇的产率/二氧化碳转化率。若单纯从选择率角度看,上表中氢气与二氧化碳的最佳投料比应为_____ (填字母标号);若从生产甲醇所需成本角度考虑,实际生产中氢气与二氧化碳的最佳投料比应接近_____ (填字母标号)。
A. B.
B. C.
C. D.
D.
(3)工业生产对催化剂进行选择的时候,除了要考虑催化剂的效宰以外,催化剂的稳定性也是很重要的参考条件,一般工业生产所用催化剂更换间隔为半年到一年,请根据下图信息,选出最适合的催化剂_____。
(4)在恒温( )密闭容器中,往容器中注入一定量
)密闭容器中,往容器中注入一定量 和
和 发生以上反应,
发生以上反应,
_____ ;若反应达到平衡时 和
和 浓度相等,则平衡时
浓度相等,则平衡时 的浓度
的浓度
_____  。
。
(5)甲醇除了可以用作燃料外,还可以用于燃料电池中。燃料电池是一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源。
①标况下,液态甲醇的燃烧热为 。请写出表示甲醇燃烧热的热化学方程式:
。请写出表示甲醇燃烧热的热化学方程式:_____ 。
②在甲醇燃料电池中,将甲醇和空气分别通入两个电极,电解质溶液为 溶液,则负极的电极反应式为:
溶液,则负极的电极反应式为:_____ 。
①
②
③
回答下列问题:
(1)反应③活化能E(正)
(2)当只发生以上反应时,单位时间内反应物投料与
| 11.6 | 13.7 | 15.9 | 18.7 | |
| 3.0 | 4.1 | 5.3 | 6.9 |
A.
(3)工业生产对催化剂进行选择的时候,除了要考虑催化剂的效宰以外,催化剂的稳定性也是很重要的参考条件,一般工业生产所用催化剂更换间隔为半年到一年,请根据下图信息,选出最适合的催化剂_____。

| A. | B. | C. | D. |
(5)甲醇除了可以用作燃料外,还可以用于燃料电池中。燃料电池是一种连续地将燃料和氧化剂的化学能直接转化为电能的化学电源。
①标况下,液态甲醇的燃烧热为
②在甲醇燃料电池中,将甲醇和空气分别通入两个电极,电解质溶液为
Ⅰ.甲醇是一种理想的储氢载体,我国科学家研发的全球首套太阳能燃料合成项目被称为“液态阳光”计划,可利用太阳能电解水产生H2,再将CO2与H2转化为甲醇,以实现碳中和。
(1)下列关于甲醇(CH3OH)的说法中,正确的是___________
Ⅱ.已知,CO2生产甲醇过程主要发生以下反应:
反应Ⅰ.CO2(g) + 3H2(g) CH3OH(g) + H2O(g) ∆H1= −48.97kJ·mol−1
CH3OH(g) + H2O(g) ∆H1= −48.97kJ·mol−1
反应Ⅱ.CO2(g) + H2(g) CO(g) + H2O(g) ∆H2= +41.17 kJ·mol−1
CO(g) + H2O(g) ∆H2= +41.17 kJ·mol−1
反应Ⅲ.CO(g) + 2H2(g) CH3OH(g) ∆H3
CH3OH(g) ∆H3
(2)反应Ⅲ中,①活化能E(正)___________ E (逆) (填“>”、“<”或“=”);
②该反应在___________ 条件下能自发进行;
A.在高温条件下自发进行 B.在低温条件下自发进行
C.在任何条件下都能自发进行 D.在任何条件下都不能自发进行
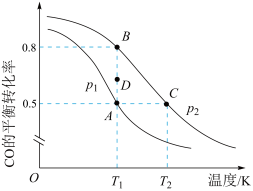
(3)反应III中,CO的平衡转化率与温度的关系如图所示:___________ 。T1时,由D点到B点过程中,正、逆反应速率之间的关系:v正 ___________ v逆。(填“>”、“<”或“=”)
②向某恒温恒压密闭 容器中充入1mol CO(g)和2mol H2(g),下列能说明反应III达到平衡的是___________ ;
A.容器内混合气体的密度不再改变
B.容器内混合气体的平均相对分子质量不再改变
C.两种反应物转化率的比值不再改变
D.v正(CO)=2 v逆(H2)
③在2L恒容密闭 容器中充入2mol CO和4mol H2,在p2和T1条件下经10min达到平衡状态。在该条件下,v(H2)=___________ mol·L−1·min−1。
(4)在CO2加氢合成甲醇的体系中,①下列说法不正确的是___________ ;
A.若在绝热恒容 容器,反应I的平衡常数K保持不变,说明反应I、II都已达平衡
B.若气体的平均相对分子质量不变,说明反应I、II都已达平衡
C.体系达平衡后,若压缩体积,反应I平衡正向移动,反应II平衡不移动
D.选用合适的催化剂可以提高甲醇在单位时间内的产量
②已知:CH3OH的选择性= ×100%,不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是
×100%,不考虑催化剂活性温度,为同时提高CO2的平衡转化率和甲醇的选择性,应选择的反应条件是___________ ,并说明其原因
A.高温高压 B.高温低压 C.低温低压 D.低温高压
原因:___________
(5)我国科学家设计了离子液体电还原CO2合成CH3OH工艺,写出碱性条件下CO2生成甲醇的电极反应式___________ 。
(1)下列关于甲醇(CH3OH)的说法中,正确的是___________
| A.甲醇在一定条件下可被氧化生成CO2 | B.甲醇储氢符合“相似相溶”原理 |
C.甲醇官能团的电子式: | D.甲醇分子是含有极性键的非极性分子 |
Ⅱ.已知,CO2生产甲醇过程主要发生以下反应:
反应Ⅰ.CO2(g) + 3H2(g)
反应Ⅱ.CO2(g) + H2(g)
反应Ⅲ.CO(g) + 2H2(g)
(2)反应Ⅲ中,①活化能E(正)
②该反应在
A.在高温条件下自发进行 B.在低温条件下自发进行
C.在任何条件下都能自发进行 D.在任何条件下都不能自发进行
(3)反应III中,CO的平衡转化率与温度的关系如图所示:
②向某
A.容器内混合气体的密度不再改变
B.容器内混合气体的平均相对分子质量不再改变
C.两种反应物转化率的比值不再改变
D.v正(CO)=2 v逆(H2)
③在2L
(4)在CO2加氢合成甲醇的体系中,①下列说法不正确的是
A.若在
B.若气体的平均相对分子质量不变,说明反应I、II都已达平衡
C.体系达平衡后,若压缩体积,反应I平衡正向移动,反应II平衡不移动
D.选用合适的催化剂可以提高甲醇在单位时间内的产量
②已知:CH3OH的选择性=
A.高温高压 B.高温低压 C.低温低压 D.低温高压
原因:
(5)我国科学家设计了离子液体电还原CO2合成CH3OH工艺,写出碱性条件下CO2生成甲醇的电极反应式
Ⅰ.二氧化碳和甲烷是两种主要的温室效应气体
(1)写出碳在元素周期表的位置___________ 写出 的电子式
的电子式___________ 。
(2)下列关于甲烷的描述正确的是___________。(双选)
Ⅱ.二氧化碳的封存是指将 废气富集后加压通入地下进行石油、天然气的开采。
废气富集后加压通入地下进行石油、天然气的开采。
(3)对 加压过程中系统的
加压过程中系统的
___________ 0
A.大于 B.小于 C.等于
(4)工业上用 溶液吸收废气中的
溶液吸收废气中的 ,流程如下
,流程如下
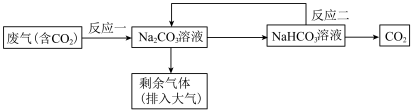
①写出反应一的离子方程式___________ 。
②根据所学知识,推测反应一的
___________ 0
A.大于 B.小于
③根据所学知识,推测反应二的
___________ 0
A.大于 B.小于
Ⅲ.富集后的 也可进行再利用,例如“加氢法减碳”制甲醇。
也可进行再利用,例如“加氢法减碳”制甲醇。
总反应可表示为①

该反应一般认为通过如下步骤来实现:
②
③

(5)上述总反应的
___________ (列式,用 和
和 表示);写出总反应的平衡常数表达式
表示);写出总反应的平衡常数表达式___________
(6)上述三个反应对应的平衡常数分别为 、
、 、
、 ,它们随温度变化的曲线如图所示。则
,它们随温度变化的曲线如图所示。则
___________ 

A.大于 B.小于 C.等于
(7)对于上述反应体系,下列说法正确 的是___________。
(8)一定条件下向2L的密闭容器中充入 和
和 发生反应③,
发生反应③, 的平衡转化率与温度、压强的关系如下图。
的平衡转化率与温度、压强的关系如下图。
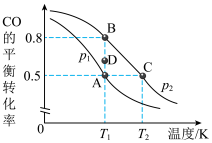
压强
___________  (“>”“<”或“=”);A、B、C三点平衡常数
(“>”“<”或“=”);A、B、C三点平衡常数 、
、 、
、 的大小关系是
的大小关系是___________ _;保持温度为 ,压强为
,压强为 的条件,反应达平衡后,再加入
的条件,反应达平衡后,再加入 和
和 ,新平衡下
,新平衡下 的转化率
的转化率___________  (“>”“<”或“=”)。
(“>”“<”或“=”)。
(9)在一定温度下,将 和
和 充入体积为
充入体积为 的恒容密闭容器中发生反应并达到平衡:
的恒容密闭容器中发生反应并达到平衡:
 ,测得平衡混合气体中
,测得平衡混合气体中 的物质的量分数为
的物质的量分数为 。下列说法
。下列说法不正确 的是
Ⅳ.化石燃料在能源结构中依然占比巨大,选择碳排放较低的化石燃料利于碳中和的实现

(10)已知甲烷的单位热值含碳量为 ,丙烷
,丙烷 的燃烧热
的燃烧热 ,计算丙烷的单位热值含碳量
,计算丙烷的单位热值含碳量___________ ,从单位热值含碳量角度分析,哪种燃料更利于碳中和?[ ]
]________ 。
(1)写出碳在元素周期表的位置
(2)下列关于甲烷的描述正确的是___________。(双选)
A. 可表示甲烷的空间填充模型 可表示甲烷的空间填充模型 |
B. 可表示甲烷的球棍模型 可表示甲烷的球棍模型 |
| C.甲烷的燃烧热为 |
| D.气态氢化物的热稳定性: |
Ⅱ.二氧化碳的封存是指将
(3)对
A.大于 B.小于 C.等于
(4)工业上用

①写出反应一的离子方程式
②根据所学知识,推测反应一的
A.大于 B.小于
③根据所学知识,推测反应二的
A.大于 B.小于
Ⅲ.富集后的
总反应可表示为①
该反应一般认为通过如下步骤来实现:
②
③
(5)上述总反应的
(6)上述三个反应对应的平衡常数分别为

A.大于 B.小于 C.等于
(7)对于上述反应体系,下列说法
| A.增大初始投料比 |
| B.当气体的平均摩尔质量保持不变时,说明反应体系已达平衡 |
| C.体系达平衡后,若压缩容器体积,则反应②平衡不移动,反应①平衡正向移动 |
| D.选用合适的催化剂可以提高反应①中 |
(8)一定条件下向2L的密闭容器中充入

压强
(9)在一定温度下,将
| A.平衡混合气体中C原子的物质的量是 |
| B.该反应的反应物的总能量高于生成物的总能量 |
| C.升高温度,平衡常数 |
| D.使用催化剂可以降低反应的活化能 |
Ⅳ.化石燃料在能源结构中依然占比巨大,选择碳排放较低的化石燃料利于碳中和的实现
(10)已知甲烷的单位热值含碳量为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


