解答题-原理综合题 适中0.65 引用1 组卷73
(1)
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
则反应
(2)电解法转化
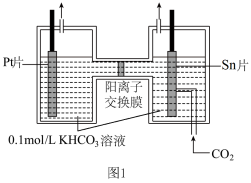
写出阴极
(3)
反应Ⅰ:
反应Ⅱ:
①反应Ⅱ的平衡常数表达式
②在恒压、
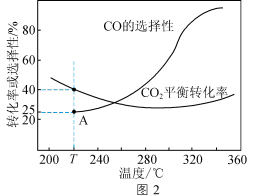
T℃时,起始投入
23-24高三上·天津武清·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网