解答题-结构与性质 适中0.65 引用1 组卷173
硼、砷、铁等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填标号)。
(2)同周期中第一电离能大于砷的元素有___________ 种。CH3As(OH)2与(CH3)2AsOH两种含砷有机酸中沸点较高的是___________ (填化学式)。
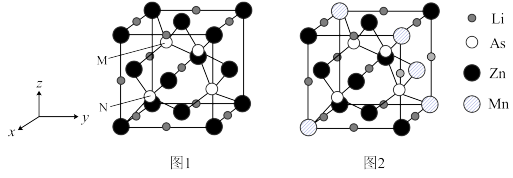
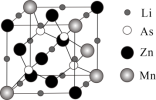
(3)LiZnAs晶体的立方晶胞结构如图1所示,N点原子坐标为(0.75,0.25,0.25);LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs,其立方晶胞结构如图2所示。
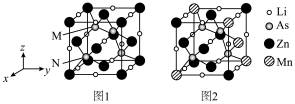
①M点原子分数坐标为___________ 。② m=___________
③设NA为阿伏加德罗常数的值,LiZnmMnnAs的摩尔质量为 M g·mol-1,晶体密度为d g·cm-3.晶胞中As原子与Mn原子之间的最短距离为___________ nm(列出计算式)。
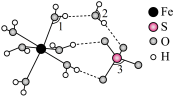
(4)FeSO4·7H2O的结构如图所示。图中键角1、2、3由大到小的顺序是___________ (填标号)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________(填标号)。
A.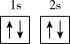 | B.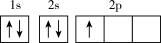 |
C.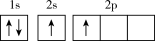 | D.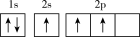 |
(2)同周期中第一电离能大于砷的元素有
(3)LiZnAs晶体的立方晶胞结构如图1所示,N点原子坐标为(0.75,0.25,0.25);LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs,其立方晶胞结构如图2所示。

①M点原子分数坐标为
③设NA为阿伏加德罗常数的值,LiZnmMnnAs的摩尔质量为 M g·mol-1,晶体密度为d g·cm-3.晶胞中As原子与Mn原子之间的最短距离为
(4)FeSO4·7H2O的结构如图所示。图中键角1、2、3由大到小的顺序是

23-24高二上·广东深圳·阶段练习
类题推荐
钛(Ti)和锆(Zr)是同一副族的相邻元素,它们的化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)钛和锆的价层电子结构相同,基态锆原子的价电子排布式为_______ ;与钛位于同一周期且基态原子单电子数与钛相同的元素,第一电离能由大到小的顺序为_______ (用元素符号填空)。
(2)Ti(BH4)2是一种储氢材料。BH 的空间构型是
的空间构型是_______ 。
(3)下列各组微粒互为等电子体的是_______(填字母标号)。
(4)ZrCl4可以与乙二胺形成配合物[ZrCl4(H2NCH2CH2NH2)]。
①1mol [ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为_______ mol。
②H2NCH2CH2NH2形成[ZrCl4(H2NCH2CH2NH2)]后,H-N-H键角将_______ (填“变大”、“变小”或“不变”),原因是_______ 。
(5)已知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,其晶胞结构如下图所示。

①TiO2晶胞中O2-的配位数是_______ 。
②TiO2晶胞中A、B的原子坐标为(0.69,0.69,1),(0.19,0.81,0.5),则C原子坐标为_______ 。
③已知二氧化锆晶胞的密度为ρ g·cm-3,则晶体中Zr原子和O原子之间的最短距离_______ pm(列出表达式,NA为阿伏加德罗常数的值,ZrO2的摩尔质量为M g/mol)。
(1)钛和锆的价层电子结构相同,基态锆原子的价电子排布式为
(2)Ti(BH4)2是一种储氢材料。BH
(3)下列各组微粒互为等电子体的是_______(填字母标号)。
| A.H2O与SO2 | B.CO2与N2O | C.CH2O与BF3 | D.C6H6与B3N3H6 |
①1mol [ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为
②H2NCH2CH2NH2形成[ZrCl4(H2NCH2CH2NH2)]后,H-N-H键角将
(5)已知TiO2晶胞中Ti4+位于O2-所构成的正八面体的体心,ZrO2晶胞中Zr4+位于O2-所构成的立方体的体心,其晶胞结构如下图所示。

①TiO2晶胞中O2-的配位数是
②TiO2晶胞中A、B的原子坐标为(0.69,0.69,1),(0.19,0.81,0.5),则C原子坐标为
③已知二氧化锆晶胞的密度为ρ g·cm-3,则晶体中Zr原子和O原子之间的最短距离
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网