解答题-工业流程题 适中0.65 引用1 组卷184
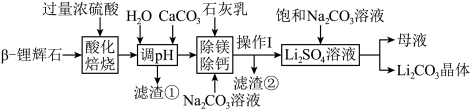
锂被誉为“新能源金属”、“金属味精”和“推动世界前进的金属”,具有极高的战略价值。碳酸锂是生产金属锂制品的基础材料,以β-锂辉石为原料,用硫酸焙烧法制取碳酸锂的工艺流程(部分试剂和步骤等已略去)如下。
【资料】
①β-锂辉石的主要成分是 ,含少量Ca、Mg元素。
,含少量Ca、Mg元素。
② (浓)
(浓) 。
。
(1)工业上将β-锂辉石磨至粒径为0.125mm左右,再送入酸化炉的原因是___________ 。
(2)浓硫酸用量不宜过量太多,原因可能是___________ 。
(3)写出“酸化焙烧”步骤中氧化锂发生反应的化学方程式___________ 。
(4)操作Ⅰ的名称为___________ ,滤渣②的成分是___________ 。
(5)在“除镁除钙”步骤中,先加入石灰乳,再加入 溶液。添加试剂的顺序不能调换,其原因是
溶液。添加试剂的顺序不能调换,其原因是___________ 。
(6)母液中的溶质是___________ 。
(7) 和
和 的溶解度如表所示:
的溶解度如表所示:
为了提高产品的纯度,需要将得到的晶体洗涤,需选用___________ ℃的水;证明 晶体洗涤干净的方法操作是
晶体洗涤干净的方法操作是___________ 。

【资料】
①β-锂辉石的主要成分是
②
(1)工业上将β-锂辉石磨至粒径为0.125mm左右,再送入酸化炉的原因是
(2)浓硫酸用量不宜过量太多,原因可能是
(3)写出“酸化焙烧”步骤中氧化锂发生反应的化学方程式
(4)操作Ⅰ的名称为
(5)在“除镁除钙”步骤中,先加入石灰乳,再加入
(6)母液中的溶质是
(7)
| T/℃ | 20 | 40 | 60 | 80 |
| S( | 1.33 | 1.17 | 1.01 | 0.85 |
| S( | 34.2 | 32.8 | 31.9 | 30.7 |
23-24高三上·四川绵阳·阶段练习
类题推荐
工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:

已知:①Li2O·Al2O3·4SiO2+H2SO4(浓) =Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是____________________________________________________________________ 。
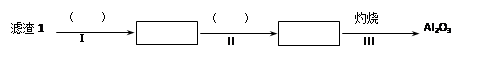
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)__________________________________________________ 。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是________________________________________________________ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是_____________________________ 。
②b中,生成Li2CO3反应的化学方程式是__________________________________ 。

已知:①Li2O·Al2O3·4SiO2+H2SO4(浓) =Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是
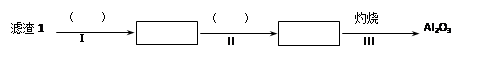
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3。
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是
②b中,生成Li2CO3反应的化学方程式是
工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
已知:① Li2O·Al2O3·4SiO2 H2SO4(浓)
H2SO4(浓)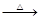 Li2SO4
Li2SO4 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓
② 某些物质的溶解度(S)如下表所示:
③ 从滤渣1中分离出Al2O3的部分流程如下图所示:
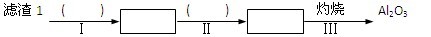
(1)请依次写出在括号内加入试剂的化学式________ 、________ 。
(2)请依次写出方框中所得到物质的化学式________ 、________ 。
(3)步骤Ⅰ中反应的离子方程式是_________________ 。
(4)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)______________________________ 。
(5)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是__________ 。
(6)氧化铝在工业上用作高温耐火材料,制耐火砖、坩埚、瓷器、人造宝石等,同时氧化铝也是炼铝的原料。写出用氧化铝炼铝的化学方程式:_________________ 。

已知:① Li2O·Al2O3·4SiO2
 H2SO4(浓)
H2SO4(浓)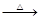 Li2SO4
Li2SO4 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓② 某些物质的溶解度(S)如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
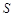 (Li2CO3)/g (Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
 (Li2SO4)/g (Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
③ 从滤渣1中分离出Al2O3的部分流程如下图所示:
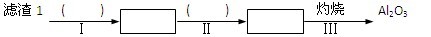
(1)请依次写出在括号内加入试剂的化学式
(2)请依次写出方框中所得到物质的化学式
(3)步骤Ⅰ中反应的离子方程式是
(4)已知滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)
(5)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
(6)氧化铝在工业上用作高温耐火材料,制耐火砖、坩埚、瓷器、人造宝石等,同时氧化铝也是炼铝的原料。写出用氧化铝炼铝的化学方程式:
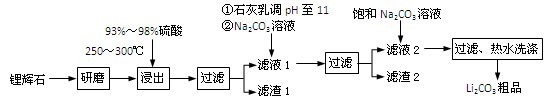
工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如图:

已知:①Li2O·Al2O3·4SiO2 + H2SO4(浓) Li2SO4 +Al2O3·4SiO2·H2O↓
Li2SO4 +Al2O3·4SiO2·H2O↓
(1)从滤渣1中分离出Al2O3的部分流程如图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中反应的离子方程式是_______ 。
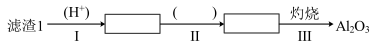
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3,写出生成滤渣2反应的离子方程式:_______ 。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是_______ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
①将粗产品Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解。阳极的电极反应式是_______ 。
②电解后向产品LiOH溶液中加入过量NH4HCO3溶液生成Li2CO3反应的化学方程式是_______ 。

已知:①Li2O·Al2O3·4SiO2 + H2SO4(浓)
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
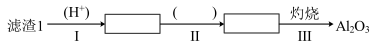
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3,写出生成滤渣2反应的离子方程式:
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
①将粗产品Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解。阳极的电极反应式是
②电解后向产品LiOH溶液中加入过量NH4HCO3溶液生成Li2CO3反应的化学方程式是
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


