解答题-原理综合题 适中0.65 引用1 组卷62
环戊二烯( )是一种重要的有机化工原料。
)是一种重要的有机化工原料。
Ⅰ.环戊二烯容易反应生成双环戊二烯( ):
): ,不同温度下,溶液中环戊二烯(
,不同温度下,溶液中环戊二烯( )浓度(初始浓度为
)浓度(初始浓度为 )与反应时间的关系如图所示:
)与反应时间的关系如图所示:
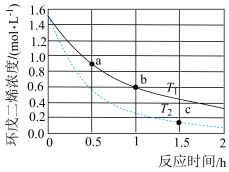
(1)反应开始至b点时,用双环戊二烯( )表示的平均速率为
)表示的平均速率为______ 。
(2)
______  ,b点的逆反应速率
,b点的逆反应速率______ a点的正反应速率(两空均选填“>”、“<”或“=”)。
(3)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是______ 。
a.
b.容器内气体压强不再变化
c.容器内混合气体的密度不再变化
d.容器内混合气体的平均相对分子质量不再变化
Ⅱ.可用伓戊烯( )制备环戊二烯(
)制备环戊二烯( ),有如下反应:
),有如下反应:
反应i:

反应ii:

反应iii:

(4)反应i的焓变
______ ,反应iii的平衡常数 为
为______ (用 、
、 表示)。
表示)。
(5)某温度时在恒容密闭容器中充入等物质的量的碘和环戊烯发生反应iii,起始总压为 ,平衡时总压为
,平衡时总压为 。
。
①平衡时HI的体积分数为______ %。
②用平衡分压代替平衡浓度计算压强平衡常数
______ (要求用最简整数比,含 的代数式表示)。
的代数式表示)。
③达到平衡后,既增加环戊烯( )的平衡转化率同时加快反应速率的措施有
)的平衡转化率同时加快反应速率的措施有______ (仅写一条)
Ⅰ.环戊二烯容易反应生成双环戊二烯(

(1)反应开始至b点时,用双环戊二烯(
(2)
(3)一定量的环戊二烯气体在恒温恒压的密闭容器中发生上述反应,可说明一定达化学平衡状态的是
a.
b.容器内气体压强不再变化
c.容器内混合气体的密度不再变化
d.容器内混合气体的平均相对分子质量不再变化
Ⅱ.可用伓戊烯(
反应i:
反应ii:
反应iii:
(4)反应i的焓变
(5)某温度时在恒容密闭容器中充入等物质的量的碘和环戊烯发生反应iii,起始总压为
①平衡时HI的体积分数为
②用平衡分压代替平衡浓度计算压强平衡常数
③达到平衡后,既增加环戊烯(
23-24高三上·四川绵阳·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
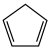 (g)+H2(g)
(g)+H2(g)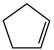 (g)
(g)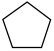 (g)
(g) (g)
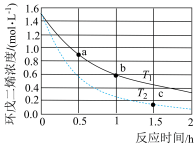
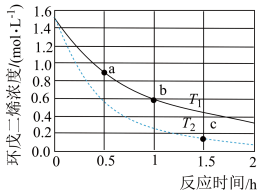
(g) (g)。不同温度下,溶液中环戊二烯的浓度(初始浓度为1.5mol·L-1)与反应时间的关系如图所示。
(g)。不同温度下,溶液中环戊二烯的浓度(初始浓度为1.5mol·L-1)与反应时间的关系如图所示。