解答题-原理综合题 较难0.4 引用2 组卷45
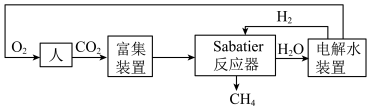
2022年中国航天在诸多领域实现重大突破。空间站一种处理 的重要方法是对
的重要方法是对 进行收集和再生处理,重新生成可供人体呼吸的氧气。部分技术路线可分为:
进行收集和再生处理,重新生成可供人体呼吸的氧气。部分技术路线可分为:_______ 。
(2)Sabatier反应
已知:H2(g)、CH4(g)的燃烧热分别为285.8kJ•mol-1、890.3kJ•mol-1,H2O(l)=H2O(g) ΔH = +44kJ•mol-1。
①则反应Ⅰ:CO2(g) +4H2(g) CH4(g) +2H2O(g) 的ΔH =
CH4(g) +2H2O(g) 的ΔH =_____ kJ•mol-1。
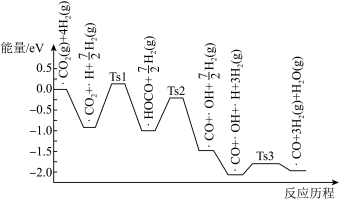
②科学家研究Sabatier反应,部分历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法中错误的是_______ 。
B.该转化反应的速率取决于Ts1的能垒
C.·HOCO转化为·CO和·OH的反应ΔH<0
D.催化剂能降低反应的活化能,提高反应物的平衡转化率
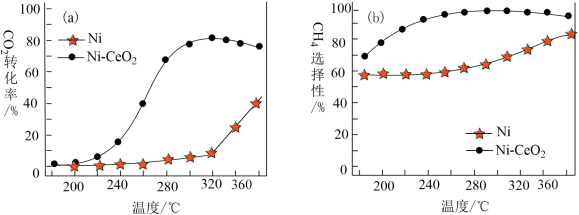
③空间站的反应器内,通常采用反应器前段加热,后段冷却的方法以提高CO2的转化效率,原因是_______ 。
④在CO2催化加氢制甲烷过程中存在竞争性的反应Ⅱ:CO2(g)+ H2(g) CO(g)+ H2O(g),一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)=
CO(g)+ H2O(g),一定温度下,向10L恒容密闭容器中充入1mol CO2和1mol H2,发生反应Ⅰ和反应Ⅱ,5min末达到平衡时测得CO2的转化率为50%,CH4与CO的分压之比为1∶4,H2O(g)的分压为p0.则0~5min内,平均反应速率v(H2)= ______ mol•L-1•min-1;反应Ⅱ的平衡常数Kp=______ (Kp是用分压表示的平衡常数,用各组分的分压代替浓度)。
(2)Sabatier反应
已知:H2(g)、CH4(g)的燃烧热分别为285.8kJ•mol-1、890.3kJ•mol-1,H2O(l)=H2O(g) ΔH = +44kJ•mol-1。
①则反应Ⅰ:CO2(g) +4H2(g)
②科学家研究Sabatier反应,部分历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法中错误的是

B.该转化反应的速率取决于Ts1的能垒
C.·HOCO转化为·CO和·OH的反应ΔH<0
D.催化剂能降低反应的活化能,提高反应物的平衡转化率
③空间站的反应器内,通常采用反应器前段加热,后段冷却的方法以提高CO2的转化效率,原因是
④在CO2催化加氢制甲烷过程中存在竞争性的反应Ⅱ:CO2(g)+ H2(g)
22-23高二上·山西晋中·期末
类题推荐
2022年4月16日,中国空间站的3名航天员乘神舟十三号载人飞船平安返回地球。空间站处理CO2的一种重要方法是对CO2进行收集和再生处理,重新生成可供人体呼吸的氧
气。其技术路线可分为以下三步:
I.固态胺吸收与浓缩CO2
(1)在水蒸气存在下固态胺吸收CO2反应生成酸式碳酸盐(该反应是放热反应) ,再解吸出CO2的简单方法是_______ 。
II.CO2的加氢甲烷化
H2还原CO2制CH4的部分反应如下:
i. CO2(g) + H2(g) CO(g) + H2O(g) △H1= +41 kJ·mol-1
CO(g) + H2O(g) △H1= +41 kJ·mol-1
ii. CO(g) +3H2(g) CH4(g) +H2O(g) △H2= -246 kJ·mol-1
CH4(g) +H2O(g) △H2= -246 kJ·mol-1
(2)反应CO2(g) +4H2(g) CH4(g) +2H2O(g)的△H=
CH4(g) +2H2O(g)的△H=_______ kJ·mol-1。
(3)有利于提高甲烷平衡产率的反应条件是_______ (写一种)。
(4)科学家研究在催化剂表面上CO2与H2的反应,前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法中一定正确的是_______(填字母)。
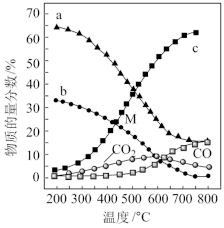
(5)控制起始时 =4,p=1 atm,恒容条件下,若只发生反应i、ii ,平衡时各物质的物质的量分数随温度的变化如图所示:
=4,p=1 atm,恒容条件下,若只发生反应i、ii ,平衡时各物质的物质的量分数随温度的变化如图所示:
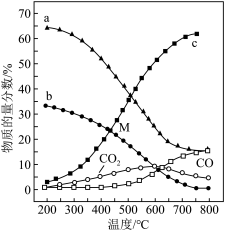
①图中代表CH4的曲线是_______ (填“a”、 “b”或 “c”);温度低于500℃时,CO的物质的量分数约为0,说明此条件下,反应_______ (填“ i”或“ii”)化学平衡常数大,反应完全。
②M点(T <500℃)时,平衡分压p(CO2) =_______ atm,反应CO2(g) +4H2(g)  CH4(g) +2H2O(g)的平衡常数Kp=
CH4(g) +2H2O(g)的平衡常数Kp=_______ atm -2(用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)。
III.CO2甲烷化生成的H2O电解再生氧气
(6)电解时阳极产生O2的电极反应式为_______ 。
气。其技术路线可分为以下三步:
I.固态胺吸收与浓缩CO2
(1)在水蒸气存在下固态胺吸收CO2反应生成酸式碳酸盐(该反应是放热反应) ,再解吸出CO2的简单方法是
II.CO2的加氢甲烷化
H2还原CO2制CH4的部分反应如下:
i. CO2(g) + H2(g)
ii. CO(g) +3H2(g)
(2)反应CO2(g) +4H2(g)
(3)有利于提高甲烷平衡产率的反应条件是
(4)科学家研究在催化剂表面上CO2与H2的反应,前三步历程如图所示,吸附在催化剂表面上的物种用“·”标注,Ts表示过渡态。下列说法中一定正确的是_______(填字母)。

| A.第一步历程中只发生了非极性共价键的断裂 |
| B.该转化反应的速率取决于Ts1的能垒 |
| C.·HOCO转化为·CO和·OH的反应△H<0 |
| D.催化剂参与化学反应,能降低反应的活化能,提高反应物的平衡转化率 |

①图中代表CH4的曲线是
②M点(T <500℃)时,平衡分压p(CO2) =
III.CO2甲烷化生成的H2O电解再生氧气
(6)电解时阳极产生O2的电极反应式为
2022年4月16日,中国空间站的3名航天员乘神舟十三号载人飞船平安返回地球。空间站处理CO2的一种重要方法是对CO2进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:
I.固态胺吸收与浓缩CO2
在水蒸气存在下固态胺吸收CO2反应生成酸式碳酸盐(该反应是放热反应),再解吸出CO2的简单方法是加热。
II.CO2的加氢甲烷化
H2还原CO2制CH4的部分反应如下:
i.CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41kJ•mol-1
CO(g)+H2O(g) △H1=+41kJ•mol-1
ii.CO(g)+3H2(g) CH4(g)+H2O(g) △H2=-246kJ•mol-1
CH4(g)+H2O(g) △H2=-246kJ•mol-1
(1)反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的△H=
CH4(g)+2H2O(g)的△H=________ kJ•mol-1。
(2)有利于提高甲烷平衡产率的反应条件是________ (写一种)。
(3)科学家研究在催化剂表面上CO2与H2的反应,前三步历程如图所示,吸附在催化剂表面上的物种用“•”标注,Ts表示过渡态。下列说法中一定正确的是________ (填字母)。
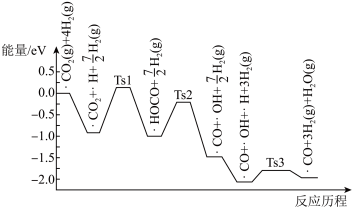
(4)控制起始时 =4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
=4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
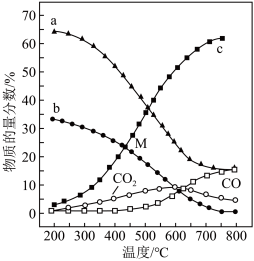
①图中代表CH4的曲线是_______ (填“a”、“b”或“c”);温度低于500℃时,CO的物质的量分数约为0,说明此条件下,反应_______ (填“i”或“ii”)化学平衡常数大,反应完全。
②M点(T<500℃)时,平衡分压p(CO2)=_______ atm,反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的平衡常数Kp=
CH4(g)+2H2O(g)的平衡常数Kp=_______ atm-2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
III.CO2甲烷化生成的H2O电解再生氧气。
(5)电解时阳极产生O2的电极反应式为_______ 。
I.固态胺吸收与浓缩CO2
在水蒸气存在下固态胺吸收CO2反应生成酸式碳酸盐(该反应是放热反应),再解吸出CO2的简单方法是加热。
II.CO2的加氢甲烷化
H2还原CO2制CH4的部分反应如下:
i.CO2(g)+H2(g)
ii.CO(g)+3H2(g)
(1)反应CO2(g)+4H2(g)
(2)有利于提高甲烷平衡产率的反应条件是
(3)科学家研究在催化剂表面上CO2与H2的反应,前三步历程如图所示,吸附在催化剂表面上的物种用“•”标注,Ts表示过渡态。下列说法中一定正确的是

| A.第一步历程中只发生了非极性共价键的断裂 |
| B.该转化反应的速率取决于Ts1的能垒 |
| C.•HOCO转化为•CO和•OH的反应△H<0 |
| D.催化剂参与化学反应,能降低反应的活化能,提高反应物的平衡转化率 |
(4)控制起始时

①图中代表CH4的曲线是
②M点(T<500℃)时,平衡分压p(CO2)=
III.CO2甲烷化生成的H2O电解再生氧气。
(5)电解时阳极产生O2的电极反应式为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网