单选题 适中0.65 引用1 组卷42
2SO2(g)+O2(g)  2SO3(g) ΔH 的反应机理如下:
2SO3(g) ΔH 的反应机理如下:
反应I:V2O5(s)+SO2(g) V2O4(s)+SO3(g) ΔH1=+24 kJ·mol-1
V2O4(s)+SO3(g) ΔH1=+24 kJ·mol-1
反应II:2V2O4(s)+O2(g) 2V2O5(s) ΔH2=-246 kJ·mol-1
2V2O5(s) ΔH2=-246 kJ·mol-1
反应中的能量变化如图,下列说法不正确的是

反应I:V2O5(s)+SO2(g)
反应II:2V2O4(s)+O2(g)
反应中的能量变化如图,下列说法不正确的是

| A.ΔH=-198kJ·mol-1 | B.反应速率由反应I决定 |
| C.反应II的平衡常数K=c-1(O2) | D.通入过量空气,可提高SO2的平衡转化率 |
22-23高二上·山西晋中·期末
类题推荐
已知2H2O(l)=2H2(g)+O2(g) ∆H=+571.0 kJ·mol-1,两步热循环制H2的过程如图。下列说法正确的是
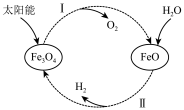
过程I:2Fe3O4(s)=6FeO(s)+O2(g) ∆HⅠ =+604.8 kJ·mol-1
过程II:H2O(l)+3FeO(s)=Fe3O4(s)+H2(g) ∆H II

过程I:2Fe3O4(s)=6FeO(s)+O2(g) ∆HⅠ =+604.8 kJ·mol-1
过程II:H2O(l)+3FeO(s)=Fe3O4(s)+H2(g) ∆H II
| A.该制氢过程中FeO为催化剂 |
| B.整个过程中能量转化形式只存在太阳能转化为化学能 |
| C.过程II在任何温度下均为自发反应 |
| D.根据盖斯定律∆H I+∆H II=0 |
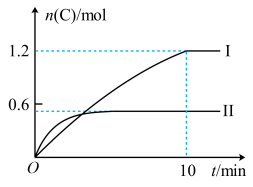
在2L恒容密闭容器中,发生反应A(g)+B(g) ⇌ 2C(g)+D(s) △H=-akJ·mol-1,有关实验内容和结果分别如表和如图所示。下列说法正确的是( )
| 实验 序号 | 温度 | 起始物质的量 | 平衡时 热量变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1 mol | 3 mol | 96 kJ |
| Ⅱ | 800℃ | 0.5 mol | 1.5mol | —— |

| A.实验I中,10 min内平均速率υ(B)=0.06mol·L-1·min-1 |
| B.600℃时,上述热化学方程式中a=160 |
| C.600℃时,该反应的平衡常数K=0.45 |
| D.向实验II的平衡体系中再充入0.5molA和1.5molB,A的转化率增大 |
煤的液化可以合成甲醇。下列有关说法正确的是
①“气化”:C(s)+2H2O(g) =CO2(g)+2H2(g);△H1= 90.1kJ•mol-1
②催化液化I:CO2(g)+3H2(g)= CH3OH(g)+H2O(g) ;△H2= -49.0kJ•mol-1
③催化液化II:CO2(g)+2H2(g)=H3OH(g)+ O2(g) ;△H3= akJ•mol-1
O2(g) ;△H3= akJ•mol-1
①“气化”:C(s)+2H2O(g) =CO2(g)+2H2(g);△H1= 90.1kJ•mol-1
②催化液化I:CO2(g)+3H2(g)= CH3OH(g)+H2O(g) ;△H2= -49.0kJ•mol-1
③催化液化II:CO2(g)+2H2(g)=H3OH(g)+
| A.催化液化I中使用催化剂,反应的活化能Ea、△H2都减小 |
| B.反应C(s)+H2O(g) +H2(g)=CH3OH(g) △H= 41.1 kJ•mol-1 |
| C.△H2>△H3 |
D.下图为甲醇燃料电池的工作原理,负极的电极反应为: CH3OH-6e-+6OH-= CO2+5H2O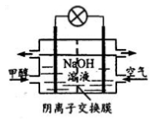 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


