解答题-原理综合题 适中0.65 引用2 组卷256
亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g)⇌2NOCl(g)。
(1)在1L恒容密闭容器中充入2molNO(g)和1molCl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:___________ mol·L-1·min-1。
②T2时该反应的平衡常数K=___________ 。
③T2时Cl2的平衡转化率为___________ 。
(2)若按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:___________ (填“>”“<”或“=”)0。
②在p压强条件下,M点时容器内NO的体积分数为___________ 。
③若反应一直保持在p压强条件下进行,则M点的压强平衡常数Kp=___________ (用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(1)在1L恒容密闭容器中充入2molNO(g)和1molCl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:
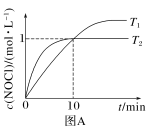
②T2时该反应的平衡常数K=
③T2时Cl2的平衡转化率为
(2)若按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:
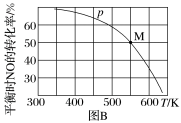
②在p压强条件下,M点时容器内NO的体积分数为
③若反应一直保持在p压强条件下进行,则M点的压强平衡常数Kp=
23-24高三上·河南周口·阶段练习
类题推荐
亚硝酰氯(NOCl)是有机合成中的重要试剂。可通过反应制得:
NO(g)+Cl2(g)⇌2ClNO(g)
(1)氮氧化物与悬浮在大气的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g)⇌2ClNO(g) K3
则K3=___________ (用K1和K2表示)
(2)300℃时,2NO(g)+Cl2(g)⇌2ClNO(g)的正应速率表达式为v正=k•cn(ClNO),测得速率和浓度的关系如下表:
n=____________ ;k=_____________ 。
(3)按投料比[n(NO) ∶n(Cl2)]=2∶1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强P(总压)的关系如图A所示:
①该反应的△H_______ 0(填“>”“<”或“=”)
②在P压强条件下,M点时容器内NO的体积分数为_________________ 。
③若反应一直保持在P 压强条件下进行,则M点的分压平衡常数Kp=________ (用含P的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2 (g),平衡时ClNO的体积分数随n(NO) /n(Cl2)的变化如图B,则A、B、C三状态中NO的转化率最大的是__________ ;当n(NO) /n(Cl2)=1.5时,达到平衡状态C1NO的体积分数可能是D、E、F三点中的_________ 点。
NO(g)+Cl2(g)⇌2ClNO(g)
(1)氮氧化物与悬浮在大气的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g)⇌2ClNO(g) K3
则K3=
(2)300℃时,2NO(g)+Cl2(g)⇌2ClNO(g)的正应速率表达式为v正=k•cn(ClNO),测得速率和浓度的关系如下表:
| 序号 | c (C1NO) /(mol/L) | v/(×10-8mol·L·s) |
| ① | 0.30 | 0.36 |
| ② | 0.60 | 1.44 |
| ③ | 0.90 | 3.24 |
n=
(3)按投料比[n(NO) ∶n(Cl2)]=2∶1把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强P(总压)的关系如图A所示:
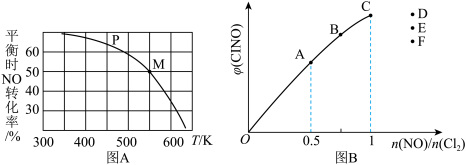
①该反应的△H
②在P压强条件下,M点时容器内NO的体积分数为
③若反应一直保持在P 压强条件下进行,则M点的分压平衡常数Kp=
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2 (g),平衡时ClNO的体积分数随n(NO) /n(Cl2)的变化如图B,则A、B、C三状态中NO的转化率最大的是
亚硝酰氯(ClNO)是有机合成中的重要试剂.可通过反应获得:2NO(g)+Cl2(g) 2ClNO(g)
2ClNO(g)
(1)300℃时,2NO(g)+Cl2(g) 2ClNO(g)的正反应速率表达式为v正=k•cn(ClNO),测得速率和浓度的关系如表:
2ClNO(g)的正反应速率表达式为v正=k•cn(ClNO),测得速率和浓度的关系如表:
n=___ ;k=___ 。
(2)按投料比[n(NO):n(Cl2)=2:1]把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强P(总压)的关系如图A所示:
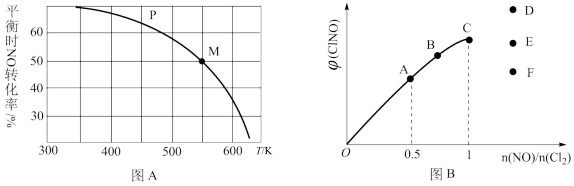
①在P压强条件下,M点时容器内NO的体积分数为___ ;
②若反应一直保持在P压强条件下进行,则M点的分压平衡常数Kp=___ (用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随 变化图象如图B,,则A、B、C三状态中NO转化率最大的是
变化图象如图B,,则A、B、C三状态中NO转化率最大的是___ 点;当 =1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的
=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的___ 点。
(1)300℃时,2NO(g)+Cl2(g)
| 序号 | c(ClNO)/(mol/L) | v/(×10-8mol•L-1•s-1) |
| ① | 0.30 | 0.36 |
| ② | 0.60 | 1.44 |
| ③ | 0.90 | 3.24 |
(2)按投料比[n(NO):n(Cl2)=2:1]把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强P(总压)的关系如图A所示:

①在P压强条件下,M点时容器内NO的体积分数为
②若反应一直保持在P压强条件下进行,则M点的分压平衡常数Kp=
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随
亚硝酰氯(ClNO)是有机合成中的重要试剂,可通过反应Cl2(g)+2NO(g) 2ClNO(g)获得。
2ClNO(g)获得。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
①2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s) 2NaNO3(s)+ 2NO(g)+Cl2(g) K2
2NaNO3(s)+ 2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g) 2ClNO(g) K3
2ClNO(g) K3
则K3=______ (用K1、K2表示)。
(2)300℃时,2NO(g)+Cl2(g) 2ClNO(g)的正反应速率表达式为v正=k·cn(ClNO),测得速率和浓度的关系如下表所示:
2ClNO(g)的正反应速率表达式为v正=k·cn(ClNO),测得速率和浓度的关系如下表所示:
k=________ L·mol-1·s-1。
(3)按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图所示:
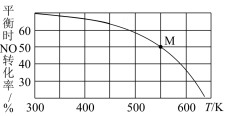
①在p压强条件下,M点时容器内NO的体积分数为______ 。
②若反应一直保持在p压强条件下进行,则M点的压强平衡常数Kp=_____ (用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时,涉及如下反应:
①2NO2(g)+NaCl(s)
②4NO2(g)+2NaCl(s)
③2NO(g)+Cl2(g)
则K3=
(2)300℃时,2NO(g)+Cl2(g)
| 序号 | c(ClNO)/(mol·L-1) | v/(×10-8 mol·L-1·s-1) |
| ① | 0.30 | 0.36 |
| ② | 0.60 | 1.44 |
| ③ | 0.90 | 3.24 |
(3)按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图所示:

①在p压强条件下,M点时容器内NO的体积分数为
②若反应一直保持在p压强条件下进行,则M点的压强平衡常数Kp=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


