填空题 较难0.4 引用1 组卷237
V2O5-WO3/TiO2催化剂可以催化NH3脱除烟气中的NO,反应为:4NO(g) + 4NH3(g) + O2(g)=4N2(g) + 6H2O(g)  =-1632.4kJ·mol-1,工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备V2O5,主要经过“焙烧、水浸、除杂、沉钒、煅烧”等过程。
=-1632.4kJ·mol-1,工业上以石煤(主要成分为V2O3,含有少量SiO2、P2O5等杂质)为原料制备V2O5,主要经过“焙烧、水浸、除杂、沉钒、煅烧”等过程。
已知:NaVO3溶于水,NH4VO3难溶于水。
回答下列问题:
(1)向石煤中加纯碱,在通入空气的条件下焙烧, 转化为
转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“沉钒”时加入NH4Cl析出NH4VO3,沉钒温度需控制在50℃左右,温度不能过高的原因为___________ ;在水溶液中VO 水解为H3VO4沉淀的离子方程式为
水解为H3VO4沉淀的离子方程式为___________ 。
(3)还原V2O5可制得VO2,下图为VO2的晶胞,该晶胞中钒的配位数为___________ 。

(4)催化剂的应用。将模拟烟气(含NO、NH3、N2、O2)以一定流速通过装有V2O5-WO3/TiO2催化剂的反应管,反应相同时间,测得NO的转化率随温度的变化如图所示,反应温度高于350℃,NO转化率下降的原因可能是___________ 。

(5)为测定回收所得V2O5样品的纯度,进行如下实验:称取2.000g样品,用稀硫酸溶解、定容得100mL (VO2)2SO4溶液,量取20.00mL溶液放入锥形瓶中,加入10.00mL 0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液24.00mL,滴定过程中发生如下反应:
VO +Fe2++2H+ = VO2++Fe3++H2O;MnO
+Fe2++2H+ = VO2++Fe3++H2O;MnO +5Fe2++ 8H+ = Mn2++5Fe3++4H2O。
+5Fe2++ 8H+ = Mn2++5Fe3++4H2O。
则V2O5样品的纯度为___________ 。(写出计算过程)
已知:NaVO3溶于水,NH4VO3难溶于水。
回答下列问题:
(1)向石煤中加纯碱,在通入空气的条件下焙烧,
(2)“沉钒”时加入NH4Cl析出NH4VO3,沉钒温度需控制在50℃左右,温度不能过高的原因为
(3)还原V2O5可制得VO2,下图为VO2的晶胞,该晶胞中钒的配位数为

(4)催化剂的应用。将模拟烟气(含NO、NH3、N2、O2)以一定流速通过装有V2O5-WO3/TiO2催化剂的反应管,反应相同时间,测得NO的转化率随温度的变化如图所示,反应温度高于350℃,NO转化率下降的原因可能是

(5)为测定回收所得V2O5样品的纯度,进行如下实验:称取2.000g样品,用稀硫酸溶解、定容得100mL (VO2)2SO4溶液,量取20.00mL溶液放入锥形瓶中,加入10.00mL 0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液24.00mL,滴定过程中发生如下反应:
VO
则V2O5样品的纯度为
23-24高二上·江苏南京·期末
类题推荐
五氧化二钒(V2O5)是广泛用于冶金、化工等行业的催化剂。由富钒废渣制备V2O5的一种流程如下:
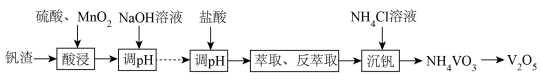
已知:i.NaVO3溶于水,NH4VO3难溶于水。
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
(1)“酸浸”时,MnO2将VO+转化为 的离子反应方程式为
的离子反应方程式为___________ 。
(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO3溶液。
已知 能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为:
能被有机萃取剂(简称ROH)萃取,其萃取原理可表示为: 。
。
①萃取前,加盐酸调节溶液的pH为7的目的是___________ 。
②反萃取中, 反萃取率随着pH的升高呈现先增大后减小的趋势的原因是
反萃取率随着pH的升高呈现先增大后减小的趋势的原因是___________ 。
(3)“沉钒”时,向pH为8的NaVO3溶液中加入NH4Cl溶液,析出NH4VO3沉淀。沉钒温度需控制在70℃左右,温度不能过高的原因是___________ 。
(4)NH4VO3在空气中灼烧得V2O5。为测定回收所得V2O5样品的纯度,进行如下实验:称取1.000g灼烧后的样品,用稀硫酸溶解、定容得100mL(VO2)2SO4溶液。量取20.00mL溶液放入锥形瓶中,加入过量的5.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液12.00mL。
已知: ;
;
 。
。
计算V2O5样品的纯度(写出计算过程)。___________ 。
(5)用活化后的V2O5作催化剂,NH3将NO还原为N2的一种反应历程如图所示。V2O5与H2O形成能提供质子的酸性位,NH3以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X反应生成不稳定的“过渡态”物质,随后分解生成N2和H2O。“中间体X”的结构式可表示为:___________ 。


已知:i.NaVO3溶于水,NH4VO3难溶于水。
ii.部分含钒(五价)物质在水溶液中的主要存在形式:
| pH | <1.0 | 1.0~4.0 | 4.0~6.0 | 6.0~8.5 | 8.5~13.0 | >13.0 |
| 主要存在形式 | V2O5 | 多钒酸根 | 多钒酸根 | |||
| 备注 | 多钒酸盐在水中溶解度较小 | |||||
(2)通过“调pH、萃取、反萃取”等过程,可制得NaVO3溶液。
已知
①萃取前,加盐酸调节溶液的pH为7的目的是
②反萃取中,
(3)“沉钒”时,向pH为8的NaVO3溶液中加入NH4Cl溶液,析出NH4VO3沉淀。沉钒温度需控制在70℃左右,温度不能过高的原因是
(4)NH4VO3在空气中灼烧得V2O5。为测定回收所得V2O5样品的纯度,进行如下实验:称取1.000g灼烧后的样品,用稀硫酸溶解、定容得100mL(VO2)2SO4溶液。量取20.00mL溶液放入锥形瓶中,加入过量的5.00mL0.5000mol·L-1(NH4)2Fe(SO4)2溶液,再用0.01000mol·L-1KMnO4标准溶液滴定至终点,消耗标准溶液12.00mL。
已知:
计算V2O5样品的纯度(写出计算过程)。
(5)用活化后的V2O5作催化剂,NH3将NO还原为N2的一种反应历程如图所示。V2O5与H2O形成能提供质子的酸性位,NH3以“氢键”形式吸附在酸性位上生成“中间体X”;NO与X反应生成不稳定的“过渡态”物质,随后分解生成N2和H2O。“中间体X”的结构式可表示为:

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网






