解答题-原理综合题 适中0.65 引用1 组卷44
甲醇(CH3OH)是重要有机化工原料,现在全球的能源紧张,甲醇需求也在增大。利用合成气(主要成分为CO和H2)在催化剂的作用下合成甲醇的方法是:CO(g)+2H2(g) CH3OH(g) ∆H。
CH3OH(g) ∆H。
(1)已知该反应为自发反应,则∆H___________ 0。(填“>”,“<”或“=”)
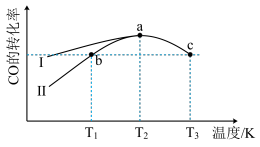
(2)向恒容密闭容器中充入一定量的CO和H2,在使用不同催化剂时,相同时间t内测得CO的转化率随温度的变化如下图所示,有关说法不正确的是___________。
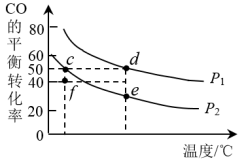
(3)已知:v(正)=k(正)·p(CO)·p2(H2),v(逆)=k(逆)·p(CH3OH);p(CO),p(H2),p(CH3OH)为各组分气体的分压(分压=气体的物质的量分数×体系总压)。在密闭容器中按物质的量之比为1:2充入CO和H2,测得平衡混合气体中CO的平衡转化率随温度、压强的变化关系如图所示。
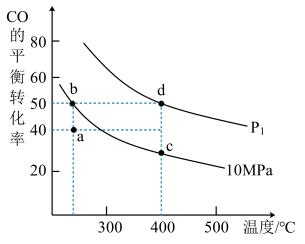
①P1___________ 10Mpa(填“>”或“<”);
②b、c、d三点平衡常数Kb、Kc、Kd三者之间的关系为___________ 。
③实际工业生产往往采用300-400℃和10Mpa的条件,其原因可能有___________ 。(至少写出两方面的原因)
④在10Mpa下,求a点的 =
=___________ 。(保留1位小数)
(1)已知该反应为自发反应,则∆H
(2)向恒容密闭容器中充入一定量的CO和H2,在使用不同催化剂时,相同时间t内测得CO的转化率随温度的变化如下图所示,有关说法不正确的是___________。

| A.使用催化剂Ⅰ时,反应的活化能较高 |
| B.b点时v正>v逆。 |
| C.KT1对应的平衡常数等于KT3对应的平衡常数 |
| D.在相同时间t内,理论上最佳生产温度应为T2 |
(3)已知:v(正)=k(正)·p(CO)·p2(H2),v(逆)=k(逆)·p(CH3OH);p(CO),p(H2),p(CH3OH)为各组分气体的分压(分压=气体的物质的量分数×体系总压)。在密闭容器中按物质的量之比为1:2充入CO和H2,测得平衡混合气体中CO的平衡转化率随温度、压强的变化关系如图所示。

①P1
②b、c、d三点平衡常数Kb、Kc、Kd三者之间的关系为
③实际工业生产往往采用300-400℃和10Mpa的条件,其原因可能有
④在10Mpa下,求a点的
23-24高二上·河南信阳·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网