解答题-实验探究题 适中0.65 引用1 组卷45
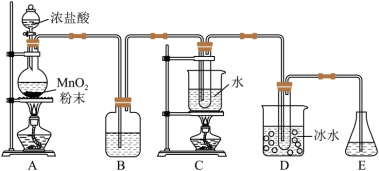
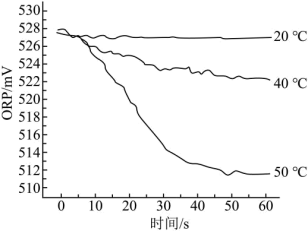
某学习小组设计了如下实验,探究浓度和温度对反应的影响。
实验探究Ⅰ:
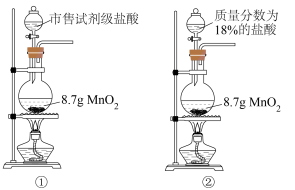
已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:___________ ;①中发生反应的离子方程式为___________ ;8.7gMnO2与33.1mL市售试剂级盐酸在加热条件下反应,生成氯气的物质的量是否为0.1mol?______ (填“是"或“否),并简述其原因:___________ 。
实验探究Ⅱ:
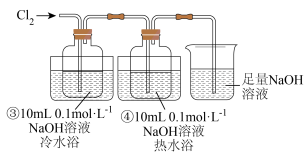
(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:___________ 。
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:___________ 。
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为___________ (用离子方程式解释)。
实验探究Ⅰ:

已知市售试剂级盐酸的密度为1.19g/mL,质量分数为37%;质量分数低于20%的盐酸为稀盐酸。
(1)装置①②同时加热,①中生成黄绿色气体,②中无明显变化,请从浓度和还原性的角度简要解释其原因:
实验探究Ⅱ:

(2)通入氯气后,取出2mL装置③反应瓶中无色液体置于试管中,滴加2滴紫色石蕊溶液,溶液变蓝后褪色,请用简要的语言叙述其原因:
(3)装置④中氧化产物和还原产物的物质的量之比为1:5,写出该反应的离子方程式并用双线桥表示电子转移的方向和数目:
(4)装置③中所得溶液称之为“84”消毒液,其不能与洁厕灵(含盐酸)同时使用的原因为
23-24高一上·江西·阶段练习
类题推荐
某实验小组想探究实验室用MnO2与盐酸反应制取氯气的反应条件,实验装置及药品如下。
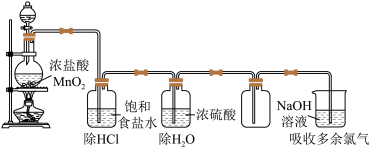
(1)写出实验室制氯气的离子方程式_______ 。
(2)结合平衡移动原理,解释饱和食盐水的作用是_______ 。
(3)已知:不同温度下MnO2与盐酸反应的平衡常数
MnO2与盐酸的反应是_______ 反应(填“放热”或“吸热”)。
(4)为探究条件对该反应的影响,小组同学设计并完成以下实验:
①根据上述实验可知MnO2与盐酸产生氯气的反应条件为_______ 。
②针对实验1和实验3的现象,小组同学从电极反应角度分析物质氧化性和还原性的变化规律。
写出实验中制氯气反应的电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:_______ 。
提出假设:
ⅰ.增大c(H+),可以_______ 。
ⅱ.增大c(Cl-),可以增大Cl-的还原性。
③补充实验,实验II、III分别证实了②中的分析。
(固液混合物A为一定浓度的盐酸和MnO2混合物;加热装置已略去)
较浓a溶液是_______ ,固体b是_______ 。

(1)写出实验室制氯气的离子方程式
(2)结合平衡移动原理,解释饱和食盐水的作用是
(3)已知:不同温度下MnO2与盐酸反应的平衡常数
| 温度t/℃ | 50 | 80 | 110 |
| 平衡常数K | 3.104×10-4 | 2.347×10-3 | 1.293×10-2 |
(4)为探究条件对该反应的影响,小组同学设计并完成以下实验:
| 序号 | 试剂 | 实验操作 | 现象 |
| 实验1 | 4 mol/L盐酸、MnO2 | 加热 | 无明显现象 |
| 实验2 | 7 mol/L浓盐酸、MnO2 | 不加热 | 无明显现象 |
| 实验3 | 7 mol/L浓盐酸、MnO2 | 加热 | 产生黄绿色气体 |
②针对实验1和实验3的现象,小组同学从电极反应角度分析物质氧化性和还原性的变化规律。
写出实验中制氯气反应的电极反应式:
i.还原反应:MnO2+2e-+4H+=Mn2++2H2O
ii.氧化反应:
提出假设:
ⅰ.增大c(H+),可以
ⅱ.增大c(Cl-),可以增大Cl-的还原性。
③补充实验,实验II、III分别证实了②中的分析。
| 实验序号 | 实验操作 | 试剂 | 产物 |
| I |  | 没有添加新的试剂 | 无氯气生成 |
| II | 较浓a溶液 | 有氯气生成 | |
| III | 固体b | 有氯气生成 |
较浓a溶液是
某小组同学探究高铁酸钾(K2FeO4)的制备条件及性质。
资料:K2FeO4为紫色固体,有强氧化性,酸性条件下分解放出气体,微溶于KOH溶液。
Ⅰ:K2FeO4的制备(夹持和加热装置已略)___________ 。
(2)C中得到紫色固体和紫色溶液,写出C中Cl2发生的反应: 和
和___________ 。
(3)实验表明:C中 和KOH的用量对K2FeO4的产率有影响。
和KOH的用量对K2FeO4的产率有影响。
注:上述实验中,溶液总体积、 的物质的量、Cl2的通入量均相同。
的物质的量、Cl2的通入量均相同。
结合电极反应式,分析实验ⅰ和实验ⅱ现象不同的原因可能是___________ 。
Ⅱ:探究K2FeO4的性质
实验ⅲ:取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a。
取少量a,滴加KSCN溶液至过量,溶液呈红色。
(4)根据气体中有Cl2生成,得出:氧化性K2FeO4>Cl2,是否合理?理由是___________ 。
(5)a溶液变红可知a中含有 离子,但该离子的产生不能判断一定是K2FeO4将
离子,但该离子的产生不能判断一定是K2FeO4将 氧化,还可能由
氧化,还可能由___________ 产生(用离子方程式表示)。
(6)实验ⅳ:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。该方案可证明K2FeO4氧化了 。用KOH溶液洗涤的目的是
。用KOH溶液洗涤的目的是___________ 。
(7)实验反思
①实验一中装置B的作用是___________ 。
②实验一中得到紫色溶液后,持续通入Cl2,观察到溶液紫色变浅。解释可能原因___________ 。
资料:K2FeO4为紫色固体,有强氧化性,酸性条件下分解放出气体,微溶于KOH溶液。
Ⅰ:K2FeO4的制备(夹持和加热装置已略)
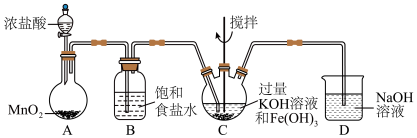
(2)C中得到紫色固体和紫色溶液,写出C中Cl2发生的反应:
(3)实验表明:C中
| 实验序号 | 试剂 | C中实验现象 |
| ⅰ | 无明显现象 | |
| ⅱ | 得到紫色溶液和紫色固体 |
结合电极反应式,分析实验ⅰ和实验ⅱ现象不同的原因可能是
Ⅱ:探究K2FeO4的性质
实验ⅲ:取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a。
取少量a,滴加KSCN溶液至过量,溶液呈红色。
(4)根据气体中有Cl2生成,得出:氧化性K2FeO4>Cl2,是否合理?理由是
(5)a溶液变红可知a中含有
(6)实验ⅳ:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b.取少量b,滴加盐酸,有Cl2产生。该方案可证明K2FeO4氧化了
(7)实验反思
①实验一中装置B的作用是
②实验一中得到紫色溶液后,持续通入Cl2,观察到溶液紫色变浅。解释可能原因
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网