解答题-实验探究题 适中0.65 引用1 组卷92
某小组探究Na2CO3和NaHCO3的性质。
(1)探究溶解性。在两支试管中,分别加入约1g Na2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是______ 。
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。
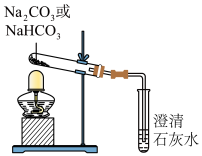
①能够证明Na2CO3的热稳定性强于NaHCO3的证据是______ 。
②NaHCO3受热分解的化学方程式是______ 。
(3)探究与酸的反应。
(4)该小组在探究Na2CO3和NaHCO3的性质时,运用的化学思想方法有______ (填序号)。
a.比较 b.定性与定量相结合
(1)探究溶解性。在两支试管中,分别加入约1g Na2CO3和NaHCO3固体,分别加入5mL水,充分振荡后,一支试管中固体有剩余,剩余的固体是
(2)探究稳定性。按照如图所示装置进行实验(部分夹持装置已略去)。

①能够证明Na2CO3的热稳定性强于NaHCO3的证据是
②NaHCO3受热分解的化学方程式是
(3)探究与酸的反应。
实验步骤 | 实现现象 | 用离子方程式解释现象 |
向盛有Na2CO3溶液的试管中滴加稀盐酸 | 开始无气泡产生,一段时间后产生气泡 | ① ② |
向盛有NaHCO3溶液的试管中滴加稀盐酸 | 立即产生气泡 |
(4)该小组在探究Na2CO3和NaHCO3的性质时,运用的化学思想方法有
a.比较 b.定性与定量相结合
23-24高一上·北京西城·期末
类题推荐
实验小组探究 Na2CO3和 NaHCO3的性质。
【进行实验】
(1)写出实验 1 中 NaHCO3与盐酸反应的离子方程式______________ 。
(2)①把表格中实验 2 的现象补充完整:____________________________
②写出试管 2 中 NaHCO3与少量澄清石灰石反应的离子反应方程式________________ 。
(3)① 实验 3 中,写出 NaHCO3受热分解的化学方程式______________ 。
②称量 NaHCO3固体 168g,加热一段时间之后,剩余固体的质量为 137g,则剩余固体中NaHCO3与 Na2CO3 的物质的量之比为______________ 。
(4)实验 4:研究 NaHCO3和 Na2CO3分别与CaCl2溶液的反应,记录实验如下:
已知:Ca(HCO3)2易溶于水。
① 实验 4 中,NaHCO3 溶液与CaCl2溶液混合的现象中,浓度较大的两个溶液混合观察到浑浊同时产生气体,该沉淀经检验是碳酸钙,该气体经检测是CO2,试写出该反应的离子方程式______________ 。
② 有些只观察到浑浊但没有观察到气体,可能原因是____________ 。
【反思评价】
(5)根据实验 4,鉴别浓度均为 0.50mol/L的Na2CO3 和NaHCO3 的方法是:分别取等量溶液置于两试管中,______________ 。
【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验1 |  | 向两支分别盛有Na2CO3和NaHCO3溶液的试管中,分别滴加盐酸 | 2支试管中均有气泡产生 |
| 实验2 |  | 向两支分别盛有Na2CO3和NaHCO3溶液的试管中分别滴加少量澄清石灰水 | ______________ |
| 实验3 | 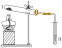 | 向II中加入试剂a,向I中加入少量Na2CO3或NaHCO3固体,分别加热一段时间 | Na2CO3受热时II中无明显现象,NaHCO3受热时II出现浑浊 |
(1)写出实验 1 中 NaHCO3与盐酸反应的离子方程式
(2)①把表格中实验 2 的现象补充完整:
②写出试管 2 中 NaHCO3与少量澄清石灰石反应的离子反应方程式
(3)① 实验 3 中,写出 NaHCO3受热分解的化学方程式
②称量 NaHCO3固体 168g,加热一段时间之后,剩余固体的质量为 137g,则剩余固体中NaHCO3与 Na2CO3 的物质的量之比为
(4)实验 4:研究 NaHCO3和 Na2CO3分别与CaCl2溶液的反应,记录实验如下:
| 实验4 | 物质 | NaHCO3 | Na2CO3 | ||
| 浓度/(mol/L) | 0.01 | 0.10 | 0.50 | 0.01 | |
| CaCl2 | 0.01 | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 0.10 | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 0.50 | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
① 实验 4 中,NaHCO3 溶液与CaCl2溶液混合的现象中,浓度较大的两个溶液混合观察到浑浊同时产生气体,该沉淀经检验是碳酸钙,该气体经检测是CO2,试写出该反应的离子方程式
② 有些只观察到浑浊但没有观察到气体,可能原因是
【反思评价】
(5)根据实验 4,鉴别浓度均为 0.50mol/L的Na2CO3 和NaHCO3 的方法是:分别取等量溶液置于两试管中,
实验小组探究 和
和 的性质。
的性质。
【进行实验】
(1)写出实验1中 与盐酸反应的离子方程式
与盐酸反应的离子方程式___________ 。
(2)①实验2中,试剂a是___________ ,此实验得出的结论是___________ 。
②称量 固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中
固体168g,加热一段时间之后,剩余固体的质量为137g,则剩余固体中 与
与 的物质的量之比为
的物质的量之比为___________ 。
已知: 易溶于水。
易溶于水。
(3) 溶液与
溶液与 溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是
溶液混合的现象中,有些只观察到浑浊但没有观察到气体,可能原因是___________ 。
(4)写出溶液中 与
与 反应的离子方程式
反应的离子方程式___________ 。
【反思评价】
(5)根据实验3,鉴别浓度均为0.50 的
的 和
和 的方法是:分别取等量溶液置于两试管中,
的方法是:分别取等量溶液置于两试管中,___________ 。
【进行实验】
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
| 实验1 |  | 向2支试管中分别加入少量 | 2支试管中均有气泡产生 |
| 实验2 | 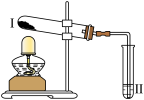 | 向Ⅱ中加入试剂a,向Ⅰ中加入少量 |
(1)写出实验1中
(2)①实验2中,试剂a是
②称量
| 实验3 | |||||
| 浓度/ | 0.01 | 0.10 | 0.50 | 0.01 | |
| 0.01 | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 | |
| 0.10 | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 0.50 | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
已知:
(3)
(4)写出溶液中
【反思评价】
(5)根据实验3,鉴别浓度均为0.50
某小组同学依据性质差异,采用比较的方法设计实验鉴别Na2CO3和NaHCO3。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中___________ (填“放出”或“吸收”)热量,可判断固体b为___________ (填物质的化学式)。
(2)实验Ⅱ中,向试管C和D中分别加入5 mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。
①判断固体c为___________ (填物质的化学式)。
②分别向两支试管中滴加2滴酚酞,___________ 试管中红色较深。(填“C”或“D”)
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因___________ 。
(4)请你再设计一个鉴别Na2CO3和NaHCO3的实验方案:___________ 。
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
 |  |  |
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中
(2)实验Ⅱ中,向试管C和D中分别加入5 mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。
①判断固体c为
②分别向两支试管中滴加2滴酚酞,
(3)实验Ⅲ中,分别向溶液e和溶液f中逐滴加入稀盐酸,F中开始滴加就可以观察到气泡;E中开始无气泡产生,一段时间后产生气泡。结合离子方程式解释E中开始无气泡产生的原因
(4)请你再设计一个鉴别Na2CO3和NaHCO3的实验方案:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


