单选题 适中0.65 引用1 组卷126
在一定温度和催化剂的条件下,将(0.1mol NH3通入3L的恒容密闭容器中进行反应2NH3(g)=N2(g)+3H2(g)(初始容器内总压为200kPa),各物质的分压随时间的变化曲线如下图所示。下列说法错误的是


| A.用H2的浓度变化表示0~t1时间内的反应速率v(H2)=0.02/t1mol |
| B.混合气体的平均相对分子质量不再改变时,反应达平衡 |
| C.在该温度下的压强平衡常数为4800(kPa)2 |
| D.若t2时将容器体积迅速缩小至原来的一半,N2分压变化趋势的曲线是a |
23-24高三上·辽宁大连·期末
类题推荐
在一定温度和催化剂的条件下,发生 。将0.1 mol NH3通入3 L的密闭容器中进行反应(此时容器内总压为200 kPa),各物质的分压随时间的变化曲线如图所示。下列的说法不正确的是
。将0.1 mol NH3通入3 L的密闭容器中进行反应(此时容器内总压为200 kPa),各物质的分压随时间的变化曲线如图所示。下列的说法不正确的是
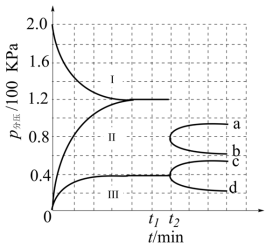

| A.曲线I表示NH3的分压随时间的变化 |
| B.用H2的浓度变化表示0-t1时间内的反应速率 |
| C.t2时将容器体积迅速缩小至原来的一半并保持不变,N2分压变化趋势的曲线是b |
| D.在此温度下该反应的化学平衡常数 |
在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa,已知:分压=总压×该组分物质的量分数),各物质的分压随时间的变化曲线如图所示。下列说法不正确的是
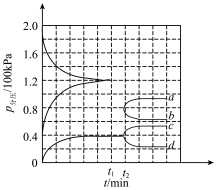

| A.若保持容器体积不变,氨气分压不变可说明反应已达平衡状态 |
| B.若保持容器体积不变,用H2浓度变化表示0~t1时间内的反应速率v(H2)= |
| C.t2时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后N2分压变化趋势的曲线是d |
| D.若保持容器体积不变,t2时充入He,反应仍处于平衡状态,氨气的分压保持不变 |
已知:反应反应2NH3(g) N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是
N2(g)+3H2(g) △H=+akJ•mol﹣1(a>0)。某兴趣小组在一定温度和催化剂的条件下,将1molNH3通入2L的密闭容器中进行反应(此时容器内总压强为200kPa),各物质的分压随时间的变化曲线如图所示。下列有关说法正确的是


| A.若保持容器体积不变,0~t1min内,N2的平均反应速率为 |
| B.若保持容器体积不变,该温度下,当N2和H2的分压比保持不变时,表明反应已达平衡 |
| C.若保持容器体积不变,t1min时,反应放出0.2akJ的热量 |
| D.t2min时,将容器体积迅速缩小一半并保持不变,N2的分压变化如图中曲线b所示 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


