填空题 较难0.4 引用1 组卷90
工业燃煤、石油等化石燃料烧释放出大量 等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。目前,在常温下处理
等气体,严重污染空气。对废气进行处理可实现绿色环保、废物利用。目前,在常温下处理 主要采用碱液吸收法。
主要采用碱液吸收法。
(1)用过量的烧碱溶液吸收 ,发生反应
,发生反应 ,若向所得的
,若向所得的 溶液滴入过氧化氢溶液,发生反应的离子方程式为
溶液滴入过氧化氢溶液,发生反应的离子方程式为_______ 。
(2)研究发现, 溶液也可以用来处理废气中的
溶液也可以用来处理废气中的 ,发生反应
,发生反应 ,查阅资料可知,常温下,
,查阅资料可知,常温下, 电离平衡常数:
电离平衡常数: ,
, 。
。
①写出 发生水解反应的离子方程式:
发生水解反应的离子方程式:_______ ;常温下,该反应的
_______ 。
② 溶液中
溶液中
_______ (填“>”、“<”或“=”) 。
。
(3)常温下,若向 溶液中缓慢通入
溶液中缓慢通入 ,整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入
,整个过程无气体逸出,忽略溶液体积的变化,测得溶液的pH与通入 物质的量之间的变化曲线如图所示:
物质的量之间的变化曲线如图所示:
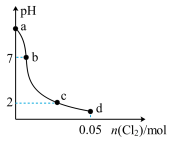
①a点
_______ (精确到小数点后一位)。
②下列说法错误的是_______ (填标号)。
A.c点溶液中存在
B.b点
C.d点溶液中溶质只有 、
、 和
和
D.a点溶液中存在
(4)还可以采用多步法来处理废气中的 :
:
第1步:用过理的浓氨水吸收 ,并在空气中氧化;
,并在空气中氧化;
第2步:加入石灰水,发生反应 K。
K。
则
_______ [已知: ,
, ]。
]。
(1)用过量的烧碱溶液吸收
(2)研究发现,
①写出
②
(3)常温下,若向

①a点
②下列说法错误的是
A.c点溶液中存在
B.b点
C.d点溶液中溶质只有
D.a点溶液中存在
(4)还可以采用多步法来处理废气中的
第1步:用过理的浓氨水吸收
第2步:加入石灰水,发生反应
则
23-24高二上·湖南·阶段练习
类题推荐
硫酸工业的尾气中含 等污染性气体,通常用碱液如氨水进行吸收处理,实现绿色环保和废物利用。研究发现,
等污染性气体,通常用碱液如氨水进行吸收处理,实现绿色环保和废物利用。研究发现, 溶液也可以用来处理废气中的
溶液也可以用来处理废气中的 ,发生反应
,发生反应 。
。
查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
(1)相同物质的量浓度的三种酸溶液 、
、 和
和 由水电离的
由水电离的 最大的是
最大的是_______ (填化学式)
(2)若向 溶液中加入少量水,则溶液中
溶液中加入少量水,则溶液中 将
将_______ (填“增大”、“减小”或“不变”)。
(3)将浓度均为 的
的 和
和 等体积混合,溶液
等体积混合,溶液 。分析该溶液中离子浓度从大到小依次是
。分析该溶液中离子浓度从大到小依次是_______ 。
(4)①下列离子方程式或守恒关系正确的是_______ (填字母)。
A.
B.
C.向亚硫酸溶液中加入氨水至中性:
D. 氨水和
氨水和 溶液等体积混合:
溶液等体积混合: mol/L+c(H2SO3)+c(H+)
mol/L+c(H2SO3)+c(H+)
②向过量 溶液中通入少量
溶液中通入少量 气体,写出离子方程式
气体,写出离子方程式_______ 。
③根据表内数据,计算 溶液的
溶液的
_______ (忽略 的第二步水解)。
的第二步水解)。
(5)测得吸收 后的
后的 和
和 某混合溶液
某混合溶液 ,进行电解制硫酸并再生
,进行电解制硫酸并再生 原理示意图如图所示。
原理示意图如图所示。
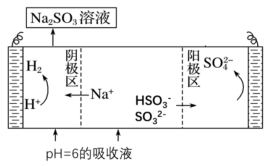
电解时阳极区会产生少量刺激性气体,结合电极方程式分析产生气体的原因是_______ 。
查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
| 弱酸 | |||
| 电离平衡常数 |
(1)相同物质的量浓度的三种酸溶液
(2)若向
(3)将浓度均为
(4)①下列离子方程式或守恒关系正确的是
A.
B.
C.向亚硫酸溶液中加入氨水至中性:
D.
②向过量
③根据表内数据,计算
(5)测得吸收

电解时阳极区会产生少量刺激性气体,结合电极方程式分析产生气体的原因是
硫酸工业的尾气中含SO2等污染性气体,通常用碱液如氨水进行吸收处理,实现绿色环保和废物利用。研究发现,Na2SO3溶液也可以用来处理废气中的SO2,发生反应Na2SO3+SO2+H2O=2NaHSO3,查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
(1)相同物质的量浓度的三种酸溶液HClO、H2CO3和H2SO3由水电离的c(H+)最大的是___________ (填化学式)
(2)若向Na2SO3溶液中加入少量水,则溶液中 将
将___________ (填“增大”、“减小”或“不变”)。
(3)将浓度均为0.1mol/L的NaHSO3和Na2SO3等体积混合,溶液pH=7.2。分析该溶液中离子浓度从大到小依次是___________ 。
(4)下列离子方程式或守恒关系正确的是___________(填字母)。
(5)根据表内数据,计算0.06mol/L Na2SO3溶液的pH=______ (忽略SO 的第二步水解)。
的第二步水解)。
(6)测得吸收SO2后的NaHSO3和Na2SO3某混合溶液pH=6,进行电解制硫酸并再生Na2SO3原理示意图如图所示。
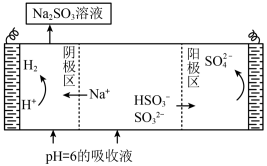
电解时阳极区会产生少量刺激性气体,结合电极方程式分析产生气体的原因是___________ 。
| 弱酸 | HClO | H2CO3 | H2SO3 |
| 电离平衡常数(25℃) | Ka=4.0×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.5×10-2 Ka2=6×10-8 |
(1)相同物质的量浓度的三种酸溶液HClO、H2CO3和H2SO3由水电离的c(H+)最大的是
(2)若向Na2SO3溶液中加入少量水,则溶液中
(3)将浓度均为0.1mol/L的NaHSO3和Na2SO3等体积混合,溶液pH=7.2。分析该溶液中离子浓度从大到小依次是
(4)下列离子方程式或守恒关系正确的是___________(填字母)。
| A.2ClO-+H2O+SO2=2HClO+ SO |
| B.Cl2+H2O+2CO |
| C.向亚硫酸溶液中加入等浓度等体积的氨水:c(NH |
| D.少量 SO2气体通入过量Na2CO3溶液中,反应的离子方程式为:2CO |
(6)测得吸收SO2后的NaHSO3和Na2SO3某混合溶液pH=6,进行电解制硫酸并再生Na2SO3原理示意图如图所示。

电解时阳极区会产生少量刺激性气体,结合电极方程式分析产生气体的原因是
加强对工业废水、废气的处理,可以保护环境,利于健康,某电镀废水中含有重金属铬(Ⅵ)污染物,而硫酸工业会产生废气 ,有人考虑综合处理可降低污染。
,有人考虑综合处理可降低污染。
(1)硫酸工业的尾气中含 等污染性气体,研究发现
等污染性气体,研究发现 溶液可以用来处理废气中的
溶液可以用来处理废气中的 ,产生亚硫酸氢钠,发生反应
,产生亚硫酸氢钠,发生反应 。
。
查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
①常温时, 溶液呈
溶液呈_________ (填“酸”、“碱”或“中”)性,其原因是_________ (用电离方程式表示)。
②相同物质的量浓度的三种酸溶液HClO、 和
和 由水电离的
由水电离的 最大的是
最大的是_________ (填化学式)
③将未知浓度的 和
和 等体积混合,溶液
等体积混合,溶液 ,分析该溶液中
,分析该溶液中
_________  填“>”,“<”或“=”)。
填“>”,“<”或“=”)。
(2)废水中铬(Ⅵ)主要以 和
和 形式存在,处理的方法是将铬(Ⅵ)还原为
形式存在,处理的方法是将铬(Ⅵ)还原为 ,再转化为
,再转化为 沉淀。常温下,
沉淀。常温下, 与
与 在溶液中存在如下平衡:
在溶液中存在如下平衡: ,该反应的平衡常数
,该反应的平衡常数 。
。
①若废水中Cr(Ⅵ)的总的物质的量浓度 mol·L
mol·L ,要将废水中
,要将废水中 调节为
调节为 ,则需调节溶液的
,则需调节溶液的
_________ 。(忽略调节 时溶液体积的变化)
时溶液体积的变化)
②一种还原酸性废水中 的方法是向其中加入
的方法是向其中加入 ,写出
,写出 所发生反应的离子方程式:
所发生反应的离子方程式:_________
(3)有关该平衡 说法正确的是_________(填序号)
说法正确的是_________(填序号)
(1)硫酸工业的尾气中含
查阅资料可知,常温下,部分弱酸的电离平衡常数如表:
| 弱酸 | HClO | ||
| 电离平衡常数(25℃) |
②相同物质的量浓度的三种酸溶液HClO、
③将未知浓度的
(2)废水中铬(Ⅵ)主要以
①若废水中Cr(Ⅵ)的总的物质的量浓度
②一种还原酸性废水中
(3)有关该平衡
| A.反应达平衡时, |
| B.加入少量水稀释,溶液中离子总数增加 |
| C.溶液的颜色不变,说明反应达到平衡 |
| D.加入少量 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


