解答题-原理综合题 适中0.65 引用1 组卷42
回答下列问题
(1)常温下向一定浓度的 溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示,已知:
溶液中滴入盐酸,粒子浓度与混合溶液的pH变化的关系如图所示,已知: 是二元弱酸,Y表示
是二元弱酸,Y表示 或
或 ,
, 。回答下列问题:
。回答下列问题:
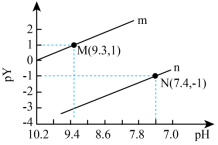
①曲线n表示p_______ (填 或
或 )与pH的变化关系。
)与pH的变化关系。
②
_______ 。
③NaHX溶液呈_______ 性(填“酸”、“碱”或“中”)。
(2)在 溶液中,加入
溶液中,加入 固体可制备莫尔盐[
固体可制备莫尔盐[ ]晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如表:(已知莫尔盐的分子量为392)
]晶体,为了测定产品纯度,称取ag产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如表:(已知莫尔盐的分子量为392)
滴定终点的现象是_______ ,通过实验数据,计算该产品的纯度为_______ (用含字母a、c的式子表示)。表中第一次实验中记录数据明显大于后两次,其原因可能是_______ 。
A.第一次滴定时,锥形瓶用待装液润洗
B.读数时:滴定前平视,滴定后俯视
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
(1)常温下向一定浓度的

①曲线n表示p
②
③NaHX溶液呈
(2)在
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗 | 25.52 | 25.02 | 24.98 |
A.第一次滴定时,锥形瓶用待装液润洗
B.读数时:滴定前平视,滴定后俯视
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
23-24高二上·四川南充·阶段练习
类题推荐
请根据所学知识回答:
(1) 是温室气体,可用NaOH溶液吸收得到
是温室气体,可用NaOH溶液吸收得到 或
或 。已知:25℃时,
。已知:25℃时, ,
, 。
。
① 俗称纯碱,因
俗称纯碱,因 水解而使其水溶液呈碱性,写出
水解而使其水溶液呈碱性,写出 第一步水解的离子方程式
第一步水解的离子方程式___________ 。NaOH溶液吸收 得到的某溶液中,当
得到的某溶液中,当 时,溶液的pH=
时,溶液的pH=___________ 。
②泡沫灭火器中通常装有 溶液和
溶液和 溶液,请写出这两种溶液混合时的离子反应方程式
溶液,请写出这两种溶液混合时的离子反应方程式___________ 。
(2)某温度下,水的离子积常数 ,该温度下,将pH=1的HCl溶液与pH=10的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液pH=3,则盐酸溶液与NaOH溶液的体积比为
,该温度下,将pH=1的HCl溶液与pH=10的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液pH=3,则盐酸溶液与NaOH溶液的体积比为_______ 。
(3)莫尔盐 是一种常用原料。在
是一种常用原料。在 溶液中,加入
溶液中,加入 固体可制备莫尔盐晶体,为了测定产品纯度,称取a克产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如表:(已知莫尔盐的分子量为392)
固体可制备莫尔盐晶体,为了测定产品纯度,称取a克产品溶于水,配制成500mL溶液,用浓度为cmol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00mL,实验结果记录如表:(已知莫尔盐的分子量为392)
滴定终点的现象是_______ ;通过实验数据,计算该产品的纯度为_______ (用含字母a、c的式子表示)。上表第一次实验中记录数据明显大于后两次,其原因可能是_______ 。
A.锥形瓶用待装液润洗
B.滴定达到终点时,俯视刻度线读数
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
(1)
①
②泡沫灭火器中通常装有
(2)某温度下,水的离子积常数
(3)莫尔盐
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗 | 25.52 | 25.02 | 24.98 |
A.锥形瓶用待装液润洗
B.滴定达到终点时,俯视刻度线读数
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
氢叠氮酸(HN3)和莫尔盐 是两种常用原料。
是两种常用原料。
(1)氢叠氮酸易溶于水,25℃时,该酸的电离常数为
①氢叠氮酸在水溶液中的电离方程式为___________ 。
②0.1 mol/L的HN3溶液与0.1 mol/L的NaOH溶液等体积混合后,恢复到25℃时溶液中质子守恒关系式为___________ 。
③已知T℃时, ,
, ,在此温度下,
,在此温度下, ,该反应正反应方向
,该反应正反应方向___________ (填“能”或“不能”)基本进行彻底,请通过计算说明___________ 。
(2)在FeSO4溶液中,加入(NH4)2SO4固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500 mL溶液,用浓度为c mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00 mL,实验结果记录如下(已知莫尔盐的相对分子质量为392):
滴定终点的现象是___________ ,通过实验数据,计算该产品的纯度为___________ (用含字母a、c的式子表示)。上表中第一次实验的记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
(1)氢叠氮酸易溶于水,25℃时,该酸的电离常数为
①氢叠氮酸在水溶液中的电离方程式为
②0.1 mol/L的HN3溶液与0.1 mol/L的NaOH溶液等体积混合后,恢复到25℃时溶液中质子守恒关系式为
③已知T℃时,
(2)在FeSO4溶液中,加入(NH4)2SO4固体可制备莫尔盐晶体,为了测定产品纯度,称取ag产品溶于水,配制成500 mL溶液,用浓度为c mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00 mL,实验结果记录如下(已知莫尔盐的相对分子质量为392):
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.第一次滴定时,锥形瓶用待装液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
氢叠氮酸( )和莫尔盐
)和莫尔盐 是两种常用工业原料。
是两种常用工业原料。
(1) 易溶于水,25℃时,该酸的电离常数为
易溶于水,25℃时,该酸的电离常数为
① 在水溶液中的电离方程式为
在水溶液中的电离方程式为___________ 。
②初始浓度为 的
的 溶液,达电离平衡后,溶液的pH=
溶液,达电离平衡后,溶液的pH=___________ 。
③已知T℃时, ,
, ,在此温度下,
,在此温度下, ,该反应正反应方向
,该反应正反应方向___________ (填“能”或“不能”)基本进行完全(已知但 时,反应就进行的基本完全),请通过计算说明
时,反应就进行的基本完全),请通过计算说明___________ 。
(2)在 溶液中,加入固体
溶液中,加入固体 可制备莫尔盐晶体,为了测定产品纯度,称取
可制备莫尔盐晶体,为了测定产品纯度,称取 产品溶于水,配制成500mL溶液,用浓度为
产品溶于水,配制成500mL溶液,用浓度为 的酸性高锰酸钾溶液滴定,每次所取待测液体积均为
的酸性高锰酸钾溶液滴定,每次所取待测液体积均为 ,实验结果记录如下(已知莫尔盐的相对分子质量为392):
,实验结果记录如下(已知莫尔盐的相对分子质量为392):
滴定终点的现象是___________ ,通过实验数据计算该产品的纯度为___________ (用含字母a、c的式子表示)。上表中第一次实验的记录数据明显大于后两次,其原因可能是___________ (填字母)。
A.第一次滴定时,锥形瓶用待测液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
(1)
①
②初始浓度为
③已知T℃时,
(2)在
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗 | 25.52 | 25.02 | 24.98 |
A.第一次滴定时,锥形瓶用待测液润洗
B.该酸性高锰酸钾标准液保存时间过长,部分变质
C.滴定前酸式滴定管中尖嘴处有气泡,滴定结束后气泡消失
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


