解答题-实验探究题 适中0.65 引用1 组卷159
某兴趣小组设计如图实验装置制备次磷酸钠(NaH2PO2)。
已知:①白磷(P4)在空气中可自燃,与过量烧碱溶液混合,80~ 90℃生成NaH2PO2和PH3。
②PH3是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成NaH2PO2。
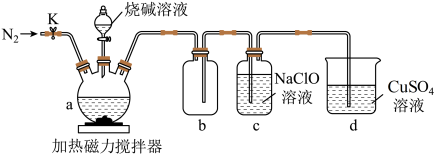
(1)仪器a的名称是___________ ,a 中发生反应的化学方程式是___________ 。
(2)仪器b组成的装置的作用是___________ ,检查装置气密性后,应先打开K通入N2一段时间,目的是___________ 。
(3)下列有关说法正确的是___________ 。
A.次磷酸(H3PO2)是三元酸
B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状
C.d中所盛硫酸铜溶液,可用酸性高锰酸钾溶液代替
(4)①仪器c中充分反应后生成NaH2PO2和NaCl,经过一系列操作可获得固体NaH2PO2,相关物质的溶解度(S)如下:
从下列选项a-g中选择合理的仪器或操作,补全如下步骤。
取仪器c中溶液,用蒸发皿___________→___________(趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到NaH2PO2)→___________→干燥→NaH2PO2粗品。___________
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗 f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式___________ 。
(5)产品纯度的测定:
取产品mg配成250mL溶液,取25mL于锥形瓶中,然后用0.01 KMnO4标准溶液滴定至终点(还原产物是Mn2+,氧化产物是
KMnO4标准溶液滴定至终点(还原产物是Mn2+,氧化产物是 ),达到滴定终点时消耗VmL标准溶液,产品的纯度为
),达到滴定终点时消耗VmL标准溶液,产品的纯度为___________ 。
已知:①白磷(P4)在空气中可自燃,与过量烧碱溶液混合,80~ 90℃生成NaH2PO2和PH3。
②PH3是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成NaH2PO2。

(1)仪器a的名称是
(2)仪器b组成的装置的作用是
(3)下列有关说法正确的是
A.次磷酸(H3PO2)是三元酸
B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状
C.d中所盛硫酸铜溶液,可用酸性高锰酸钾溶液代替
(4)①仪器c中充分反应后生成NaH2PO2和NaCl,经过一系列操作可获得固体NaH2PO2,相关物质的溶解度(S)如下:
| S(25℃) | S(100℃) | |
| NaCl | 37 | 39 |
| NaH2PO2 | 100 | 667 |
取仪器c中溶液,用蒸发皿___________→___________(趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到NaH2PO2)→___________→干燥→NaH2PO2粗品。
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗 f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式
(5)产品纯度的测定:
取产品mg配成250mL溶液,取25mL于锥形瓶中,然后用0.01
23-24高三上·天津·阶段练习
类题推荐
磷化氢(PH3)常用于有机合成、粮仓杀虫等。实验室用白磷(P4)与浓NaOH加热制备PH3,同时得到次磷酸钠(NaH2PO2)装置如下图。

已知,PH3是无色有毒气体,有强还原性,易自燃;丁醇沸点117.7℃)
(1)实验室少量白磷保存于___________
(2)仪器a的名称为___________ ,B应选用下图中装置___________ 。
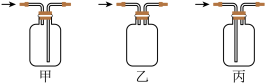
(3)实验操作有如下步骤:
①打开K1,通入N2一段时间;
②检查装置气密性;
③关闭K1,打开磁力加热搅拌器加热至50℃~60℃,滴加烧碱溶液;
④在A中加入丁醇和白磷。
则正确的操作顺序是___________ 。
(4)装置A中发生反应的化学方程式为___________ ,使用丁醇作为反应物的分散剂,目的是___________ 。
(5)反应结束后也要打开K1,继续通入N2的目的是___________ ,装置d的作用是___________ 。
(6)c中生成NaH2PO2和NaCl,相关溶解度(S)如表:
充分反应后c中分离出NaH2PO2粗产品的操作是___________ 过滤、洗涤、干燥。
(7)测定NaH2PO2纯度。
提纯A中反应后的混合物,得到NaH2PO2(M=88·mol-1)粗品,取1.00g配成100 mL溶液,取20.00mL于锥形瓶中,酸化后加入30.00mL 0.100mol·L-1碘水,充分反应,以淀粉溶液作指示剂,用0.100 mol·L-1 Na2S2O3溶液滴定至终点,平均消耗20.00 mL。则产品纯度为___________ 。(相关反应为 ,
, )
)

已知,PH3是无色有毒气体,有强还原性,易自燃;丁醇沸点117.7℃)
(1)实验室少量白磷保存于
(2)仪器a的名称为

(3)实验操作有如下步骤:
①打开K1,通入N2一段时间;
②检查装置气密性;
③关闭K1,打开磁力加热搅拌器加热至50℃~60℃,滴加烧碱溶液;
④在A中加入丁醇和白磷。
则正确的操作顺序是
(4)装置A中发生反应的化学方程式为
(5)反应结束后也要打开K1,继续通入N2的目的是
(6)c中生成NaH2PO2和NaCl,相关溶解度(S)如表:
| S(25℃) | S(100℃) | |
| NaCl | 37 | 39 |
| NaH2PO2 | 100 | 667 |
(7)测定NaH2PO2纯度。
提纯A中反应后的混合物,得到NaH2PO2(M=88·mol-1)粗品,取1.00g配成100 mL溶液,取20.00mL于锥形瓶中,酸化后加入30.00mL 0.100mol·L-1碘水,充分反应,以淀粉溶液作指示剂,用0.100 mol·L-1 Na2S2O3溶液滴定至终点,平均消耗20.00 mL。则产品纯度为
硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g·mol-1),已知它易溶于水,难溶于乙醇,在40~50℃熔化,48℃分解。某兴趣小组用两种方法制取硫代硫酸钠晶体并加以应用。
Ⅰ.制备Na2S2O3·5H2O
方法一:亚硫酸钠法。
反应原理:S+Na2SO3=Na2S2O3
实验步骤:称取一定量的Na2SO3于烧杯中,溶于煮沸过的蒸馏水。另取过量的硫粉,加入少量乙醇充分搅拌均匀后,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶后析出Na2S2O3·5H2O晶体。再进行减压过滤、洗涤并低温干燥。
(1)向硫粉中加入少量乙醇充分搅拌均匀的目的是___________ 。
(2)下列说法不正确的是 ___________。
方法二:硫化碱法,装置如图。

(3)盛放70%硫酸的仪器名称___________ 。
(4)装置C中,通入SO2后Na2S和Na2CO3将以2:1的物质的量之比发生反应制得Na2S2O3和CO2反应的化学方程式为___________ 。
Ⅱ.Na2S2O3的应用
(5)Na2S2O3解毒氰化物原理:S2O +CN-→SCN-+SO
+CN-→SCN-+SO 。为检验该转化生成了SCN-,取反应后的少量溶液,先加入足量的盐酸,再加入的试剂是
。为检验该转化生成了SCN-,取反应后的少量溶液,先加入足量的盐酸,再加入的试剂是 ___________ 。
(6)设计以下实验测定粗产品中Na2S2O3·5H2O的含量:
步骤1:准确称取8.00g样品,溶于水,加入5mL甲醛,配成100ml的溶液。
步骤2:准确称取0.294g(0.001mol) K2Cr2O7于碘量瓶中,加入20mL蒸馏水溶解,再加入5mL1mol·L-1 H2SO4和20mL 10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL 1%淀粉,用待测Na2S2O3溶液滴定碘量瓶中溶液至滴定终点,消耗Na2S2O3溶液20.00mL。(已知:I2+2S2O =2I-+S4O
=2I-+S4O )。
)。
①出“步骤2”中反应的离子方程式___________ 。
②试计算Na2S2O3·5H2O的纯度___________ 。
Ⅰ.制备Na2S2O3·5H2O
方法一:亚硫酸钠法。
反应原理:S+Na2SO3=Na2S2O3
实验步骤:称取一定量的Na2SO3于烧杯中,溶于煮沸过的蒸馏水。另取过量的硫粉,加入少量乙醇充分搅拌均匀后,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶后析出Na2S2O3·5H2O晶体。再进行减压过滤、洗涤并低温干燥。
(1)向硫粉中加入少量乙醇充分搅拌均匀的目的是
(2)下列说法不正确的是 ___________。
| A.蒸发浓缩至溶液表面出现大量沉淀时,停止加热 |
| B.快速冷却,可析出较大晶体颗粒 |
| C.冷却结晶后的固液混合物中加入乙醇可提高产率 |
| D.反应后趁热过滤是除去硫等不溶物 |
方法二:硫化碱法,装置如图。

(3)盛放70%硫酸的仪器名称
(4)装置C中,通入SO2后Na2S和Na2CO3将以2:1的物质的量之比发生反应制得Na2S2O3和CO2反应的化学方程式为
Ⅱ.Na2S2O3的应用
(5)Na2S2O3解毒氰化物原理:S2O
(6)设计以下实验测定粗产品中Na2S2O3·5H2O的含量:
步骤1:准确称取8.00g样品,溶于水,加入5mL甲醛,配成100ml的溶液。
步骤2:准确称取0.294g(0.001mol) K2Cr2O7于碘量瓶中,加入20mL蒸馏水溶解,再加入5mL1mol·L-1 H2SO4和20mL 10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL 1%淀粉,用待测Na2S2O3溶液滴定碘量瓶中溶液至滴定终点,消耗Na2S2O3溶液20.00mL。(已知:I2+2S2O
①出“步骤2”中反应的离子方程式
②试计算Na2S2O3·5H2O的纯度
次磷酸钠(NaH2PO2)是电镀业上重要还原剂,一般制备方法是将白磷(P4)和过量烧碱溶液混合、加热,生成次磷酸钠和PH3,PH3是一种无色、有毒的可燃性气体。实验装置如下图所示:
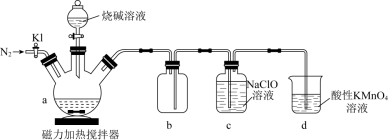
回答下列问题:
(1)盛放烧碱溶液的仪器的名称是______ 。b的作用______ 。次磷酸是______ 元酸。
(2)检查整套装置气密性的方法是______ 。
(3)在a中加入白磷,打开K1,通入N2一段时间,关闭K1,打开磁力加热搅拌器,滴加烧碱溶液,反应结束后,打开K1,继续通入N2,目的是______ 。
(4)c中生成NaH2PO2和NaCl,相关物质溶解度(S)如下:
充分反应后,将c中混合液蒸发浓缩,有大量晶体析出,该晶体主要成分的化学式为______ ,然后______ 、______ 过滤、洗涤、干燥,得到NaH2PO2的粗产品。
(5)产品纯度测定:取NaH2PO2的粗产品2.50克配成250mL溶液,取25.0mL于锥形瓶中,酸化后加入25mL0.10 mol·L-1碘水,于暗处充分反应后,以淀粉溶液做指示剂,用0.10 mol·L-1 Na2S2O3溶液滴定至终点,平均消耗10.0mL Na2S2O3溶液,相关反应方程式为H2PO +H2O+I2=H2PO
+H2O+I2=H2PO +2H++2 I-,2S2O
+2H++2 I-,2S2O +I2=S4O
+I2=S4O +2I-。判断滴定终点的现象是
+2I-。判断滴定终点的现象是______ ,产品纯度为______ (保留3位有效数字)。

回答下列问题:
(1)盛放烧碱溶液的仪器的名称是
(2)检查整套装置气密性的方法是
(3)在a中加入白磷,打开K1,通入N2一段时间,关闭K1,打开磁力加热搅拌器,滴加烧碱溶液,反应结束后,打开K1,继续通入N2,目的是
(4)c中生成NaH2PO2和NaCl,相关物质溶解度(S)如下:
| S(20℃) | S(98℃) | |
| NaCl | 36 | 38.8 |
| NaH2PO2 | 90 | 657 |
(5)产品纯度测定:取NaH2PO2的粗产品2.50克配成250mL溶液,取25.0mL于锥形瓶中,酸化后加入25mL0.10 mol·L-1碘水,于暗处充分反应后,以淀粉溶液做指示剂,用0.10 mol·L-1 Na2S2O3溶液滴定至终点,平均消耗10.0mL Na2S2O3溶液,相关反应方程式为H2PO
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


