解答题-原理综合题 适中0.65 引用3 组卷420
脱除沼气中的H2S具有重要意义,脱除H2S有多种方法。
(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g) =169.8kJ/mol
=169.8kJ/mol
反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g) =63.7kJ/mol
=63.7kJ/mol
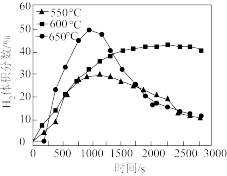
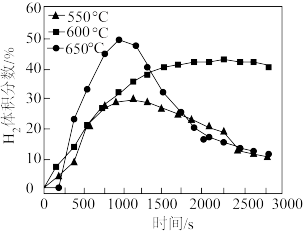
现将硫化氢和甲烷按照2:1体积比投料,并用N2稀释,常压和不同温度下反应,反应相同时间后,H2、S2和CS2体积分数如图所示。 =
=___________ 。
②1050℃时,H2的体积分数为___________ 。
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,其原因可能是___________ 。
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。___________ 。
②与受热分解法相比,光电催化法的优点是___________ 。
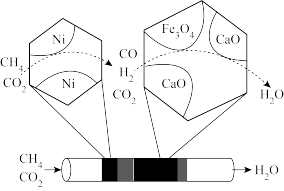
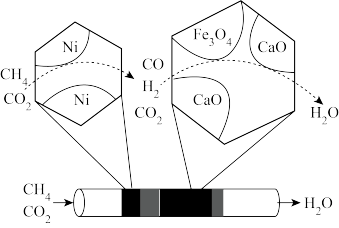
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。___________ 。
②脱除一段时间后,催化剂的活性降低,原因是___________ 。
(1)受热分解法。将H2S和CH4混合气导入热解器,反应分两步进行。
反应Ⅰ:2H2S(g)=2H2(g)+S2(g)
反应Ⅱ:CH4(g)+S2(g)=CS2(g)+2H2(g)
现将硫化氢和甲烷按照2:1体积比投料,并用N2稀释,常压和不同温度下反应,反应相同时间后,H2、S2和CS2体积分数如图所示。

②1050℃时,H2的体积分数为
③在950℃~1150℃范围内,其他条件不变,随着温度的升高,S2(g)的体积分数先增大而后减小,其原因可能是
(2)光电催化法。某光电催化法脱除H2S的原理如图所示。
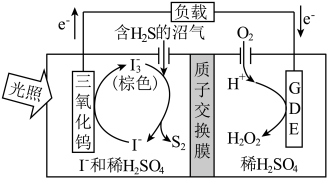
②与受热分解法相比,光电催化法的优点是
(3)催化重整法。Fe2O3可以用作脱除H2S的催化剂,脱除过程如图所示。
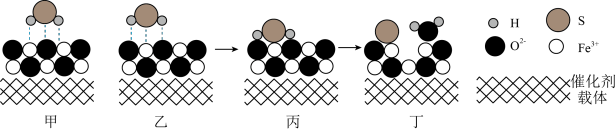
②脱除一段时间后,催化剂的活性降低,原因是
22-23高二·全国·假期作业
类题推荐
主要成分为H2S的工业废气的回收利用有重要意义。
(1)回收单质硫。将三分之一的H2S燃烧,产生的SO2与其余的H2S混合后反应:2H2S(g)+SO2(g)
 S8(g)+2H2O(g) ΔH
S8(g)+2H2O(g) ΔH
已知部分键能数据:H-S:364 kJ·mol-1、S-S:266 kJ·mol-1、S=O:522 kJ·mol-1、H-O:464 kJ·mol-1,则ΔH=__________ 。
(2)热解H2S制H2。根据文献,将H2S和CH4的混合气导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(g) S2(g)+2H2(g) ΔH1=+170 kJ·mol-1
S2(g)+2H2(g) ΔH1=+170 kJ·mol-1
Ⅱ.CH4(g)+ S2(g) CS2(g)+2H2(g) ΔH2=+64 kJ·mol-1
CS2(g)+2H2(g) ΔH2=+64 kJ·mol-1
总反应:
Ⅲ.CH4(g)+ 2H2S(g) CS2(g)+4H2(g)
CS2(g)+4H2(g)
投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释;常压,不同温度下反应相同时间后,测得H2和CS2体积分数如下表:
回答下列问题:
①反应Ⅲ高温下能自发进行的原因是__________ 。
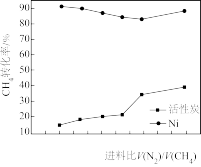
②在1000℃、常压下,保持通入的H2S体积分数不变,提高投料比[V(H2S)∶V(CH4)],H2S的转化率不变,原因是__________ 。
(3)新型的脱硫剂ZnxFeyOz,可脱除煤气中的H2S。
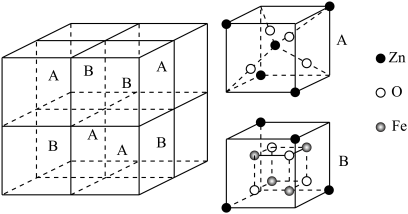
①该脱硫剂晶胞结构如图所示(A、B分别为晶胞的 的结构),其化学式为
的结构),其化学式为__________ 。
②400℃时,将一定比例的H2、CO、CO2和H2S混合气体以一定流速通过该脱硫剂的反应器。
ⅰ.硫化过程中脱硫剂与H2、H2S反应生成ZnS和FeS。
ⅱ.一段时间后,在出口处检测到有COS生成。研究表明ZnS参与了H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该反应过程可描述为__________ 。
(1)回收单质硫。将三分之一的H2S燃烧,产生的SO2与其余的H2S混合后反应:2H2S(g)+SO2(g)
已知部分键能数据:H-S:364 kJ·mol-1、S-S:266 kJ·mol-1、S=O:522 kJ·mol-1、H-O:464 kJ·mol-1,则ΔH=
(2)热解H2S制H2。根据文献,将H2S和CH4的混合气导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(g)
Ⅱ.CH4(g)+ S2(g)
总反应:
Ⅲ.CH4(g)+ 2H2S(g)
投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释;常压,不同温度下反应相同时间后,测得H2和CS2体积分数如下表:
| 温度/℃ | 950 | 1000 | 1050 | 1100 | 1150 |
| H2/V(%) | 0.5 | 1.5 | 3.6 | 5.5 | 8.5 |
| CS2/V(%) | 0.0 | 0.0 | 0.1 | 0.4 | 1.8 |
回答下列问题:
①反应Ⅲ高温下能自发进行的原因是
②在1000℃、常压下,保持通入的H2S体积分数不变,提高投料比[V(H2S)∶V(CH4)],H2S的转化率不变,原因是
(3)新型的脱硫剂ZnxFeyOz,可脱除煤气中的H2S。
①该脱硫剂晶胞结构如图所示(A、B分别为晶胞的

②400℃时,将一定比例的H2、CO、CO2和H2S混合气体以一定流速通过该脱硫剂的反应器。
ⅰ.硫化过程中脱硫剂与H2、H2S反应生成ZnS和FeS。
ⅱ.一段时间后,在出口处检测到有COS生成。研究表明ZnS参与了H2S与CO2生成COS的反应,反应前后ZnS的质量不变,该反应过程可描述为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网