解答题-原理综合题 适中0.65 引用1 组卷60
Ⅰ.工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,反应为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mo1,ΔS=-200J/(mol·K)。请回答下列问题:
2NH3(g) ΔH=-92.4kJ/mo1,ΔS=-200J/(mol·K)。请回答下列问题:
(1)常温下,合成氨反应___________ (填“能”或“不能”)自发进行,其平衡常数表达式K=___________ 。
(2)对于合成氨的反应,下列说法正确的是___________(填序号)。
Ⅱ.在500°C、20MPa时,将N2、H2置于一个容积为2L的恒容密闭容器中发生反应。反应过程中各种物质的物质的量变化如图所示:
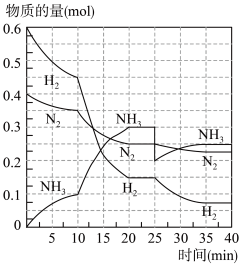
(3)10min内以H2表示的平均反应速率为___________ 。
(4)反应第一次达到平衡时N2的转化率为___________ 。
(5)在反应进行至10min时,曲线发生变化的原因为___________ (填序号,下同);在反应进行至25min时,曲线发生变化的原因为___________ 。
A.加了催化剂 B.降低温度 C.分离了部分NH3
(6)实验室中模拟合成氨过程,将1molN2和2.7molH2置于恒温、体积恒为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是___________ (填序号)。
a.反应不再进行,已经停止
b.单位时间内生成nmolN2的同时,消耗3nmolH2
c.3v正(H2)= 2v逆(NH3)
d. N2、H2和NH3的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变
f.混合气体的密度不再改变
(1)常温下,合成氨反应
(2)对于合成氨的反应,下列说法正确的是___________(填序号)。
| A.该反应在任意条件下都可以自发进行 |
| B.加入催化剂,能提高NH3的产率 |
| C.若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1>K2 |
| D.该反应属于人工固氮 |
Ⅱ.在500°C、20MPa时,将N2、H2置于一个容积为2L的恒容密闭容器中发生反应。反应过程中各种物质的物质的量变化如图所示:

(3)10min内以H2表示的平均反应速率为
(4)反应第一次达到平衡时N2的转化率为
(5)在反应进行至10min时,曲线发生变化的原因为
A.加了催化剂 B.降低温度 C.分离了部分NH3
(6)实验室中模拟合成氨过程,将1molN2和2.7molH2置于恒温、体积恒为2L的容器中反应。下列情况可说明该反应已经达到化学平衡状态的是
a.反应不再进行,已经停止
b.单位时间内生成nmolN2的同时,消耗3nmolH2
c.3v正(H2)= 2v逆(NH3)
d. N2、H2和NH3的物质的量浓度之比为1:3:2
e.混合气体的压强不再改变
f.混合气体的密度不再改变
23-24高二上·云南·阶段练习
类题推荐
工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖,其反应为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
2NH3(g) ΔH=-92.4kJ/mol ΔS=-200J·K-1·mol-1。
回答下列问题:
(1)合成氨反应在常温下___________  填“能”或“不能”
填“能”或“不能” 自发。
自发。
(2)某小组进行工业合成氨N2(g)+3H2(g) 2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。
2NH3(g) ΔH<0的模拟研究,在1 L密闭容器中,分别加入0.1 mol N2和0.3 mol H2。实验①、②、③中c(N2)随时间(t)的变化如图所示。

与实验①相比,实验②所改变的外界条件可能是___________ ,实验③所改变的外界条件可能为 ___________ 。
(3)400℃时,N2(g)+3H2(g) 2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)
2NH3(g) ΔH<0,K1=0.5,则对于反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数K2=
N2(g)+3H2(g)的化学平衡常数K2=___________ ,若某时刻测得NH3、N2和H2物质的量浓度均为1mol•L-1时,则该反应的v正___________ v逆(填“<”、“>”或“=”)。
(4)某小组往一恒温恒压容器中充入9molN2和23molH2模拟合成氨的反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。
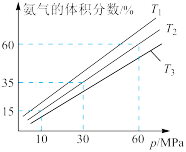
①温度T1、T2、T3中,最大的是___________ 。
②若体系在T2、60MPa下达到平衡如图所示,计算此时N2的平衡转化率为___________ 。
(5)某合成氨速率方程为: ,根据表中数据,
,根据表中数据,
___________ ;
回答下列问题:
(1)合成氨反应在常温下
(2)某小组进行工业合成氨N2(g)+3H2(g)

与实验①相比,实验②所改变的外界条件可能是
(3)400℃时,N2(g)+3H2(g)
(4)某小组往一恒温恒压容器中充入9molN2和23molH2模拟合成氨的反应,如图为不同温度下平衡混合物中氨气的体积分数与总压强(P)的关系图。

①温度T1、T2、T3中,最大的是
②若体系在T2、60MPa下达到平衡如图所示,计算此时N2的平衡转化率为
(5)某合成氨速率方程为:
| 实验 | c(N2)/mol/L | c(H2)/mol/L | c(NH3)/mol/L | v/mol·L-1·s-1 |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
工业合成氨是人类科学技术的一项重大突破。其合成原理为:N2(g)+3H2(g) 2NH3(g)△H<0,△S<0。
2NH3(g)△H<0,△S<0。
(1)下列关于工业合成氨的说法正确的是___ 。
A.因为△H<0,所以该反应一定能自发进行
B.因为△S<0,所以该反应一定不能自发进行
C.在高温下进行是为了提高反应物的转化率
D.生产中在考虑动力和设备材料承受能力的前提下,压强越大转化率越大
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是___ 。
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.N2百分含量保持不变
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)工业上合成氨的部分工艺流程如图:
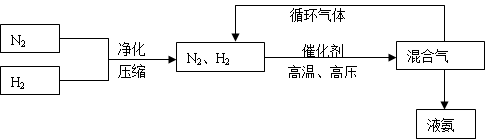
请用平衡移动原理来解释在流程中及时分离出氨气和循环使用气体的原因___ 。
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度)。
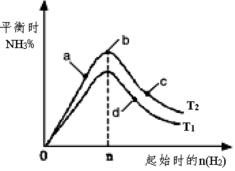
①图象中T2和T1的关系是:T1___ T2(填“>,<或=”,下同)。
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是___ 。(填字母)。
(5)恒温下,往一个4L的密闭容器中充入2molN2和5.2molH2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
①10min时用N2表示的平均反应速率为___ mol/(L·min)-1。此条件下该反应的化学平衡常数K=___ 。
②若维持容器体积不变,温度不变,往原平衡体系中加入N2、H2和NH3各4mol,化学平衡将向反应方向___ 移动(填“正”或“逆”)。
③已知:N2(g)+3H2(g) 2NH3(g)△H=-92kJ/mol
2NH3(g)△H=-92kJ/mol
N2(g)+O2(g)=2NO(g)ΔH=+181kJ/mol
2H2(g)+O2(g)=2H2O(g)ΔH=-484kJ/mol
写出氨气催化氧化生成NO和水蒸气的热化学方程式___ 。
(1)下列关于工业合成氨的说法正确的是
A.因为△H<0,所以该反应一定能自发进行
B.因为△S<0,所以该反应一定不能自发进行
C.在高温下进行是为了提高反应物的转化率
D.生产中在考虑动力和设备材料承受能力的前提下,压强越大转化率越大
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是
A.容器内N2、H2、NH3的浓度之比为1:3:2
B.N2百分含量保持不变
C.容器内压强保持不变
D.混合气体的密度保持不变
(3)工业上合成氨的部分工艺流程如图:

请用平衡移动原理来解释在流程中及时分离出氨气和循环使用气体的原因
(4)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度)。

①图象中T2和T1的关系是:T1
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是
(5)恒温下,往一个4L的密闭容器中充入2molN2和5.2molH2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
①10min时用N2表示的平均反应速率为
②若维持容器体积不变,温度不变,往原平衡体系中加入N2、H2和NH3各4mol,化学平衡将向反应方向
③已知:N2(g)+3H2(g)
N2(g)+O2(g)=2NO(g)ΔH=+181kJ/mol
2H2(g)+O2(g)=2H2O(g)ΔH=-484kJ/mol
写出氨气催化氧化生成NO和水蒸气的热化学方程式
课本里介绍的合成氨技术叫哈伯法,是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g) + 3H2(g) 
 2NH3(g) △H<0,△S <0。
2NH3(g) △H<0,△S <0。
(1)下列关于工业合成氨的说法不正确的是_______
A.因为△H<0,所以该反应一定能自发进行
B.因为△S<0,所以该反应一定不能自发进行
C.在高温下进行是为了提高反应物的转化率
D.使用催化剂加快反应速率是因为催化剂降低了反应的△H
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是_______
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v正(N2)= v逆(H2)
c.容器内压强保持不变 d.合气体的密度保持不变
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示H2物质的量)。
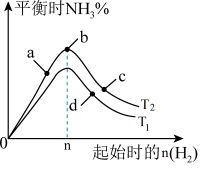
①图象中T2和T1的关系是:T2__________ T1(填“>,<或=”,下同)
②a、b、c、d四点所处的平衡状态中,反应物N2 的转化率最高的是______ (填字母)。
(4)恒温下,往一个4L的密闭容器中充入5.2mol H2和2mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
①此条件下该反应的化学平衡常数K=___________ 。
②若维持容器体积不变,温度不变,往原平衡体系中加入H2、N2和NH3各4mol,化学平衡将向_______ 反应方向移动(填“正”或“逆”)。
③N2(g)+3H2(g) 2NH3(g)△H= -92kJ/mol。在恒温恒容的密闭容器中充入1mol N2和一定量的H2发生反应。达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%,则起始时充入的H2的物质的量为
2NH3(g)△H= -92kJ/mol。在恒温恒容的密闭容器中充入1mol N2和一定量的H2发生反应。达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%,则起始时充入的H2的物质的量为______ mol。
(5)已知:N2(g)+3H2(g) 2NH3(g)△H= -92kJ/mol
2NH3(g)△H= -92kJ/mol
N2(g)+O2(g)=2NO(g) ΔH= +181kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH= -484kJ/mol
写出氨气催化氧化生成NO和水蒸气的热化学方程式_________ 。
(1)下列关于工业合成氨的说法不正确的是
A.因为△H<0,所以该反应一定能自发进行
B.因为△S<0,所以该反应一定不能自发进行
C.在高温下进行是为了提高反应物的转化率
D.使用催化剂加快反应速率是因为催化剂降低了反应的△H
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v正(N2)= v逆(H2)
c.容器内压强保持不变 d.合气体的密度保持不变
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示H2物质的量)。

①图象中T2和T1的关系是:T2
②a、b、c、d四点所处的平衡状态中,反应物N2 的转化率最高的是
(4)恒温下,往一个4L的密闭容器中充入5.2mol H2和2mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
①此条件下该反应的化学平衡常数K=
②若维持容器体积不变,温度不变,往原平衡体系中加入H2、N2和NH3各4mol,化学平衡将向
③N2(g)+3H2(g)
(5)已知:N2(g)+3H2(g)
N2(g)+O2(g)=2NO(g) ΔH= +181kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH= -484kJ/mol
写出氨气催化氧化生成NO和水蒸气的热化学方程式
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


