解答题-工业流程题 适中0.65 引用2 组卷309
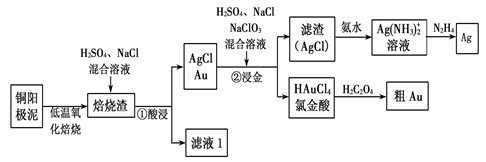
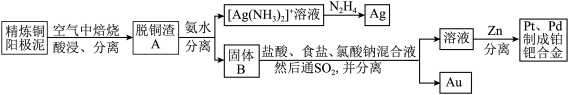
资源的高效利用对保护环境、促进经济持续健康发展具有重要作用,如回收利用电解精炼铜的阳极泥中含有的银、铂、金等贵重金属。提炼阳极泥的方法有多种,湿法提炼是其中重要的一种,其主要生产流程如下:
(1)各步生产流程中都涉及了同一种分离方法,该方法需要的玻璃仪器有玻璃棒和___________ 。
(2)脱铜渣A中含有AgCl,它溶于浓氨水的离子方程式为___________ 。
(3)已知N2H4 被银氨溶液氧化的产物是氮气,则每生成1 mol Ag,需要消耗___________ g N2H4。
(4)固体B中单质Au在酸性环境下与NaClO3、NaCl反应生成NaAuCl4,在NaAuCl4中Au元素的化合价为___________ ,该反应的离子方程式为___________ 。
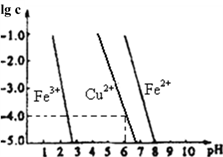
(5)阳极泥中的铜可以用FeCl3 溶液浸出,所得溶液主要含有的阳离子为Cu2+、Fe3+和Fe2+;结合下图分析:(其中的纵坐标代表金属阳离子浓度的对数)___________ (用离子方程式表示),然后加入适量的CuO调节pH=3.7,除去___________ (离子);
②根据图中数据计算可得Cu(OH)2的Ksp约为___________ 。
(1)各步生产流程中都涉及了同一种分离方法,该方法需要的玻璃仪器有玻璃棒和
(2)脱铜渣A中含有AgCl,它溶于浓氨水的离子方程式为
(3)已知N2H4 被银氨溶液氧化的产物是氮气,则每生成1 mol Ag,需要消耗
(4)固体B中单质Au在酸性环境下与NaClO3、NaCl反应生成NaAuCl4,在NaAuCl4中Au元素的化合价为
(5)阳极泥中的铜可以用FeCl3 溶液浸出,所得溶液主要含有的阳离子为Cu2+、Fe3+和Fe2+;结合下图分析:(其中的纵坐标代表金属阳离子浓度的对数)
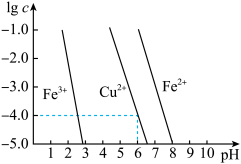
②根据图中数据计算可得Cu(OH)2的Ksp约为
23-24高三上·四川内江·阶段练习
类题推荐
电解精炼铜的阳极泥中含有大量的贵重金属和硒、碲等非金属元素。实验室从电解精炼铜的阳极泥中提取金、银、硒的流程如下:
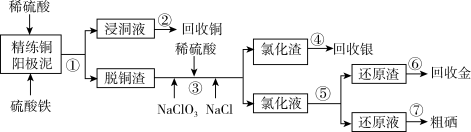
已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原。
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为______ (用化学式表示);加入稀硫酸的目的是____________________ 。
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式___________ ;银元素进入“氯化渣”中,则其存在的形态为_______ (用化学式表示)。
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为______ (填代号)。
若“氯化液”中c(AuCl )为0.01mol·L-1,则处理500mL该“氯化液”需消耗该物质的质量为
)为0.01mol·L-1,则处理500mL该“氯化液”需消耗该物质的质量为_______ g。
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为__________ ;在步骤③中,硒元素被氧化成亚硒酸,则步骤⑦制粗硒的化学反应方程式_____________ 。

已知:单质金在酸性环境下与NaClO3、NaCl反应生成NaAuCl4;NaAuCl4可被Fe2+、SO2还原为单质金;硒的化合物不能被Fe2+还原,而能被SO2还原。
请回答下列问题:
(1)步骤①所得“浸铜液”中铜元素的存在形态为
(2)写出步骤③中金元素进入“氯化液”的离子反应方程式
(3)步骤⑤需在氯化液中加入适当的试剂,可选择的试剂为
| A.FeSO4·7H2O | B.FeCl3 | C.SO2 | D.Na2SO3 |
(4)步骤②可以通过电解的方法得到单质铜,则电解时阴极的电极反应式为
湿法炼锌产生的铜镉渣主要含锌、镉(Cd)、铜、铁、钴(Co)等金属单质。利用铜镉渣可生产Cu、Cd及ZnSO4·7H2O 等,其生产流程如图:
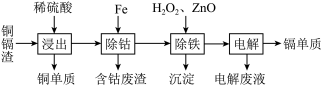
如表是部分金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
请回答下列问题:
(1)提高铜镉渣的“浸出”速率的措施有________________________________ (写出1条即可)。
(2)Fe的金属性比Co强,该流程中“除钴”________ (填“能”或“不能”)用Zn代替Fe,“除钴”中Fe发生反应的离子方程式是__________________________________ 。
(3)“除铁”操作中加入H2O2的目的是______________________________ ,加入ZnO的目的是调节溶液pH,以除去溶液中的铁元素,调节溶液pH的范围为_________ ,“除铁”操作中的沉淀成分是__________ (写化学式)。
(4)“电解”操作中,Cd2+在________ 极放电得到金属Cd,电极反应式是________________________ 。
(5)“电解”后的电解废液是ZnSO4溶液,用该电解废液制备ZnSO4·7H2O的方法是__________________ 。
(6)“除钴”后的含钴废渣在空气中煅烧,煅烧后的成分测定如表:
则煅烧后所得固体混合物中,钴氧化物的化学式是________ 。

如表是部分金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为0.1 mol·L-1计算):
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 | Zn(OH)2 |
开始沉淀的pH | 1.9 | 7.0 | 7.2 | 5.4 |
沉淀完全的pH | 3.2 | 9.0 | 9.5 | 8.2 |
(1)提高铜镉渣的“浸出”速率的措施有
(2)Fe的金属性比Co强,该流程中“除钴”
(3)“除铁”操作中加入H2O2的目的是
(4)“电解”操作中,Cd2+在
(5)“电解”后的电解废液是ZnSO4溶液,用该电解废液制备ZnSO4·7H2O的方法是
(6)“除钴”后的含钴废渣在空气中煅烧,煅烧后的成分测定如表:
元素 | Co | Zn | Cu | Fe |
含量/% | 59.00 | 0.52 | 0.20 | 13.16 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网