解答题-结构与性质 适中0.65 引用1 组卷83
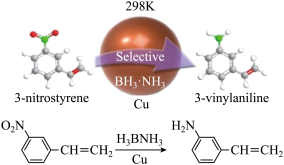
铜纳米催化剂室温催化氨硼烷产氢串联选择性还原催化3-硝基苯乙烯到3-氨基苯乙烯”在有机化学选择性加氢反应研究领域取得重要进展。
请回答下列问题:
(1)下列分别为B、C、N、Cu基态原子价电子排布图,其中正确的是___________(填标号)
(2)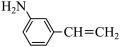 物质的沸点高于
物质的沸点高于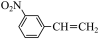 ,原因是
,原因是___________ ,硝基(-NO2)和氨基(-NH2)中N的杂化方式分别为___________ 。
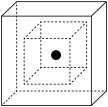
(3)SiC结构类似金刚石,则SiC为_____ 晶体。图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用●表示),其余Si原子位于大正方体的_______ 位置。
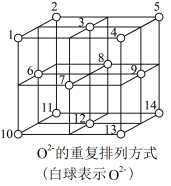
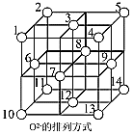
(4)科学研究表明,Fe3O4是由Fe2+、Fe3+、O2-通过离子键而组成的复杂离子晶体。Fe3+比Fe2+稳定性更好,原因是_________ 。O2-的重复排列方式如图所示,晶胞中O2-个数为_________ ,Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,有______ %正四面体空隙填有Fe3+。

请回答下列问题:
(1)下列分别为B、C、N、Cu基态原子价电子排布图,其中正确的是___________(填标号)
A.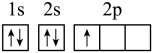 | B.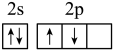 |
C.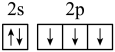 | D.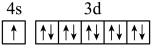 |
(2)
 物质的沸点高于
物质的沸点高于 ,原因是
,原因是(3)SiC结构类似金刚石,则SiC为

(4)科学研究表明,Fe3O4是由Fe2+、Fe3+、O2-通过离子键而组成的复杂离子晶体。Fe3+比Fe2+稳定性更好,原因是

23-24高三上·宁夏银川·阶段练习
类题推荐
近日,哈尔滨工业大学于永生教授研究成果以“铜纳米催化剂室温催化氨硼烷产氢串联选择性还原催化3一硝基苯乙烯到3-氨基苯乙烯”为题以封面文章发表在国际期刊《美国化学学会杂志》(JACS)上,在有机化学选择性加氢反应研究领域取得重要进展。
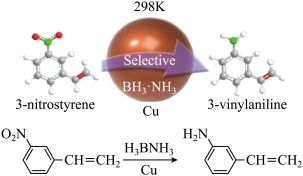
请回答下列问题:
(1)下列分别为B、C、N、Cu基态原子价电子排布图,其中正确的是__ (填标号)
A.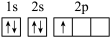
B.
C.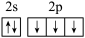
D.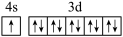
(2)按IUPAC规定H为元素周期表第1列,He位于元素周期表第18列,则Cu位于元素周期表第____ 列。
(3)氨硼烷(H3BNH3)中B和N均位于第二周期,但r(B)大于r(N),原因是___ 。
(4)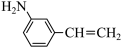 物质的沸点高于
物质的沸点高于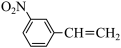 ,原因是
,原因是____ ,硝基(-NO2)和氨基(-NH2)中N的杂化方式分别为 ___ 。
(5)元素的基态气态原子得到一个电子形成气态 -1价离子时所放出的能量称为第一电子亲和能(E1),-1价阴离子再获得一个电子的能量变化称为第二电子亲和能(E2),氧原子或离子的电子亲和能数据如下表所示。
下列说法正确的是____ 。
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O-时放出14lkJ的能量
C.氧元素的第二电子亲和能是 - 780kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
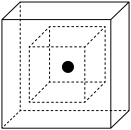
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,则SiC 为____ 晶体。上图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用●表示),试在小立方体的顶点画出C原子(用○表示)的位置,在大正方体画出相应Si原子的位置_________ 。

请回答下列问题:
(1)下列分别为B、C、N、Cu基态原子价电子排布图,其中正确的是
A.

B.

C.

D.

(2)按IUPAC规定H为元素周期表第1列,He位于元素周期表第18列,则Cu位于元素周期表第
(3)氨硼烷(H3BNH3)中B和N均位于第二周期,但r(B)大于r(N),原因是
(4)
 物质的沸点高于
物质的沸点高于 ,原因是
,原因是(5)元素的基态气态原子得到一个电子形成气态 -1价离子时所放出的能量称为第一电子亲和能(E1),-1价阴离子再获得一个电子的能量变化称为第二电子亲和能(E2),氧原子或离子的电子亲和能数据如下表所示。
元素 | O | O- |
电子亲和能(kJ/mol) | 141 | -780 |
下列说法正确的是
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O-时放出14lkJ的能量
C.氧元素的第二电子亲和能是 - 780kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量

(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,则SiC 为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
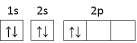 ,该表示式违背了
,该表示式违背了
 )检验Fe3+。
)检验Fe3+。


