单选题 适中0.65 引用2 组卷150
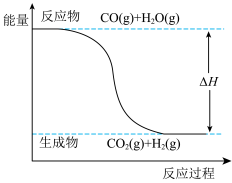
水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g) ΔH]是重要的化工过程,反应过程中的能量变化如下图所示。
②H2O(g)=H2O(l) ΔH=-44kJ/mol
下列叙述错误的是
| 化学键 | H-H | H-O | C=O | C≡O |
| E/(kJ·mol-1) | 436 | 465 | 805 | 1076 |
下列叙述错误的是
| A.反应使用催化剂时,不会改变其ΔH |
| B.CO中化学键的键能为1076kJ/mol |
| C.水煤气变换反应的ΔH=-40kJ/mol |
| D.若H2O的状态为液态,则该反应仍为放热反应 |
23-24高三上·重庆·阶段练习
类题推荐
反应热计算是一种基本化学能力。
(1)已知相关的化学键键能数据如下:
CO(g)+2H2(g)  CH3OH(g) ΔH=
CH3OH(g) ΔH=_______ kJ·mol-1
(2)水煤气变换反应CO(g)+H2O(g) CO2 (g)+H2(g) ΔH<0 (简称WGS),在金属催化剂Au(III)表面上发生的所有基元反应步骤的活化能数值(单位: kJ/mol)如下表,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。
CO2 (g)+H2(g) ΔH<0 (简称WGS),在金属催化剂Au(III)表面上发生的所有基元反应步骤的活化能数值(单位: kJ/mol)如下表,其中*表示催化剂表面活性位,X*表示金属表面活性位吸附物种。
由表中数据计算WGS反应的焓变ΔH=___________ kJ/mol。
(3)已知: N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol
N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol
H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
则反应4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH=_______ kJ/mol
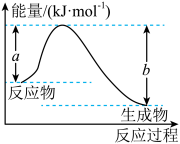
(4)已知下列物质的相对能量如图,则C2H6(g)+2CO2(g)=4CO(g)+3H2(g) ΔH=___ kJ/mol

(1)已知相关的化学键键能数据如下:
| 化学键 | H-H | C-O | H-O | C-H | |
| E/( | 436 | 343 | 1076 | 465 | 413 |
(2)水煤气变换反应CO(g)+H2O(g)
基元反应 | 正逆反应活化能 | ||
| E正反应 | E逆反应 | ||
| ① | H2O+* | 0 | 67 |
| ② | H2O*+* | 150 | 0 |
| ③ | OH*+* | 71 | 67 |
| ④ | 2H*+* | 74 | 25 |
| ⑤ | CO+* | 0 | 42 |
| ⑥ | CO*+O* | 37 | 203 |
| ⑦ | CO2* | 17 | 0 |
(3)已知: N2(g)+O2(g)=2NO(g) ΔH=+180.0 kJ/mol
N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ/mol
H2O(l)=H2O(g) ΔH=+44.0 kJ/mol
则反应4NH3(g)+5O2(g)=4NO(g)+6H2O(l) ΔH=
(4)已知下列物质的相对能量如图,则C2H6(g)+2CO2(g)=4CO(g)+3H2(g) ΔH=

工业上常利用合理的催化剂,将含碳氧化物转化为重要的化工原料一甲醇,由CO、CO2和H2合成甲醇发生的主要反应如下:
I.CO(g)+2H2(g)⇌CH3OH(g) ΔH1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-58kJ/mol
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=41kJ/mol
回答下列问题:
已知反应I中相关的化学键键能数据如下表:
则x=_______ 。
I.CO(g)+2H2(g)⇌CH3OH(g) ΔH1
II.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-58kJ/mol
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=41kJ/mol
回答下列问题:
已知反应I中相关的化学键键能数据如下表:
| 化学键 | H—H | C—O | C | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | x |
则x=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
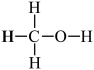 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)

