填空题 适中0.65 引用1 组卷172
按要求回答下列问题:
(1)已知Na2O2可用于呼吸面具供氧,请用化学方程式解释:___________ 。
(2)已知制备Fe(OH)2时,白色沉淀会迅速变为灰绿色,最终变为红褐色,请用化学方程式解释这一变化结果:___________ 。
(3)家庭中常用消毒液(主要成分NaClO、NaCl)与洁厕灵(主要成分盐酸)清洁卫生。两者同时使用容易产生氯气引起中毒,写出反应的离子方程式___________ 。
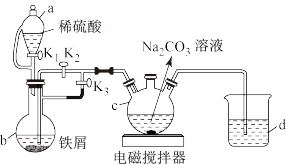
(4)已知燃煤烟气的主要成分为N2、CO、SO2,如图装置可以测SO2的体积分数,已知A的目的是观察气流速度,则B中发生反应的离子方程式:___________ 。

(5)已知亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,通过下面实验过程可以得到该产品,写出反应②的离子方程式:___________ 。

(1)已知Na2O2可用于呼吸面具供氧,请用化学方程式解释:
(2)已知制备Fe(OH)2时,白色沉淀会迅速变为灰绿色,最终变为红褐色,请用化学方程式解释这一变化结果:
(3)家庭中常用消毒液(主要成分NaClO、NaCl)与洁厕灵(主要成分盐酸)清洁卫生。两者同时使用容易产生氯气引起中毒,写出反应的离子方程式
(4)已知燃煤烟气的主要成分为N2、CO、SO2,如图装置可以测SO2的体积分数,已知A的目的是观察气流速度,则B中发生反应的离子方程式:

(5)已知亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,通过下面实验过程可以得到该产品,写出反应②的离子方程式:

21-22高一上·广东深圳·期末
类题推荐
I.据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。
(1)84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸钠的电子式:__________ ;若将84消毒液长期露置于空气中,溶液中的主要成分将变为__________ (填化学式)。
(2)洁厕灵的主要成分是HCl。洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式:______________________________ 。
(3)下列氧化还原反应中,与上述反应类型不同的是________。
II.已知高锰酸钾(硫酸酸化)溶液和草酸(H2C2O4)溶液可以发生氧化还原反应。请回答下列问题:
(4)该反应中的还原剂是________ (填化学式)。
(5)写出该反应的离子方程式:____________________ 。
(6)若生成1molCO2则转移电子_______ mol
(1)84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸钠的电子式:
(2)洁厕灵的主要成分是HCl。洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式:
(3)下列氧化还原反应中,与上述反应类型不同的是________。
| A.Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O | B.2FeCl3+Fe=3FeCl2 |
| C.S+2H2SO4(浓) | D.KClO3+5KCl+3H2SO4=3K2SO4+3Cl2↑+3H2O |
II.已知高锰酸钾(硫酸酸化)溶液和草酸(H2C2O4)溶液可以发生氧化还原反应。请回答下列问题:
(4)该反应中的还原剂是
(5)写出该反应的离子方程式:
(6)若生成1molCO2则转移电子
工业上用 和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
和碱制漂白粉、漂粉精及漂白液。请回答下列问题:
(1) Ca(ClO)2中Cl元素的化合价是___________ ;工业上将氯气制成漂白粉的主要目的是___________ 。工业上制成漂白粉的化学方程式:___________ 。
(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是___________(填字母)。
(3)浸泡衣物时加入漂粉精(有效成分Ca(ClO)2)在空气中放置一段时间漂白效果更好,请用化学方程式解释原因:___________ 。
(4)若将漂白液(有效成分NaClO)与洁厕灵(主要成分是盐酸)混合使用,则会产生有毒气体,其反应的离子方程式是___________ 。
(5)有效氯是漂白粉中有效成分Ca(ClO)2含量大小的标志。
已知:①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
② 。
。
若某漂粉精的有效氯为60%,该漂粉精中Ca(ClO)2的质量分数为___________ (计算结果保留一位小数)。
(1) Ca(ClO)2中Cl元素的化合价是
(2)下列物质露置在空气中会变质,在变质过程中既有非氧化还原反应发生,又有氧化还原反应发生的是___________(填字母)。
| A.生石灰 | B.漂白粉 |
| C.NaOH | D. |
(4)若将漂白液(有效成分NaClO)与洁厕灵(主要成分是盐酸)混合使用,则会产生有毒气体,其反应的离子方程式是
(5)有效氯是漂白粉中有效成分Ca(ClO)2含量大小的标志。
已知:①Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O;
②
若某漂粉精的有效氯为60%,该漂粉精中Ca(ClO)2的质量分数为
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网