解答题-实验探究题 较难0.4 引用1 组卷157
某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被OH-还原为
可被OH-还原为 。
。
iii.Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
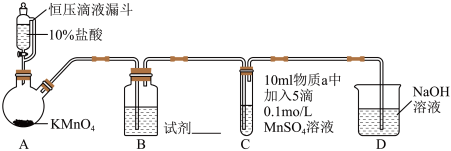
(1)实验室中利用MnO2和浓盐酸加热的反应来制取氯气,对比本实验A中的反应,说明氧化性MnO2_______ KMnO4(填“>”或“<”)。
(2)B中试剂是_______ 。(填序号)
①浓硫酸 ②饱和食盐水
(3)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色[Mn(OH)2]变为棕黑色,补全发生反应的化学方程式:___________ 。
Mn(OH)2+_______=________+H2O
(4)对比实验I、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是:
①__________ ;
②在碱性条件下可以被氧化到更高价态。
(5)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因___________ ,但通过实验测定,溶液的碱性变化很小。
②针对原因二小组同学做如下探究:
Ⅳ中溶液紫色迅速变为绿色的离子方程式为_________ 。
 +OH-=
+OH-= +___________+___________。
+___________+___________。
资料:i.Mn2+在一定条件下被Cl2或ClO-氧化成MnO2(棕黑色)、
ii.浓碱条件下,
iii.Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)

| 序号 | I | Ⅱ | Ⅲ |
| 物质a | 水 | 5%NaOH溶液 | 40%NaOH溶液 |
| 通入Cl2前 C中实验现象 | 得到无色溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 |
| 通入Cl2后 C中实验现象 | 产生棕黑色沉淀,且放置后不发生变化 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)实验室中利用MnO2和浓盐酸加热的反应来制取氯气,对比本实验A中的反应,说明氧化性MnO2
(2)B中试剂是
①浓硫酸 ②饱和食盐水
(3)通入Cl2前,Ⅱ、Ⅲ中沉淀由白色[Mn(OH)2]变为棕黑色,补全发生反应的化学方程式:
Mn(OH)2+_______=________+H2O
(4)对比实验I、Ⅱ通入Cl2后的实验现象,对于二价锰化合物还原性的认识是:
①
②在碱性条件下可以被氧化到更高价态。
(5)根据资料ii,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入Cl2导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将
①用化学方程式表示可能导致溶液碱性减弱的原因
②针对原因二小组同学做如下探究:
| 序号 | Ⅳ | Ⅴ |
| 操作 | 取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液 | 取Ⅲ中放置后的1mL悬浊液,加入4mL水, |
| 现象 | 溶液紫色迅速变为绿色,且绿色缓慢加深 | 溶液紫色缓慢加深 |
23-24高一上·北京·期中
类题推荐
某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:
ⅰ. 在一定条件下被
在一定条件下被  或
或 氧化成
氧化成  (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ⅱ.浓碱条件下, 可被
可被  还原为
还原为  。
。
ⅲ. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
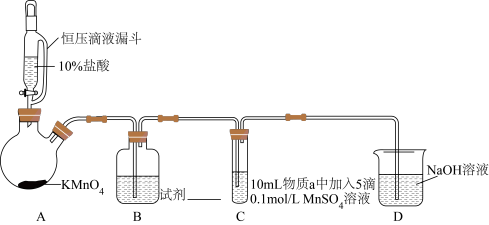
(1) 装置中制备
装置中制备  的化学反应方程式是
的化学反应方程式是__________ 。
(2) 中试剂是
中试剂是__________ 。
(3)通入 前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为
前,Ⅱ、Ⅲ中沉淀由白色变为黑色的化学方程式为__________ 。
(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为  。
。
①化学方程式表示可能导致溶液碱性减弱的原因__________ ,但通过实验测定溶液的碱性变化很小。
②取Ⅲ中放置后的 悬浊液,加入
悬浊液,加入  溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为
溶液,溶液紫色迅速变为绿色,且绿色缓慢加深。溶液紫色变为绿色的离子方程式为__________ ,溶液绿色缓慢加深,原因是  被
被__________ (填化学式)氧化,可证明Ⅲ的悬浊液中氧化剂过量;
③取Ⅱ中放置后的 悬浊液,加入
悬浊液,加入  水,溶液紫色缓慢加深,发生的反应是
水,溶液紫色缓慢加深,发生的反应是__________ 。
资料:
ⅰ.
ⅱ.浓碱条件下,
ⅲ.
实验装置如图(夹持装置略)

序号 | 物质 | C中实验现象 | |
通入 | 通入 | ||
Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
Ⅱ |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
Ⅲ |
| 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)
(2)
(3)通入
(4)根据资料ⅱ,Ⅲ中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符原因:
原因一:可能是通入
原因二:可能是氧化剂过量,氧化剂将
①化学方程式表示可能导致溶液碱性减弱的原因
②取Ⅲ中放置后的
③取Ⅱ中放置后的
某小组同学探究不同条件下 与
与 的反应产物,设计的实验装置如图所示(夹持装置已省略)。
的反应产物,设计的实验装置如图所示(夹持装置已省略)。

已知:Ⅰ. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
Ⅱ.浓碱条件下, 可与
可与 反应生成
反应生成 和
和 。
。
Ⅲ. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
回答下列问题:
(1)仪器m的名称为___________ 。
(2)装置A中发生反应的化学方程式为___________ 。
(3)装置B中盛放的试剂为___________ 。
(4)装置D的作用为___________ 。
(5)根据表格推断,通入 前,实验Ⅱ、Ⅲ中产生的白色沉淀为
前,实验Ⅱ、Ⅲ中产生的白色沉淀为___________ (填化学式)。
(6)对比实验Ⅰ、Ⅱ通入 后的实验现象,在碱性条件下
后的实验现象,在碱性条件下___________ 能被 氧化为
氧化为___________ 。
(7)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,但实验中得到紫色溶液,分析现象与资料不符的原因。
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:___________ 。
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,紫色溶液迅速变为绿色,且绿色缓慢加深。溶液由紫色变为绿色的离子方程式为___________ ,溶液绿色缓慢加深,原因是 被
被___________ (填“化学式”)氧化,可证明Ⅲ的悬浊液中氧化剂过量。

已知:Ⅰ.
Ⅱ.浓碱条件下,
Ⅲ.
| 实验 | 物质a | 装置C中实验现象 | |
| 通入 | 通入 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,但仍有棕黑色沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,但仍有棕黑色沉淀 |
(1)仪器m的名称为
(2)装置A中发生反应的化学方程式为
(3)装置B中盛放的试剂为
(4)装置D的作用为
(5)根据表格推断,通入
(6)对比实验Ⅰ、Ⅱ通入
(7)根据资料ⅱ,实验Ⅲ中应得到绿色溶液,但实验中得到紫色溶液,分析现象与资料不符的原因。
原因一:可能是通入
原因二:可能是氧化剂过量,氧化剂将
①用化学方程式表示可能导致溶液碱性减弱的原因:
②取Ⅲ中放置后的1mL悬浊液,加入4mL40%NaOH溶液,紫色溶液迅速变为绿色,且绿色缓慢加深。溶液由紫色变为绿色的离子方程式为
某小组同学探究不同条件下氯气与二价锰化合物的反应。查阅资料显示:
a. 在一定条件下能被
在一定条件下能被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
b.浓碱条件下, 可被
可被 还原为
还原为 。
。
c. 的氧化性与溶液的酸碱性无关,
的氧化性与溶液的酸碱性无关, 的氧化性随碱性增强而减弱。
的氧化性随碱性增强而减弱。
d. 为白色沉淀。
为白色沉淀。
实验装置如图(夹持装置略)
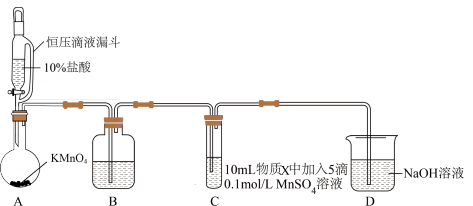
(1)A中发生的反应的化学方程式如下: 。用双线桥标出该反应中电子转移的方向和数目
。用双线桥标出该反应中电子转移的方向和数目________ 。
(2)通入 前,Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为
前,Ⅱ、Ⅲ中沉淀由白色变为棕黑色的化学方程式为_______ 。
(3)对比实验Ⅰ、Ⅱ通入 后的实验现象,对于
后的实验现象,对于 还原性与溶液酸碱性的认识是
还原性与溶液酸碱性的认识是_______ 。
(4)根据资料b,Ⅲ中应得到绿色溶液,而实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因:_______ 。
②取Ⅲ中放置后的 悬浊液,加入
悬浊液,加入 溶液,观察到溶液紫色迅速变为绿色,且有无色无味的气体产生,该气体的化学式为
溶液,观察到溶液紫色迅速变为绿色,且有无色无味的气体产生,该气体的化学式为_______ 。同时还可观察到溶液的绿色缓慢加深,即可证明Ⅲ的悬浊液中氧化剂过量。
③从化学反应进行的快慢的角度,分析实验Ⅲ未得到绿色溶液的可能原因:_______ 。
a.
b.浓碱条件下,
c.
d.
实验装置如图(夹持装置略)

| 序号 | 物质X | C中实验现象 | |
| 通入 | 通入 | ||
| Ⅰ | 水 | 得到无色溶液 | 产生棕黑色沉淀,且放置后不发生变化 |
| Ⅱ | 5%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
| Ⅲ | 40%NaOH溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(2)通入
(3)对比实验Ⅰ、Ⅱ通入
(4)根据资料b,Ⅲ中应得到绿色溶液,而实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
原因二:可能是氧化剂过量,氧化剂将
①用化学方程式表示可能导致溶液碱性减弱的原因:
②取Ⅲ中放置后的
③从化学反应进行的快慢的角度,分析实验Ⅲ未得到绿色溶液的可能原因:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


