填空题 适中0.65 引用1 组卷36
溶液体系是化学反应的重要场所,也是高中化学重要的研究对象,物质在水溶液中有多种行为,请用化学用语解释下列行为
(1)25℃时,测得0.1mol/L NH3·H2O溶液的pH=11,由此确定NH3·H2O是弱电解质,NH3·H2O在水溶液中的电离方程式为:___________ 。
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液pH=6,则溶液中存在的电荷关系为:c(CH3COO-)-c(Na+)=___________ (填计算式)。
(3)向沸水中逐滴滴加饱和FeCl3溶液,制备Fe(OH)3胶体,原理为:___________ 。
(4)磁化铝(Al2S3)等盐在水中不能存在,也不能通过水溶液中的离子反应来制取,原因是:___________ 。
(5)当向白色ZnS沉淀上滴加CuSO4溶液时,反应生成黑色的CuS沉淀,这种转化可表示为:___________ 。
(1)25℃时,测得0.1mol/L NH3·H2O溶液的pH=11,由此确定NH3·H2O是弱电解质,NH3·H2O在水溶液中的电离方程式为:
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液pH=6,则溶液中存在的电荷关系为:c(CH3COO-)-c(Na+)=
(3)向沸水中逐滴滴加饱和FeCl3溶液,制备Fe(OH)3胶体,原理为:
(4)磁化铝(Al2S3)等盐在水中不能存在,也不能通过水溶液中的离子反应来制取,原因是:
(5)当向白色ZnS沉淀上滴加CuSO4溶液时,反应生成黑色的CuS沉淀,这种转化可表示为:
21-22高二上·北京海淀·期中
类题推荐
研究电解质在水溶液中的行为有重要的意义(以下均为25℃)。
I.有0.1 mol·L 的三种溶液:a.NaOH b.
的三种溶液:a.NaOH b. c.盐酸
c.盐酸
(1)溶液a的
_______ ;c中水电离出的
_______ 。
(2)溶液b的 ,用化学用语解释原因
,用化学用语解释原因_______ 。
(3) L溶液a与
L溶液a与 L溶液c混合后,若所得溶液的
L溶液c混合后,若所得溶液的 ,则
,则
_______ 。
(4)向20 mL溶液b中滴加溶液a的过程中,pH变化如图所示。
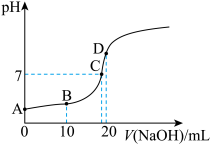
①滴加过程中发生反应的离子方程式是_______ 。
②B点溶液中,离子浓度由大到小的顺序为_______ 。
③D点溶液中,
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
II. 、
、 、HClO和
、HClO和 的电离平衡常数如下:
的电离平衡常数如下:
(5)0.1 mol·L 的下列四种溶液,pH由小到大的顺序是_______(填字母)。
的下列四种溶液,pH由小到大的顺序是_______(填字母)。
(6)0.1 mol·L
 的溶液中
的溶液中 ,结合化学用语解释原因:
,结合化学用语解释原因:_______ 。
(7)向NaClO溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(8)向NaClO溶液中分别加入下列物质,能增大 的是
的是_______ (填字母)。
A. B.
B. C.
C.
I.有0.1 mol·L
(1)溶液a的
(2)溶液b的
(3)
(4)向20 mL溶液b中滴加溶液a的过程中,pH变化如图所示。

①滴加过程中发生反应的离子方程式是
②B点溶液中,离子浓度由大到小的顺序为
③D点溶液中,
II.
| 化学式 | HClO | |||
| 电离平衡常数( |
| A. | B. | C.NaClO | D. |
(7)向NaClO溶液中通入少量
(8)向NaClO溶液中分别加入下列物质,能增大
A.
平衡思想是化学研究的一个重要观念,电解质水溶液中存在电离平衡、水解平衡、溶解平衡。常温下,向1 L 0.1 mol/L H2A溶液中逐滴加入等浓度NaOH溶液,所得溶液中含A元素的微粒的物质的量分数与溶液pH的关系如图:

(1)在0.1mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是___________;
(2)已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能是___________ 0.11mol·L-1(填“<”“>”或“=”),理由是___________ 。
(3)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,若混合后溶液的pH=7,用含的代数式表示NH3·H2O的电离常数Kb=___________ 。

(1)在0.1mol·L-1的Na2A溶液中,下列粒子浓度关系式正确的是___________;
| A.c(A2–)+c(HA–)+c(H2A)=0.1mol·L-1 |
| B.c(Na+)>c(A2–)>c(HA–)>c(OH–)>c(H+) |
| C.c(Na+)+c(H+)=c(OH–)+c(HA–)+2c(A2–) |
| D.c(Na+)=2c(A2–)+2c(HA–) |
(2)已知0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能是
(3)25℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,若混合后溶液的pH=7,用含的代数式表示NH3·H2O的电离常数Kb=
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


