解答题-结构与性质 适中0.65 引用1 组卷78
现有六种元素A、B、C、D、E、F,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的轨道表示式为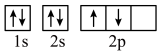 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(2)B元素的电负性___________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物的晶体类型为___________ 。
(4)E基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向。
(5)下列关于F原子的价电子轨道表示式是___________ 。
(6)基态Fe3+核外电子排布式为___________ 。过量单质F与B的最高价氧化物对应的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素是地壳中含量最多的元素 |
| D元素原子的第一至第四电离能分别是:I1=738 kJ·mol-1;I2=1451 kJ·mol-1;I3=7733kJ·mol-1;I4=10540 kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
(1)某同学根据上述信息,推断A基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)B元素的电负性
(3)C与D形成的化合物的晶体类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)下列关于F原子的价电子轨道表示式是
(6)基态Fe3+核外电子排布式为
23-24高二上·江西宜春·期中
类题推荐
现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_______ 。(填“泡利原理”“洪特规则”或“能量最低原理”)
(2)B元素的电负性_______ (填“大于”“小于”或“等于”)C元素的电负性。
(3)E基态原子中能量最高的电子,其电子云在空间有_______ 个伸展方向。
(4)下列关于F原子的价层电子轨道表示式正确的是_______(填字母)。
(5)基态D原子的核外电子排布式为_______ 。
(6)F3+比F2+化学性质更稳定,请从原子结构的角度解释其原因:_______ 。
| A元素形成的物质种类繁多,其形成的一种固体单质是自然界最硬的物质 |
| B元素原子的核外p轨道总电子数比s轨道总电子数少1 |
| C元素与B元素同周期,其基态原子p轨道有两个未成对电子 |
| D元素原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E元素原子核外所有p轨道全满或半满 |
| F元素在周期表的第8纵列,其单质是生活中使用最广泛的金属 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)E基态原子中能量最高的电子,其电子云在空间有
(4)下列关于F原子的价层电子轨道表示式正确的是_______(填字母)。
A. | B.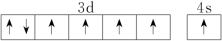 |
C. | D.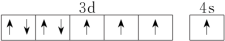 |
(6)F3+比F2+化学性质更稳定,请从原子结构的角度解释其原因:
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第4周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)B基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(2)某同学根据上述信息,推断C基态原子的轨道表示式为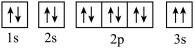 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(3)G位于___________ 族___________ 区,价电子排布为___________ 。
(4)检验F元素的方法是___________ ,请用原子结构的知识解释产生此现象的原因:________________ 。
(5)写出E的单质与水反应的离子方程式:___________ 。
| 元素 | 相关信息 |
| A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 原子的第一至第四电离能分别是I1=738 kJ·mol-1;I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
| D | 原子核外所有p轨道全充满或半充满 |
| E | 元素的主族序数与周期数的差为4 |
| F | 是前四周期中电负性最小的元素 |
| G | 在周期表的第七列 |
(1)B基态原子中能量最高的电子,其电子云在空间有
(2)某同学根据上述信息,推断C基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(3)G位于
(4)检验F元素的方法是
(5)写出E的单质与水反应的离子方程式:
现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的核外电子排布为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了_____ 。
(2)B元素的电负性_____ (填“大于”“小于”或“等于”)C元素的电负性。
(3)下列关于F原子的价层电子轨道表示式正确的是_____ (填字母)。
(4)基态F3+的核外电子排布式为______ 。
(5)元素铜与镍的第二电离能分别为ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是______ 。
(6)B原子核外有______ 种不同运动状态的电子。基态B原子中,能量最高的电子所占据的原子轨道的形状为_____ 。
(7)As的卤化物的熔点如表:
表中卤化物熔点差异的原因是______ 。
(8)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是______ ,Fe3+的配位数为______ 。

| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素基态原子p轨道有两个未成对电子 |
| D原子的第一至第四电离能分别是:I1=738kJ·mol-1;I2=1451kJ·mol-1;I3=7733kJ·mol-1;I4=10540kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(2)B元素的电负性
(3)下列关于F原子的价层电子轨道表示式正确的是
A.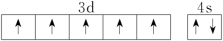 | B.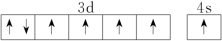 |
C. | D.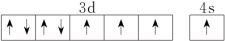 |
(5)元素铜与镍的第二电离能分别为ICu=1959kJ·mol-1,INi=1753kJ·mol-1,ICu>INi原因是
(6)B原子核外有
(7)As的卤化物的熔点如表:
| 物质 | AsCl3 | AsBr3 | AsI3 |
| 熔点/K | 256.8 | 304 | 413 |
(8)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


