单选题 适中0.65 引用1 组卷88
已知反应:①CH4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH1=-akJ/mol(a>0);
②C2H4(g)+2O2(g)=2CO(g)+2H2O(l) ΔH2=-bkJ/mol(b>0)。
其他数据如表所示:
下列说法正确的是
②C2H4(g)+2O2(g)=2CO(g)+2H2O(l) ΔH2=-bkJ/mol(b>0)。
其他数据如表所示:
| 化学键 | C=O | O=O | C-H | O-H | C=C |
| 键能/(kJ·mol-1) | 798 | x | 413 | 463 | 615 |
| A.乙烯的燃烧热为akJ/mol |
| B.上表中的x用a的代数式表示为 |
| C.反应2CO(g)+O2(g)=2CO2(g) ΔH=-(a-b)kJ/mol |
| D.若有C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) ΔH3=-ckJ/mol(c>0),则有ΔH3>ΔH1 |
23-24高三上·江西宜春·阶段练习
类题推荐
下列说法正确的是
| A.P(s,白磷)=P(s,红磷)ΔH=-176 kJ· mol-1,由此推之白磷比红磷稳定 |
| B.在“中和反应的反应热测定”实验中,改变酸的种类实验结果不变 |
| C.已知2C(s)+O2(g)=2CO(g) ΔH1;2C(s)+2O2(g)=2CO2(g) ΔH2,则ΔH1>ΔH2 |
| D.乙烯燃烧的热化学方程式为:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH < 0,由此推之C2H4的能量高于CO2的能量 |
回答下列问题。
(1)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1
反应Ⅱ:N2(g)+O2(g) 2NO(g) ΔH2=b kJ·mol-1
2NO(g) ΔH2=b kJ·mol-1
反应Ⅲ:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1
则反应Ⅱ中的b=___________ (用含a、c的代数式表示),反应Ⅲ中的ΔS___________ (填“>”“<”或“=”)0。
(2)已知:①2CO(g)+SO2(g) S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
S(l)+2CO2(g) ΔH1=-37.0 kJ·mol-1
②2H2(g)+SO2(g) S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
S(l)+2H2O(g) ΔH2=+45.4 kJ·mol-1
③CO的燃烧热ΔH3=-283 kJ·mol-1,
请回答:
表示液态硫(S)的燃烧热的热化学方程式为___________ ;反应②中,正反应活化能E1___________ (填“>”“<”或“=”)ΔH2。
(3)若某温度下,CH3COOH(aq)与NaOH(aq)反应的ΔH=-46.8 kJ·mol-1,H2SO4(aq)与NaOH(aq)的中和热为57.3 kJ·mol-1,则CH3COOH在水溶液中电离的反应热ΔH1=___________ 。
(4)已知:
则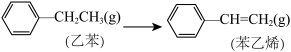 +H2(g) ΔH=
+H2(g) ΔH=___________ ;又知H2和苯乙烯的燃烧热ΔH分别为-290 kJ·mol-1和-4400 kJ·mol-1,则乙苯的燃烧热ΔH=___________ kJ·mol-1。
(1)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g)
反应Ⅱ:N2(g)+O2(g)
反应Ⅲ:4NH3(g)+6NO(g)
则反应Ⅱ中的b=
(2)已知:①2CO(g)+SO2(g)
②2H2(g)+SO2(g)
③CO的燃烧热ΔH3=-283 kJ·mol-1,
请回答:
表示液态硫(S)的燃烧热的热化学方程式为
(3)若某温度下,CH3COOH(aq)与NaOH(aq)反应的ΔH=-46.8 kJ·mol-1,H2SO4(aq)与NaOH(aq)的中和热为57.3 kJ·mol-1,则CH3COOH在水溶液中电离的反应热ΔH1=
(4)已知:
| 化学键 | C—H | C—C | C=C | H—H |
| 键能/(kJ·mol-1) | 412 | 348 | 612 | 436 |
 +H2(g) ΔH=
+H2(g) ΔH= 现有下列热化学方程式:
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH3=-890 kJ·mol-1
④CH3CH2OH(l)+3O2(g)===2CO2(g)+3H2O(l) ΔH4=-1 367 kJ·mol-1
下列说法正确的是________。
①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH2=-566 kJ·mol-1
③CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH3=-890 kJ·mol-1
④CH3CH2OH(l)+3O2(g)===2CO2(g)+3H2O(l) ΔH4=-1 367 kJ·mol-1
下列说法正确的是________。
| A.CO(g)的燃烧热比C(s)的燃烧热大 |
| B.ΔH4>ΔH3>ΔH2>ΔH1 |
| C.CO(g)具有的能量比CO2(g)高 |
| D.1 mol C2H5OH蒸气完全燃烧生成CO2和液态水,放出大于1 367 kJ的热量 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


