解答题-结构与性质 适中0.65 引用2 组卷180
过渡金属元素在工业生产中发挥着重要作用。技术人员晒制蓝图时,用K3[Fe(C2O4)3]●3H2O(三草酸合铁酸钾晶体)作感光剂,再以K3[Fe(CN)6](六氰合铁酸钾)溶液作显影剂。
请回答以下问题:
(1)铁元素位于元素周期表的___________ 区,Fe3+的基态价电子排布图为___________ ;在上述两种钾盐中第一电离能最大的元素为___________ 。
(2)C与Si为同主族元素,高纯硅制备过程中会生成SiHCl3、SiCl4等中间产物。 已知电负性:H>Si,则SiHCl3中H的化合价为___________ ;SiCl4中硅原子的杂化类型是___________ ; 沸点:SiHCl3<SiC14原因是___________ 。
(3)复兴号亚运智能动车组列车材质用到Mn、Co等元素。Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],CH3CN中σ 键与π 键数目之比为___________ ;CH3CN与Mn形成___________ 键。
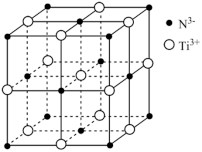
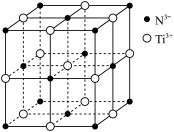
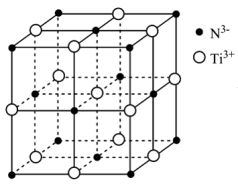
(4)时速600千米的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞棱长)为a D(1D= 10-10m),其中阴离子(N3-)采用面心立方最密堆积方式,则1个晶胞中含有___________ 个TiN;该氮化钛的密度为___________ g/cm3(列出计算式,阿伏加德罗常数的值为NA)。
请回答以下问题:
(1)铁元素位于元素周期表的
(2)C与Si为同主族元素,高纯硅制备过程中会生成SiHCl3、SiCl4等中间产物。 已知电负性:H>Si,则SiHCl3中H的化合价为
(3)复兴号亚运智能动车组列车材质用到Mn、Co等元素。Mn的一种配合物化学式为[Mn(CO)5(CH3CN)],CH3CN中σ 键与π 键数目之比为
(4)时速600千米的磁浮列车需用到超导材料。超导材料TiN具有NaCl型结构(如图),晶胞参数(晶胞棱长)为a D(1D= 10-10m),其中阴离子(N3-)采用面心立方最密堆积方式,则1个晶胞中含有

23-24高三上·宁夏银川·阶段练习
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网