解答题-原理综合题 较难0.4 引用1 组卷33
烟道气中含 、
、 、
、 等多种有害气体,合理治理烟道气中具有重要意义。
等多种有害气体,合理治理烟道气中具有重要意义。
Ⅰ.烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:




(1)则反应:

___________ (用含 、
、 的式子表示)。
的式子表示)。
Ⅱ.利用 可将
可将 转化为无害的
转化为无害的 ,其反应为:
,其反应为: 。在容积均为
。在容积均为 的甲、乙两个恒温(反应温度分别为℃、
的甲、乙两个恒温(反应温度分别为℃、 ℃)恒容密闭容器中,分别加入物质的量之比为
℃)恒容密闭容器中,分别加入物质的量之比为 的
的 和
和 ,测得各容器中
,测得各容器中 随反应时间
随反应时间 的变化情况如下表所示:
的变化情况如下表所示:
(2)
___________  ,该反应的
,该反应的
___________ 0。(填“>”或“<”)
(3) 时,该反应的平衡常数为
时,该反应的平衡常数为___________ ;若再加入 和
和 ,平衡向
,平衡向___________ (填“正反应方向”、“逆反应方向”或“不”)移动。
Ⅲ.对烟道气中的进行回收再利用具有较高的社会价值和经济价值,涉及到的主要反应是:
 。
。
(4)向三个体积相同的恒容密闭容器中通入 和
和 发生反应,反应体系的总压强随时间的变化如图所示。
发生反应,反应体系的总压强随时间的变化如图所示。
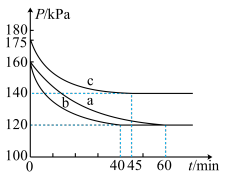
①实验 中,
中, 内
内 的平均反应速率为
的平均反应速率为___________  。
。
②与实验 相比,实验
相比,实验 改变的条件可能是
改变的条件可能是___________ 。
③实验 中
中 的平衡转化率为
的平衡转化率为___________ 。
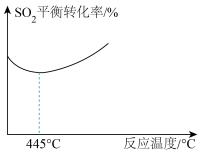
(5)其他条件不变时,随着温度的升高, 的平衡转化率随温度的变化曲线如图所示,温度高于445℃后
的平衡转化率随温度的变化曲线如图所示,温度高于445℃后 平衡转化率升高可能的原因
平衡转化率升高可能的原因___________ 。(已知硫的沸点约是445℃)
Ⅰ.烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
(1)则反应:
Ⅱ.利用
| 0 | 10 | 20 | 30 | 40 | |
| 甲( | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| 乙( | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
(2)
(3)
Ⅲ.对烟道气中的进行回收再利用具有较高的社会价值和经济价值,涉及到的主要反应是:
(4)向三个体积相同的恒容密闭容器中通入

①实验
②与实验
③实验
(5)其他条件不变时,随着温度的升高,

23-24高二上·福建福州·期中
类题推荐
烟道气中含氧NO、 、
、 等多种有害气体,合理治理烟道气中具有重要意义。
等多种有害气体,合理治理烟道气中具有重要意义。
(1)烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:




则反应:

___________ (用含 、
、 的式子表示)。
的式子表示)。
(2)利用CO可将NO转化为无害的 ,其反应为:
,其反应为: 。在容积均为2L的甲、乙两个恒温(反应温度分别为
。在容积均为2L的甲、乙两个恒温(反应温度分别为 ℃、
℃、 ℃)恒容密闭容器中,分别加入物质的量之比为1∶1的NO和CO,测得各容器中
℃)恒容密闭容器中,分别加入物质的量之比为1∶1的NO和CO,测得各容器中 随反应时间t的变化情况如下表所示:
随反应时间t的变化情况如下表所示:
①已知 ,则该反应的△H
,则该反应的△H___________ 0(填“>”或“<”)。
②甲容器达平衡时,体系的压强与反应开始时体系的压强之比为___________ 。
(3)对烟道气中的 进行回收再利用具有较高的社会价值和经济价值。
进行回收再利用具有较高的社会价值和经济价值。
其反应为:
①写出该反应平衡常数表达式___________ 。
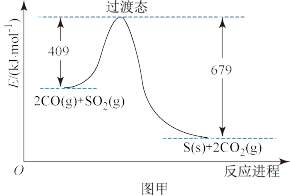
②由 和CO反应生成S和
和CO反应生成S和 的能量变化如图甲所示,在恒温恒容的密闭容器中进行反应,对此反应下列说法正确的是
的能量变化如图甲所示,在恒温恒容的密闭容器中进行反应,对此反应下列说法正确的是___________ 。
a.若混合气体密度保持不变,则已达平衡状态
b.从反应开始到平衡,容器内气体的压强保持不变
c.达平衡后若再充入一定量 ,新平衡体系混合气体中CO的体积分数增大
,新平衡体系混合气体中CO的体积分数增大
d.分离出一部分S,正、逆反应速率均保持不变
(4)用电化学法模拟工业处理对烟道气中的 。如图乙装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
。如图乙装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
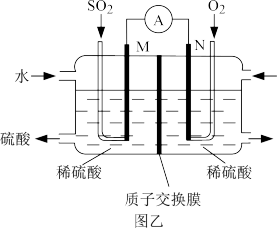
①M极发生的电极反应式为___________ 。
②当外电路通过0.2mol电子时,质子交换膜右侧的溶液质量___________ (填“增大”或“减小”),___________ g。
(1)烟道气中的氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
则反应:
(2)利用CO可将NO转化为无害的
| t/min | 0 | 10 | 20 | 30 | 40 |
| 甲( | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| 乙( | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②甲容器达平衡时,体系的压强与反应开始时体系的压强之比为
(3)对烟道气中的
其反应为:
①写出该反应平衡常数表达式
②由

a.若混合气体密度保持不变,则已达平衡状态
b.从反应开始到平衡,容器内气体的压强保持不变
c.达平衡后若再充入一定量
d.分离出一部分S,正、逆反应速率均保持不变
(4)用电化学法模拟工业处理对烟道气中的

①M极发生的电极反应式为
②当外电路通过0.2mol电子时,质子交换膜右侧的溶液质量
氯氨是常用的饮用水消毒剂,是氯气遇到氨气反应生成的一类化合物,主要包括一氯胺、二氯胺和三氯胺( 、
、 和
和 ),回答下列问题:
),回答下列问题:
(1)①工业上可利用反应 制备一氯胺,已知部分化学键的键能如下表所示(假设不同物质中同种化学键的键能相同),则该反应的
制备一氯胺,已知部分化学键的键能如下表所示(假设不同物质中同种化学键的键能相同),则该反应的
_______ 。
②一氯胺是重要的水消毒剂,原因是一氯胺在中性环境中会发生水解,生成具有强烈杀菌消毒作用的物质,该反应的化学方程式_______ 。
(2)用 和
和 反应制备二氯胺的方程式为
反应制备二氯胺的方程式为 ,向容积均为
,向容积均为 的甲
的甲 、乙
、乙 的两个容器中分别加入
的两个容器中分别加入 和
和 ,测得各容器中
,测得各容器中 随反应时间t的变化情况如下表所示:
随反应时间t的变化情况如下表所示:
①甲容器中, 内用
内用 的浓度变化表示的平均反应速率
的浓度变化表示的平均反应速率
_______ 。
②该反应的
_______ 0(填“>”或“<”)。
③对该反应,下列说法正确的是_______ (填选项字母)。
A.若容器内气体密度不变,则表明反应达到平衡状态
B.若容器内 和
和 物质的量之比不变,则表明反应达到平衡状态
物质的量之比不变,则表明反应达到平衡状态
C.反应达到平衡后其他条件不变,充入一定量氦气, 的转化率增大
的转化率增大
D.反应达到平衡后其他条件不变,加入一定量的 ,平衡向逆反应方向移动
,平衡向逆反应方向移动
(3)恒温条件下, 和
和 发生反应
发生反应 ,测得平衡时
,测得平衡时 和
和 的物质的量浓度与平衡总压的关系如图所示:
的物质的量浓度与平衡总压的关系如图所示:
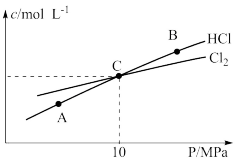
①A、B、C三点中 转化率最高的是
转化率最高的是_______ 点(填“A”“B”或“C”)。
②计算C点时该反应的压强平衡常数
_______  (
( 是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(1)①工业上可利用反应
| 化学键 | ||||
| 键能 | 391 | 243 | 191 | 431 |
(2)用
| 0 | 40 | 80 | 120 | 160 | |
| 2.00 | 1.50 | 1.10 | 0.80 | 0.80 | |
| 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②该反应的
③对该反应,下列说法正确的是
A.若容器内气体密度不变,则表明反应达到平衡状态
B.若容器内
C.反应达到平衡后其他条件不变,充入一定量氦气,
D.反应达到平衡后其他条件不变,加入一定量的
(3)恒温条件下,

①A、B、C三点中
②计算C点时该反应的压强平衡常数
氮及其化合物与人们的生活生产密切相关。回答下列问题:
(1)微生物作用下,废水中的NH 可转化为NO
可转化为NO ,该反应分两步反应:
,该反应分两步反应:
Ⅰ步:2 NH (aq)+3O2(g)=2NO
(aq)+3O2(g)=2NO (aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
(aq)+4H+(aq)+2H2O(l) ΔH=-546 kJ/mol
Ⅱ步:2NO (aq)+O2(g)=2NO
(aq)+O2(g)=2NO (aq) ΔH=-146 kJ/mol。
(aq) ΔH=-146 kJ/mol。
则低浓度氨氮废水中的NH (aq)氧化生成NO
(aq)氧化生成NO (aq)的热化学方程式为:NH
(aq)的热化学方程式为:NH (aq)+2O2(g)=2H+(aq)+H2 O(l)+NO
(aq)+2O2(g)=2H+(aq)+H2 O(l)+NO (aq) ΔH=
(aq) ΔH=___________ kJ/mol。
(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
已知可逆反应N2O4(g) 2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
2NO2(g) ΔH>0。在恒容密闭容器中充入一定量的N2O4,发生上述反应。测得N2O4的平衡转化率[α(N2O4)]随温度的变化如下图某条曲线:
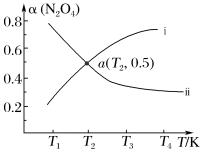
α(N2O4)随温度的变化的正确曲线是___________ (填“i”或“ii”)。若该容器中通入N2O4的起始浓度为2mol/L,则a点温度下的平衡常数K=___________ 。若加入催化剂,图中的曲线会___________ (填“上移”、“下移”或“不移”)。
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
N2(g)+2CO2(g) ΔH<0。已知甲、乙两个恒温恒容容器,容积均为1 L,两个容器中加入的CO的物质的量及CO随反应时间的变化如下表:
则反应温度高的容器是___________ (填“甲”或“乙”);甲容器中,0~120 min的速率v(N2)=___________ mol/(L·min),达到化学平衡后,乙容器中各物质均加倍,则平衡向___________ (“正反应”或“逆反应”)方向移动。
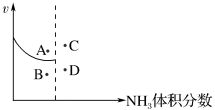
(4)500 ℃时,恒容密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,已知该反应放热,且随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为___________ (从点“A、B、C、D”中选择)。
(1)微生物作用下,废水中的NH
Ⅰ步:2 NH
Ⅱ步:2NO
则低浓度氨氮废水中的NH
(2)氮与氧能形成多种二元化合物,这些化合物往往不稳定,其中NO2比较稳定。
已知可逆反应N2O4(g)

α(N2O4)随温度的变化的正确曲线是
(3)机动车尾气是造成雾霾的主要因素之一,CO、NO在催化剂作用下可转化为无害气体:2NO(g)+2CO(g)
| t/min | 0 | 40 | 80 | 120 | 160 |
| n甲(CO)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n乙(CO)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
(4)500 ℃时,恒容密闭容器中通入1 mol N2和3 mol H2,模拟合成氨的反应,已知该反应放热,且随着反应的进行合成氨的正反应速率与NH3的体积分数的关系如下图所示,若升高温度再次达到平衡时,可能的点为

组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


