解答题-工业流程题 较难0.4 引用3 组卷406
磷酸亚铁锂( )为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池,
)为近来新开发的锂离子电池电极材料,主要用于动力锂离子电池, 废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下:
废料中(含Al、石墨),其中磷、铁、锂的综合回收工艺流程图如下:
②LiOH、 的溶解度与温度的关系如下表:
的溶解度与温度的关系如下表:
(1)过程I“碱浸”的目的是___________ 。
(2)若浸出液中存在大量 离子,则反应的离子方程式为
离子,则反应的离子方程式为___________ 。
(3)①过程III得到“沉淀Y”的离子方程式为___________ 。
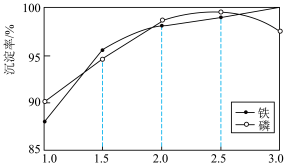
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如下图所示。由图可知,过程III应选取的最佳沉淀时的pH为___________ 。随pH的增加,磷的沉淀率开始下降,而铁沉淀率未下降,分析原因为___________ 。___________ 。
A.NaOH20-40℃ B.NaOH80-100℃
C. 20-40℃ D.
20-40℃ D. 60-80℃
60-80℃
②常温下,测得滤液1中 ,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
,某同学取该100ml滤液进行“沉锂”反应。加入50mlX溶液却未见沉淀,若不考虑液体混合时的体积变化,则该同学加入的X溶液最大浓度为
___________  。
。
②LiOH、
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | LiOH | 11.9 | 12.4 | 13.2 | 14.6 | 16.6 | 19.1 |
| 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 | ||
(1)过程I“碱浸”的目的是
(2)若浸出液中存在大量
(3)①过程III得到“沉淀Y”的离子方程式为
②一定条件下,探究了pH对磷酸铁沉淀的影响,结果如下图所示。由图可知,过程III应选取的最佳沉淀时的pH为
A.NaOH20-40℃ B.NaOH80-100℃
C.
②常温下,测得滤液1中
2023高三上·湖南湘西·竞赛
类题推荐
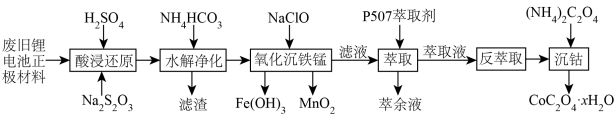
某锂离子二次电池的正极材料主要为LiCoO2,还含有少量Al、Fe、Mn、Ni的化合物。通过如图流程利用废旧锂离子电池制备草酸钴晶体(CoC2O4•xH2O):
已知该工艺条件下,有关金属离子沉淀完全(c=1×10-5mol•L-1)的pH见表:
回答下列问题:
(1)“酸浸还原”步骤,LiCoO2发生的反应中氧化产物为硫酸盐,则氧化剂与还原剂的物质的量之比为________ 。
(2)“滤渣”成分是________ 。“水解净化”时,温度不宜超过70℃,原因是________ 。
(3)“氧化沉铁锰”中,反应生成MnO2的离子方程式为________ 。
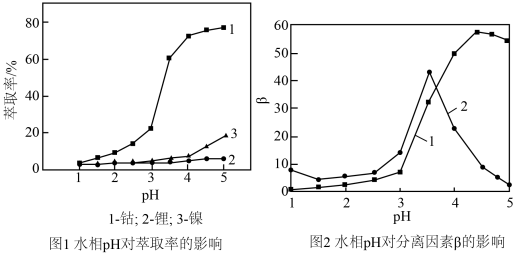
(4)利用“P507萃取剂”从“滤液”中分离Co2+。研究水相pH对金属离子分离的影响,所得结果如图所示,其中分离因素β越大,表明萃取剂对不同离子分离效果越好。
由图可知,萃取时的最佳水相pH为________ (填字母)。
(5)“沉钴”适宜温度为50℃,温度过高会使Co2+沉淀率下降,可能的原因是________ 。
(6)采用热重分析法测定草酸钴晶体样品所含结晶水数目,将样品加热到140℃时失掉1个结晶水,失重9.84%。CoC2O4•xH2O中x=________ 。

已知该工艺条件下,有关金属离子沉淀完全(c=1×10-5mol•L-1)的pH见表:
| 离子 | Co2+ | Fe3+ | Fe2+ | Al3+ | Mn2+ | Ni2+ |
| pH | 9.3 | 3.2 | 9.0 | 4.7 | 10.1 | 8.9 |
(1)“酸浸还原”步骤,LiCoO2发生的反应中氧化产物为硫酸盐,则氧化剂与还原剂的物质的量之比为
(2)“滤渣”成分是
(3)“氧化沉铁锰”中,反应生成MnO2的离子方程式为
(4)利用“P507萃取剂”从“滤液”中分离Co2+。研究水相pH对金属离子分离的影响,所得结果如图所示,其中分离因素β越大,表明萃取剂对不同离子分离效果越好。

由图可知,萃取时的最佳水相pH为
| A.2.5 | B.3.0 | C.3.5 | D.4.0 |
(5)“沉钴”适宜温度为50℃,温度过高会使Co2+沉淀率下降,可能的原因是
(6)采用热重分析法测定草酸钴晶体样品所含结晶水数目,将样品加热到140℃时失掉1个结晶水,失重9.84%。CoC2O4•xH2O中x=
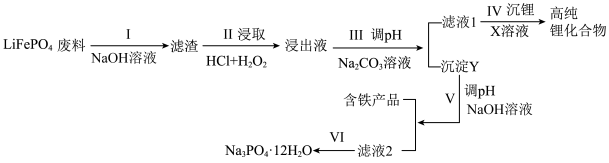
从废旧磷酸铁理电池的正极材料(含LiFePO4、石墨粉和铝箔等)中综合回收锂、铁和磷等的工艺流程如图所示:
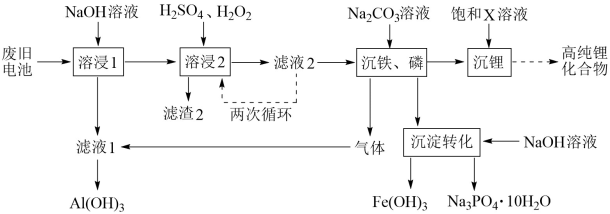
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为________ 。
(2)完成“溶浸2”反应的离子方程式:____LiFePO4+___H2O2+____=_____Li++____+_____ +____H2O
+____H2O
__________
(3)“滤渣2”的主要成分是__________ 。
(4) “滤渣2”循环两次的目的是_______ 。
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为_______ 。实验中,铁、磷的沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是_________ 。
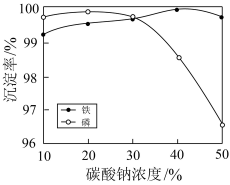
(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是_______ (填标号)。
A. NaOH 20-40℃ B. NaOH 80-100℃ C. Na2CO3 20-40℃ D. Na2CO3 60-80℃

 | 0 | 20 | 40 | 60 | 80 | 100 |
| LiOH | 11.9 | 12.4 | 13.2 | 14.6 | 16.6 | 19.1 |
| Li2CO3 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为
(2)完成“溶浸2”反应的离子方程式:____LiFePO4+___H2O2+____=_____Li++____+_____
(3)“滤渣2”的主要成分是
(4) “滤渣2”循环两次的目的是
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为

(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是
A. NaOH 20-40℃ B. NaOH 80-100℃ C. Na2CO3 20-40℃ D. Na2CO3 60-80℃
新能源汽车的核心部件是锂离子电池,常用磷酸亚铁锂(LiFePO4)作电极材料。对LiFePO4废旧电极(含杂质 A1、石墨粉)回收并获得高纯Li2CO3的工业流程图:
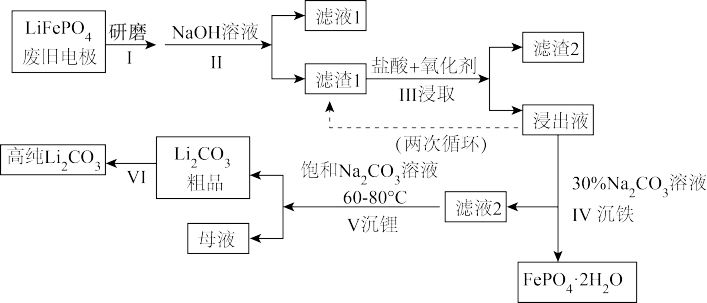
资料:碳酸锂在水中溶解度:
(1)“过程i”除研磨粉碎外,请再写出一种可以提高过程ii溶解速率的措施:____ 。
(2)“过程ii”加入足量 NaOH 溶液的离子反应方程式是________ 。
(3)“过程iii ”采用不同氧化剂分别进行实验,均采用 Li含量为3.7% 的原料,控制pH 为3.5,浸取1.5h后,实验结果如表所示:
①实验2中,NaClO3与盐酸反应生成黄绿色气体,大大增加了酸和氧化剂的用量,该反应的离子方程式为_______ 。
②“过程iii”得到的浸出液循环两次的目的是________ 。
(4)浸出液中存在大量 H2PO4 -和 HPO ,已知:H2PO
,已知:H2PO ⇌HPO
⇌HPO +H+,HPO
+H+,HPO ⇌PO
⇌PO +H+,结合
+H+,结合平衡移动 原理,解释“过程iv”得到磷酸铁晶体的原因:___ 。
(5)“过程v”中,若“沉锂”中c(Li+ )=1.0mol·L-1,加入等体积饱和 Na2CO3溶液(浓度约为1.78mol/L),此时实验所得沉锂率为___ (已知Li2CO3的Ksp为9.0×10-4)。
(6)简述“过程vi”的操作:_________________ 。

资料:碳酸锂在水中溶解度:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
(2)“过程ii”加入足量 NaOH 溶液的离子反应方程式是
(3)“过程iii ”采用不同氧化剂分别进行实验,均采用 Li含量为3.7% 的原料,控制pH 为3.5,浸取1.5h后,实验结果如表所示:
| 序号 | 酸 | 氧化剂 | 浸出液Li+浓度(g/L) | ) 滤渣中Li含量/% |
| 实验1 | HCl | H2O2 | 9.02 | 0.10 |
| 实验2 | HCl | NaClO3 | 9.05 | 0.08 |
| 实验3 | HCl | O2 | 7.05 | 0.93 |
②“过程iii”得到的浸出液循环两次的目的是
(4)浸出液中存在大量 H2PO4 -和 HPO
(5)“过程v”中,若“沉锂”中c(Li+ )=1.0mol·L-1,加入等体积饱和 Na2CO3溶液(浓度约为1.78mol/L),此时实验所得沉锂率为
(6)简述“过程vi”的操作:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


