解答题-实验探究题 较易0.85 引用2 组卷107
高纯碳酸锰广泛应用于电子工业,是制备高性能磁性材料的原料。某化学小组在实验室模拟用软锰矿粉(主要成分为 )制备
)制备 。回答下列问题:
。回答下列问题:
(1)制备 溶液:将mg软锰矿粉经除杂后制得
溶液:将mg软锰矿粉经除杂后制得 浊液,向
浊液,向 浊液中通入
浊液中通入 ,制得
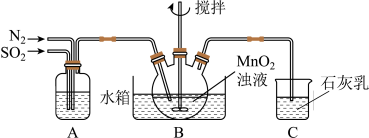
,制得 溶液,实验装置如图所示(夹持和加热装置略)。
溶液,实验装置如图所示(夹持和加热装置略)。
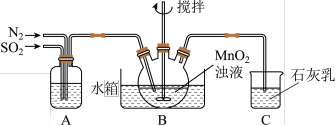
①通过装置A可观察通入: 与
与 的快慢,则A中加入的最佳试剂是
的快慢,则A中加入的最佳试剂是____________ ;
②装置C的作用是______ ;
③ 转化为
转化为 的离子方程式为
的离子方程式为____________ ;
④实验中若将 换成空气,将导致
换成空气,将导致 浓度明显大于
浓度明显大于 ,浓度,原因是
,浓度,原因是____________ 。
(2)制备 固体:在搅拌下向
固体:在搅拌下向 溶液中缓慢滴加
溶液中缓慢滴加 溶液,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。生成
溶液,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。生成 的离子方程式为
的离子方程式为______ 。检验沉淀是否洗涤干净的方法是______ 。
(3)测定碳酸锰产品的纯度:称取0.2500g碳酸锰产品于锥形瓶中,加12.50mL磷酸,加热后,立即加入1g硝酸铵,充分反应后,碳酸锰全部转化为 ,多余的硝酸铵全部分解,除去氮氧化物后,冷却至室温。将上述所得溶液加水稀释至50mL,滴加2~3滴指示剂,然后用0.1000 mol⋅L
,多余的硝酸铵全部分解,除去氮氧化物后,冷却至室温。将上述所得溶液加水稀释至50mL,滴加2~3滴指示剂,然后用0.1000 mol⋅L 的硫酸亚铁铵
的硫酸亚铁铵 标准溶液滴定[反应为
标准溶液滴定[反应为 ],重复操作3次,记录数据如表:(已知:
],重复操作3次,记录数据如表:(已知: 的摩尔质量为115g/mol)
的摩尔质量为115g/mol)
则产品的纯度为______ 。若滴定终点时仰视读数,则测得的碳酸锰产品的纯度______ (填“偏高”“偏低”或“无影响”)。
(1)制备

①通过装置A可观察通入:
②装置C的作用是
③
④实验中若将
(2)制备
(3)测定碳酸锰产品的纯度:称取0.2500g碳酸锰产品于锥形瓶中,加12.50mL磷酸,加热后,立即加入1g硝酸铵,充分反应后,碳酸锰全部转化为
滴定次数 | 0.1000 mol⋅L | |
滴定前 | 滴定后 | |
1 | 1.15 | 11.05 |
2 | 0.12 | 11.42 |
3 | 0.30 | 10.40 |
23-24高三上·贵州贵阳·阶段练习
类题推荐
高纯MnCO3广泛应用于电子工业,是制备高性能磁性材料的主要原料。某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质主要为铁的化合物)制备高纯碳酸锰。回答下列问题:
(1)制备MnSO4溶液:将mg软锰矿粉与水混合制得MnO2浊液,向MnO2浊液中通入SO2,制得MnSO4溶液,实验装置如图所示(夹持和加热装置略):
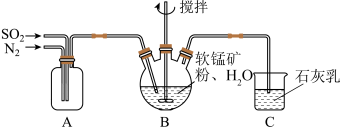
①通过装置A可观察SO2和N2的通入速率,则A中加入的最佳试剂是________ 。
②通入过量SO2和N2的混合气进行“浸锰”操作,B中发生反应的离子方程式为________ 。
③“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如图。为减少MnS2O6的生成,“浸锰”过程适宜的温度是________ 。

④“浸锰”结束后,向B中加入一定量MnO2粉末,调节pH到3.8左右过滤,即可获得MnSO4溶液。查阅表格,回答加入一定量MnO2粉末的主要作用是________ 。
(2)制备MnCO3固体:在搅拌下向MnSO4溶液中缓慢滴加NH4HCO3溶液,经过滤、洗涤、干燥,得到高纯碳酸锰,生成MnCO3的离子方程式为_______ 。已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解,选择用C2H5OH洗涤的原因是________ 。检验沉淀是否洗涤干净的操作是_______ 。
(3)测定碳酸锰产品的纯度:称取0.2500g碳酸锰产品于锥形瓶中,加12.50mL磷酸,在空气中加热充分反应,碳酸锰全部转化为[Mn(PO4)2]3-,冷却至室温。加水稀释至50mL,滴加2~3滴指示剂,然后用浓度为0.2000mol•L-1的硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定{反应方程式为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO }。重复操作3次,记录数据如表:
}。重复操作3次,记录数据如表:
则产品的纯度=_______ (保留四位有效数字)。
(1)制备MnSO4溶液:将mg软锰矿粉与水混合制得MnO2浊液,向MnO2浊液中通入SO2,制得MnSO4溶液,实验装置如图所示(夹持和加热装置略):

①通过装置A可观察SO2和N2的通入速率,则A中加入的最佳试剂是
②通入过量SO2和N2的混合气进行“浸锰”操作,B中发生反应的离子方程式为
③“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如图。为减少MnS2O6的生成,“浸锰”过程适宜的温度是

④“浸锰”结束后,向B中加入一定量MnO2粉末,调节pH到3.8左右过滤,即可获得MnSO4溶液。查阅表格,回答加入一定量MnO2粉末的主要作用是
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)3 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 |
(3)测定碳酸锰产品的纯度:称取0.2500g碳酸锰产品于锥形瓶中,加12.50mL磷酸,在空气中加热充分反应,碳酸锰全部转化为[Mn(PO4)2]3-,冷却至室温。加水稀释至50mL,滴加2~3滴指示剂,然后用浓度为0.2000mol•L-1的硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定{反应方程式为[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO
| 滴定 | 0.2000mol•L-1的硫酸亚铁铵标准溶液读数(mL) | |
| 次数 | 滴定前 | 滴定后 |
| 1 | 0.10 | 10.11 |
| 2 | 0.22 | 10.22 |
| 3 | 0.05 | 10.04 |
磁性材料产业是21世纪各国竞相发展的高科技支柱产业之一,磁性材料广泛用于电子信息、军事技术等领域。碳酸锰主要用于制备软磁铁氧体,工业上用含锰废水(主要金属离子为 、
、 、
、 ,还含有少量
,还含有少量 、
、 、
、 和
和 等离子)为原料,生产
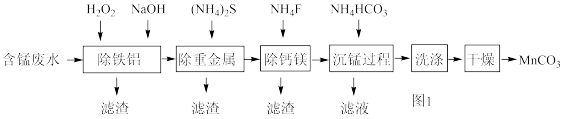
等离子)为原料,生产 的工艺流程如图1。
的工艺流程如图1。
已知该条件下 、
、 。
。
(1)流程中含锰废水经过前三步预处理,得到主要含有 的母液。
的母液。
①除铁铝时,在搅拌条件下先加入 溶液,再加入
溶液,再加入 溶液调节
溶液调节 。加入
。加入 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_______ 。
②除重金属时,滤渣的主要成分为_______ 。(填化学式)
③除钙镁时,为使 沉淀完全(当离子浓度降到
沉淀完全(当离子浓度降到 时,可视为沉淀完全),需控制溶液中
时,可视为沉淀完全),需控制溶液中 的最低浓度为
的最低浓度为_______  。
。
(2)沉锰过程在 为7.0条件下充分进行,反应温度对锰沉淀率的影响如图2所示。
为7.0条件下充分进行,反应温度对锰沉淀率的影响如图2所示。

①沉锰过程发生反应的离子方程式为_______ 。
②当温度超过30℃,沉锰反应的锰沉淀率随温度升高而下降的原因是_______ 。
(3)沉锰后过滤得到 粗产品,依次用去离子水和无水乙醇各洗涤2~3次,再低温干燥,得到纯净的
粗产品,依次用去离子水和无水乙醇各洗涤2~3次,再低温干燥,得到纯净的 。用无水乙醇洗涤的目的是
。用无水乙醇洗涤的目的是_______ 。
(4)测定碳酸锰产品的纯度:称取0.5000g碳酸锰产品于锥形瓶中,加25.00mL磷酸,加热,碳酸锰全部转化为 ,冷却至室温,加水稀释至100mL,滴加2~3滴指示剂,然后用浓度为
,冷却至室温,加水稀释至100mL,滴加2~3滴指示剂,然后用浓度为 的硫酸亚铁铵 [
的硫酸亚铁铵 [ ]标准溶液滴定(反应为
]标准溶液滴定(反应为 )。重复操作3次,记录数据如表。则产品的纯度=
)。重复操作3次,记录数据如表。则产品的纯度=_______ (MMn=55)。
若滴定终点时仰视滴定管读数,则测得的结果_______ (偏低或偏高)

已知该条件下
(1)流程中含锰废水经过前三步预处理,得到主要含有
①除铁铝时,在搅拌条件下先加入
②除重金属时,滤渣的主要成分为
③除钙镁时,为使
(2)沉锰过程在

①沉锰过程发生反应的离子方程式为
②当温度超过30℃,沉锰反应的锰沉淀率随温度升高而下降的原因是
(3)沉锰后过滤得到
(4)测定碳酸锰产品的纯度:称取0.5000g碳酸锰产品于锥形瓶中,加25.00mL磷酸,加热,碳酸锰全部转化为
| 滴定次数 | 0.2000mol/L的硫酸亚铁铵标准溶液读数 (mL) | |
| 滴定前 | 滴定后 | |
| 1 | 0.10 | 20.20 |
| 2 | 1.32 | 21.32 |
| 3 | 1.05 | 20.95 |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网