单选题 适中0.65 引用1 组卷122
实验室常用 标定(NH4)2Fe(SO4)2,同时使
标定(NH4)2Fe(SO4)2,同时使 再生,其反应原理如图所示。下列说法错误的是
再生,其反应原理如图所示。下列说法错误的是
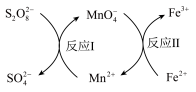

| A.反应Ⅱ中 Fe2+是还原剂 |
| B.由反应Ⅰ、Ⅱ可知,氧化性: |
| C.发生反应Ⅰ和反应Ⅱ时,溶液颜色均发生了变化 |
| D. |
23-24高一上·安徽安庆·阶段练习
类题推荐
重铬酸钾溶液中存在如下平衡: (橙色)+H2O
(橙色)+H2O 2H++2Cr
2H++2Cr (黄色)
(黄色)
①向2mL0.1mol•L-1K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴6mol/LH2SO4,溶液由黄色变为橙色。②向2mL0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量的(NH4)2Fe(SO4)2溶液,发生反应 +14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O。
下列分析正确的是
①向2mL0.1mol•L-1K2Cr2O7溶液中滴入3滴6mol•L-1NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴6mol/LH2SO4,溶液由黄色变为橙色。②向2mL0.1mol•L-1酸化的K2Cr2O7溶液中滴入适量的(NH4)2Fe(SO4)2溶液,发生反应
下列分析正确的是
| A.实验①和②均能证明K2Cr2O7溶液中存在上述平衡 |
| B.实验②能说明氧化性: |
| C.实验②的反应中电子转移总数为6 |
| D. |
常温下,在溶液中可发生以下反应:
①2Fe2++Br2===2Fe3++2Br-;②2Br-+Cl2===Br2+2Cl-;③2Fe3++2I-===2Fe2++I2。
由此判断下列说法错误的是
①2Fe2++Br2===2Fe3++2Br-;②2Br-+Cl2===Br2+2Cl-;③2Fe3++2I-===2Fe2++I2。
由此判断下列说法错误的是
| A.I-和Cl2不能够发生氧化还原反应 |
| B.反应②中当有1 mol Cl2被还原时,有2 mol Br-被氧化 |
| C.氧化性强弱顺序为:Cl2>Br2>Fe3+>I2 |
| D.还原性强弱顺序为:I->Fe2+>Br->Cl- |
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是
| A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| B.在H2O2分解过程中,溶液的pH逐渐下降 |
| C.在H2O2分解过程中, Fe2+和Fe3+的总量发生变化 |
| D.H2O2生产过程要严格避免混入Fe2+ |
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


