填空题 较易0.85 引用2 组卷232
金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的原子结构示意图表示式为___________ ,在周期表中的位置是___________ 。
(2)Na2O2的电子式为___________ 。Na2O2可作供氧剂,写出Na2O2与CO2反应的化学方程式___________ 。若有1molNa2O2参加反应则转移电子的物质的量为___________ mol。
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO +___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式
+___________H++___________Na2O2=___________Mn2++___________O2↑+___________H2O+___________Na+,配平该离子方程式_________ ;该反应说明Na2O2具有___________ 性(选填“氧化”,“还原”或“漂白”)。
(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为___________ g。
(1)基态Na原子的原子结构示意图表示式为
(2)Na2O2的电子式为
(3)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应: ___________MnO
(5)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1molNa2CO3·NaHCO3·2H2O经充分加热得到Na2CO3的质量为
23-24高三上·黑龙江哈尔滨·期中
类题推荐
金属钠及其化合物在人类生产、生活中起着重要作用。诸回答下列问题:
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为___________ ,采用空气和Na为原料可直接制备Na2O2.空气与熔融的金属Na反应前需依次通过的试剂为___________ 、___________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l) 2Na(1)+Cl2(g),加入CaCl2的目的是
2Na(1)+Cl2(g),加入CaCl2的目的是___________ 。
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
 +____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
+____ H++_____ Na2O2=____ Mn2++_____ Na+_____ O2↑+____H2O
①配平上述离子方程式___________ 。
②该反应说明Na2O2具有___________ (选填“氧化性”“还原性"或“漂白性”)。
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为___________ 。
(1)向一小烧杯中分别加入等体积的水和煤油,片刻后再向该烧杯中加入黄豆粒大小的金属钠,可能观察到的现象是___________(填序号)。
A.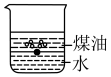 | B.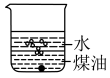 |
C. | D. |
(2)金属钠在氧气中燃烧生成Na2O2,其电子式为
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(3)NaCl的熔点为800.8℃。工业上采用电解熔融的NaCl和CaCl2混合盐制备金属Na,电解的化学方程式为:2NaCl(l)
(4)向酸性KMnO4溶液中加入Na2O2粉末,观察到溶液褪色,发生如下反应。
①配平上述离子方程式
②该反应说明Na2O2具有
(5)在密闭容器中,将a mol Na2O2和b mol NaHCO3固体混合物加热至250℃,充分反应后,若剩余固体为Na2CO3和NaOH,排出气体为O2和H2O时,a:b的取值范围为
金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)工业上用NaOH溶液捕捉废气中的SO2,下列说法错误的是_______。
(2)根据钠与水(滴有酚酞溶液)反应的实验现象,不能得出的结论是_______。
(3)采用空气和Na为原料可直接制备Na2O2,空气与熔融金属Na反应前需依次通过_______ 、_______ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1 mol该物质经充分加热得到固体的质量应为_______ g。
(1)工业上用NaOH溶液捕捉废气中的SO2,下列说法错误的是_______。
| A.捕捉过程中溶液pH会下降 | B.NaOH属于离子化合物 |
| C.SO2属于非电解质 | D.1molNaOH最多捕捉11.2LSO2(标状下) |
| A.钠的密度比水小 | B.钠的硬度小 |
| C.钠很活泼,易与水反应生成碱性物质 | D.钠的熔点低 |
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(4)天然碱的主要成分为Na2CO3·NaHCO3·2H2O,1 mol该物质经充分加热得到固体的质量应为
金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)存贮时,Na应保存在___________ 中;实验室取用少量金属钠需要用到的实验用品有玻璃片、小刀、___________ 和___________ 等。
(2)工业上采用电解熔融NaCl(熔点为 )制备金属Na,电解反应方程式:
)制备金属Na,电解反应方程式: ,加入
,加入 的目的是
的目的是___________ (填序号)。
a.作催化剂,加块电解反应的速率
b.作还原剂,将 还原为
还原为
c.作助熔剂,降低生产过程的能耗
d.作氧化剂,将 氧化为
氧化为
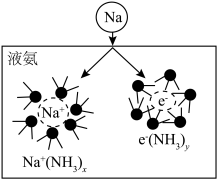
(3)钠能与液氨反应,生成氨基钠(NaNH2)和一种气体单质。将钠投入液氨中,会快速得到深蓝色溶液(生成蓝色的溶剂合电子,如图所示),后慢慢产生气泡。
①生成的气体为___________ (填分子式)
②当 钠投入液氨生成
钠投入液氨生成 气体时,Na共失去的电子
气体时,Na共失去的电子___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(4)采用空气和Na为原料可直接制备Na2O2。为防止空气中的某些成分与Na2O2反应,空气与熔融金属Na反应前需依次通过___________ 。(填序号)
a.无水 b.饱和食盐水 c.饱和
b.饱和食盐水 c.饱和 溶液 d.
溶液 d. 溶液 e.
溶液 e. 溶液
溶液
(5)对固体 充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体
充分加热,产生的气体先通过足量浓硫酸,再通过足量Na2O2,Na2O2增重0.28g,则固体 的质量为
的质量为___________ g。
(6)为确定 和
和 混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度的稀盐酸
混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度的稀盐酸 ,充分反应,产生
,充分反应,产生 的体积(已折算成标准状况下的体积,不考虑
的体积(已折算成标准状况下的体积,不考虑 在水中的溶解)如下表:
在水中的溶解)如下表:
①样品中物质的量之比
___________ 。
②稀盐酸的物质的量浓度
___________ mol/L。
(1)存贮时,Na应保存在
(2)工业上采用电解熔融NaCl(熔点为
a.作催化剂,加块电解反应的速率
b.作还原剂,将
c.作助熔剂,降低生产过程的能耗
d.作氧化剂,将
(3)钠能与液氨反应,生成氨基钠(NaNH2)和一种气体单质。将钠投入液氨中,会快速得到深蓝色溶液(生成蓝色的溶剂合电子,如图所示),后慢慢产生气泡。

①生成的气体为
②当
(4)采用空气和Na为原料可直接制备Na2O2。为防止空气中的某些成分与Na2O2反应,空气与熔融金属Na反应前需依次通过
a.无水
(5)对固体
(6)为确定
| 实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 盐酸体积(mL) | 30.0 | 30.0 | 30.0 | 30.0 |
| 样品质量(g) | 2.96 | 3.70 | 5.18 | 6.66 |
| 672 | 840 | 896 | 672 |
②稀盐酸的物质的量浓度
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


