填空题 适中0.65 引用1 组卷55
化学能与热能的转化是当今化学研究的热点。回答下列问题:
(1)卤化镁高温分解的相对能量变化如图所示。
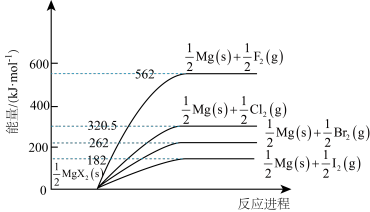
①写出该温度下MgF2(s)分解的热化学方程式:___________ 。
②反应MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=___________ kJ·mol-1。
(2)氢氟酸是一种弱酸,已知25℃时:HF(aq) H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为
H+(aq)+F-(aq) △H=-10.4kJ·mol-1,H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,则表示稀HF溶液与稀NaOH溶液的热化学方程式为___________ ,氢氟酸的中和反应反应热的绝对值大于57.3kJ·mol-1的原因可能是___________ 。
(3)H2与F2在黑暗中混合也会发生剧烈反应,反应的热化学方程式为H2(g)+F2(g)=2HF(g) △H=—536.6kJ·mol-1,查阅文献,两种化学键键能数据如表:
则F2(g)=2F(g) △H=___________ kJ·mol-1。
(1)卤化镁高温分解的相对能量变化如图所示。
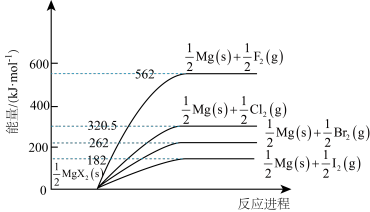
①写出该温度下MgF2(s)分解的热化学方程式:
②反应MgI2(s)+Br2(g)=MgBr2(s)+I2(g) △H=
(2)氢氟酸是一种弱酸,已知25℃时:HF(aq)
(3)H2与F2在黑暗中混合也会发生剧烈反应,反应的热化学方程式为H2(g)+F2(g)=2HF(g) △H=—536.6kJ·mol-1,查阅文献,两种化学键键能数据如表:
| 化学键 | H—H | F—H |
| E/(kJ·mol-1) | 436 | 565 |
2023高三·全国·专题练习
类题推荐
甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③CO2(g)+H2(g) CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3
(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
由此计算ΔH1=______ kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=_______ kJ·mol-1。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1 275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式_________________ 。
(3)已知常温时红磷比白磷稳定,已知:
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
比较反应中ΔH的大小:ΔH1_______ ΔH2(填“>”、“<”或“=”)。
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)===H2O(l)ΔH=﹣57.3 kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量_____ 57.3 kJ(填“>”、“<”或“=”)。
①CO(g)+2H2(g)
 CH3OH(g) ΔH1
CH3OH(g) ΔH1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2③CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH3
CO(g)+H2O(g) ΔH3(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
| E/(kJ·mol-1) | 436 | 343 | 1 076 | 465 | 413 |
由此计算ΔH1=
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1 275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(3)已知常温时红磷比白磷稳定,已知:
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1
②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2
比较反应中ΔH的大小:ΔH1
(4)已知:稀溶液中,H+(aq)+OH﹣(aq)===H2O(l)ΔH=﹣57.3 kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1 mol水,放出的热量
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
 O2(g)
O2(g) O(CO)
O(CO)
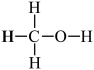 )既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)
)既是重要的化工原料,又可作为燃料。利用水煤气(主要成分为CO和H2)在催化剂作用下合成甲醇,发生的反应为:CO(g)+2H2(g)

