解答题-结构与性质 适中0.65 引用1 组卷150
I.纳米氧化亚铜 粒径在
粒径在 之间,是一种重要的无机化工原料,在涂料、有色玻璃和催化剂领域有着广泛的应用。
之间,是一种重要的无机化工原料,在涂料、有色玻璃和催化剂领域有着广泛的应用。
(1) 在元素周期表中的位置是第四周期
在元素周期表中的位置是第四周期___________ 族;
(2)基态铜原子的价电子排布式为___________。
(3)在普通玻璃中加入纳米 可制成红色玻璃。用光束照射该玻璃,在垂直方向上可以观察到
可制成红色玻璃。用光束照射该玻璃,在垂直方向上可以观察到___________ 。
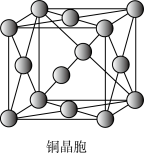
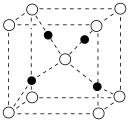
(4) 属于离子晶体,晶体结构如图所,图中●表示的微粒是___________。
属于离子晶体,晶体结构如图所,图中●表示的微粒是___________。
II. 溶于浓氨水中形成无色的
溶于浓氨水中形成无色的 ,该无色溶液接触空气会很快变成深蓝色。
,该无色溶液接触空气会很快变成深蓝色。
(5) 中
中 的N原子提供
的N原子提供___________ ,与中心离子形成___________ 。
A.空轨道、离子键 B.孤电子对、离子键
C.空轨道、配位键 D.孤电子对、配位键
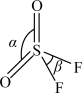
(6)已知 分子中
分子中 键角为107°,则
键角为107°,则 中
中 键角___________。
键角___________。
(7)无色溶液在空气中变色的原因可表示如下,完成并配平该离子方程式________ (化学计量数若为1可不写)。
III.纳米 的制备方法有多种,常见的有还原法、电解法等。
的制备方法有多种,常见的有还原法、电解法等。
(8)还原法以葡萄糖作为主要原料。能用葡萄糖制备 是因为其分子中含有
是因为其分子中含有___________ (填官能团名称),制备时除了葡萄糖溶液与硫酸铜溶液外,还需要___________ (填试剂名称)。
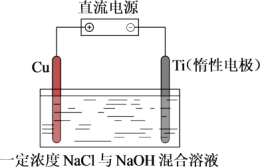
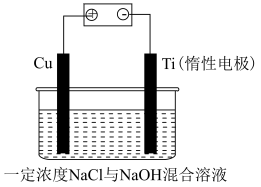
(9)电解法制备 的装置如图所示,电解过程中阳极依次发生反应:
的装置如图所示,电解过程中阳极依次发生反应:
①
②
③
阴极的电极反应式为___________ ;该法制备 的总反应可以表示为:
的总反应可以表示为:___________ 。
(1)
(2)基态铜原子的价电子排布式为___________。
| A. | B. | C. | D. |
(3)在普通玻璃中加入纳米
(4)

| A. | B. | C. | D. |
II.
(5)
A.空轨道、离子键 B.孤电子对、离子键
C.空轨道、配位键 D.孤电子对、配位键
(6)已知
| A.大于107° | B.小于107° | C.等于107° | D.等于107° |
(7)无色溶液在空气中变色的原因可表示如下,完成并配平该离子方程式
III.纳米
(8)还原法以葡萄糖作为主要原料。能用葡萄糖制备
(9)电解法制备

①
②
③
阴极的电极反应式为
23-24高三上·上海虹口·期末
类题推荐
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网
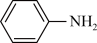 )常作为合成原料,与甲苯(
)常作为合成原料,与甲苯(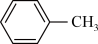 )相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是