解答题-实验探究题 较难0.4 引用1 组卷205
硫酰氯( )是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:
)是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为 ΔH<0,其实验装置如图所示(夹持仪器已省略):
ΔH<0,其实验装置如图所示(夹持仪器已省略):
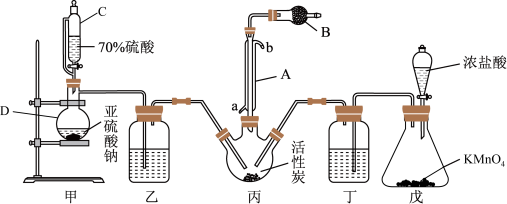
(1)仪器B的名称________ ,A的作用为________ ;B中盛放的药品是_________ 。
(2)装置戊中发生的反应的离子方程式为___________
(3)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示___________ 。
(4)装置甲发生反应的化学方程式为___________ 。
(5)实验开始时,戊中开始加入pg 固体,假设
固体,假设 在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯qmol,请计算硫酰氯的产率
在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯qmol,请计算硫酰氯的产率___________ (列出表达式)。
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| -54.1 | 69.1 | ①易水解,产生大量白雾,生成两种强酸 ②易分解: | |
| 10.4 | 338 | 强吸水性、稳定不易分解 |

(1)仪器B的名称
(2)装置戊中发生的反应的离子方程式为
(3)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示
(4)装置甲发生反应的化学方程式为
(5)实验开始时,戊中开始加入pg
22-23高二上·云南保山·期中
类题推荐
硫酰氯(SO2Cl2)是生产医药、农药、染料的重要原料。硫酰氯与硫酸的部分性质如下表:
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为SO2(g)+Cl2(g)=SO2Cl2(l) ΔH<0 ,其实验装置如图所示(夹持仪器已省略):

(1)D的名称_______ ,A的作用为_______ ;B中盛放的药品是_______ 。
(2)能替代装置戊中KMnO4是_______(填字母代号)。
(3)若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示_______ 。
(4)反应过程中,为防止SO2Cl2分解,可采取的措施有_______ 。(至少写一条)。
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾,生成两种强酸 ②易分解:SO2Cl2 |
| H2SO4 | 10.4 | 338 | 强吸水性、稳定不易分解 |

(1)D的名称
(2)能替代装置戊中KMnO4是_______(填字母代号)。
| A.氯酸钾 | B.二氧化锰 | C.五氧化二磷 | D.漂白粉 |
(4)反应过程中,为防止SO2Cl2分解,可采取的措施有
硫酰氯(SO2Cl2)对眼和上呼吸道黏膜有强烈的刺激性,但其在工业上有重要作用。其与硫酸的部分性质如表:
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为 ,其实验装置如图所示(夹持仪器已省略):
,其实验装置如图所示(夹持仪器已省略):
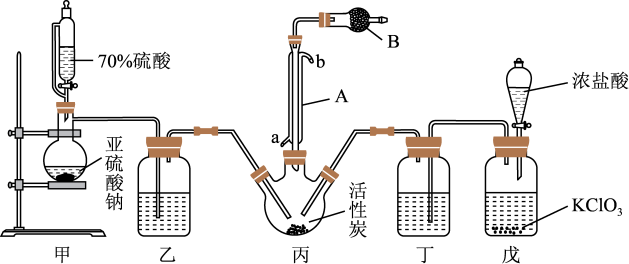
(1)甲装置中发生反应的化学方程式为:_______ 。
(2)仪器B中盛放的药品是_______ 。
(3)实验时,装置戊中发生反应的离子方程式为_______ 。
(4)若缺少装置乙和丁,则硫酰氯会水解,硫酰氯水解的化学方程式为_______ 。
(5)反应一段时间后,需在丙装置的三颈烧瓶外面加上冷水浴装置,其原因是_______ 。
(6)实验开始时,戊中开始加入 ,假设
,假设 在过量盐酸作用下完全转化为
在过量盐酸作用下完全转化为 ,实验结束后得到
,实验结束后得到 纯净的硫酰氯,则硫酰氯的产率为
纯净的硫酰氯,则硫酰氯的产率为_______ 。(产率=实际产量/理论产量 )
)
(7)少量硫酰氯也可用氯磺酸(ClSO2OH)直接分解获得,反应方程式为 。分离出的产品中往往含有少量的
。分离出的产品中往往含有少量的 ,请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、
,请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、 溶液、蒸馏水、紫色石蕊溶液):
溶液、蒸馏水、紫色石蕊溶液):_______ 。
| 物质 | 熔点/ | 沸点/ | 其他性质 |
| -54.1 | 69.1 | ①遇水易水解,产生大量白雾,生成两种强酸; ②易分解: | |
| 10.4 | 338 | 强吸水性、稳定不易分解 |

(1)甲装置中发生反应的化学方程式为:
(2)仪器B中盛放的药品是
(3)实验时,装置戊中发生反应的离子方程式为
(4)若缺少装置乙和丁,则硫酰氯会水解,硫酰氯水解的化学方程式为
(5)反应一段时间后,需在丙装置的三颈烧瓶外面加上冷水浴装置,其原因是
(6)实验开始时,戊中开始加入
(7)少量硫酰氯也可用氯磺酸(ClSO2OH)直接分解获得,反应方程式为
硫酰氯(SO2Cl2)对眼和上呼吸道黏膜有强烈的刺激性,但其在工业上有重要作用。其与硫酸的部分性质如下表:
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为:SO2(g)+Cl2(g)=SO2Cl2(1) ∆H<0,其实验装置如图所示(夹持仪器已省略):
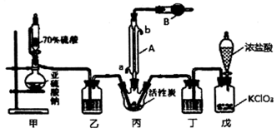
(1)仪器A的名称为____________ ,冷却水应该从______ (填“a”或“b”) 口进入。
(2)仪器B中盛放的药品是__________ 。
(3)实验时,装置戊中发生反应的化学方程式为____________ 。
(4)若缺少装置乙和丁,则硫酰氯会水解,硫酰氯水解的化学方程式为___________ 。
(5)反应一段时间后,需在丙装置的三颈瓶外面加上冷水浴装置,其原因是__________ 。
(6)实验开始时,戊中开始加入12.25gKC1O3,假设KC1O3在过量盐酸作用下完全转化为Cl2,实验结束后得到32.4g纯净的硫酰氯,则硫酰氯的产率为______ 。
(7)少量硫酰氯也可用氙磺酸(ClSO2OH)直接分解获得,反应方程式为:2ClSO2OH=H2SO4+SO2Cl2。
①在分解产物中分离出硫酰氯的实验操作名称是_____ ,现实验室提供的玻璃仪器有漏斗、烧杯、蒸发皿、酒精灯、接液管、锥形瓶,该分离操作中还需要补充的玻璃仪器是_____ 、_____ 、_____ 。
②分离出的产品中往往含有少量的H2SO4,请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊试液):___________________ 。
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2Cl2 | -54.1 | 69.1 | ①遇水易水解,产生大量白雾,生成两种强酸 ②易分解:SO2Cl2 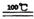 SO2↑+Cl2↑ SO2↑+Cl2↑ |
| H2SO4 | 10.4 | 338 | 强吸水性、稳定不易分解 |

(1)仪器A的名称为
(2)仪器B中盛放的药品是
(3)实验时,装置戊中发生反应的化学方程式为
(4)若缺少装置乙和丁,则硫酰氯会水解,硫酰氯水解的化学方程式为
(5)反应一段时间后,需在丙装置的三颈瓶外面加上冷水浴装置,其原因是
(6)实验开始时,戊中开始加入12.25gKC1O3,假设KC1O3在过量盐酸作用下完全转化为Cl2,实验结束后得到32.4g纯净的硫酰氯,则硫酰氯的产率为
(7)少量硫酰氯也可用氙磺酸(ClSO2OH)直接分解获得,反应方程式为:2ClSO2OH=H2SO4+SO2Cl2。
①在分解产物中分离出硫酰氯的实验操作名称是
②分离出的产品中往往含有少量的H2SO4,请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、紫色石蕊试液):
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网


