解答题-工业流程题 适中0.65 引用3 组卷149
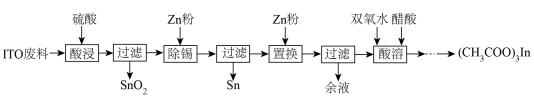
醋酸铟是一种化工产品,以ITO靶材废料(主要由 、
、 组成)为原料制备醋酸铟的流程如下:
组成)为原料制备醋酸铟的流程如下:
(1)已知 和
和 可反应生成偏铟酸铯(CsInO2),也可以与
可反应生成偏铟酸铯(CsInO2),也可以与 反应生成
反应生成 ,据此判断
,据此判断 属于
属于___________ (填“酸性氧化物”“碱性氧化物”或“两性氧化物”)。写出 与
与 反应的离子方程式:
反应的离子方程式:___________ 。
(2)酸浸时,铟的浸出率在不同温度和硫酸浓度下的数值如下表,锡的浸出率小于20%。
由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而___________ (填“增大”“减小”或“不变”,下同),温度越高,硫酸浓度对铟的浸出率影响___________ 。
(3)酸溶时无气泡产生,则酸溶时发生反应的化学方程式为___________ 。
(4)现有一份 和
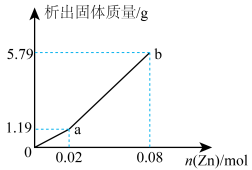
和 的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为
的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量的关系如图所示。图中ab段反应的离子方程式为___________ ,该混合溶液中, 和
和 的物质的量浓度之比为
的物质的量浓度之比为___________ 。
(1)已知
(2)酸浸时,铟的浸出率在不同温度和硫酸浓度下的数值如下表,锡的浸出率小于20%。
| 温度 | 30℃ | 50℃ | 70℃ | 90℃ |
| 56% | 72% | 83% | 91% | |
| 68% | 81% | 89% | 94% |
(3)酸溶时无气泡产生,则酸溶时发生反应的化学方程式为
(4)现有一份
23-24高三上·安徽蚌埠·阶段练习
类题推荐
铟(In)主要应用于透明导电图层、荧光材料、有机合成等,以ITO靶材废料(主要由In2O3、SnO2组成)为原料回收铟的工艺流程如图:

已知:i. 锡、锌的性质均与铝的性质相似.
ii. 铟不与强碱反应,氢氧化铟难与强碱性溶液反应,在较浓的氢氧化钠溶液中也只有少量溶解。
iii. Ksp[In(OH)3]=1×10-33 Ksp[Sn(OH)4]=1×10-56
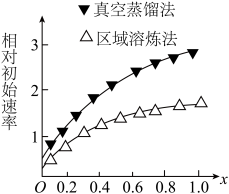
(1)海绵状ITO[xIn2O3(1-x)SnO2]可作异佛尔酮二胺合成的催化剂,如图表示相同条件下,两种不同方法制得的催化剂催化异佛尔酮二胺的相对初始速率随x的变化曲线。真空蒸馏法的相对初始速率较大的原因可能是_________ ,In2O3、SnO2两种氧化物中,催化效果更好的是__________ ;
(2)酸浸时,铟的浸出率随温度和硫酸浓度的关系如表,锡的浸出率小于20%。
①写出“浸出”反应的化学方程式:___________________________ ;
②由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而_____________ (填“增大”“减小”或“不变”下同),温度越高,硫酸浓度对铟的浸出率影响__________ ;
(3)现有一份In2(SO4)3和Sn2(SO4)2的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量关系如图所示:
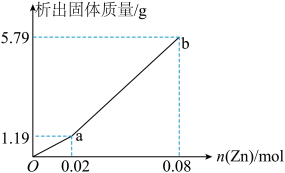
该混合溶液中,In3+和Sn4+的物质的量浓度之比为_______________ ;
(4)若“浸酸”后的溶液中In2(SO4)3的浓度为1 mol/L,取100 mL该溶液向其中滴加氨水,当Sn4+沉淀完全[设c(Sn4+)=1×10-6 mol/L]时,溶液的pH=____________ ,此时In3+是否开始形成沉淀_____ (填“是”或“否”);
(5)“碱熔”时主要反应的离子方程式为___________ ;
(6)以粗铟为阳极,纯铟为阴极,H2SO4、NaCl和InCl3混合液为电解液可提纯粗铟。写出阴极反应的电极方程式:___________ 。

已知:i. 锡、锌的性质均与铝的性质相似.
ii. 铟不与强碱反应,氢氧化铟难与强碱性溶液反应,在较浓的氢氧化钠溶液中也只有少量溶解。
iii. Ksp[In(OH)3]=1×10-33 Ksp[Sn(OH)4]=1×10-56
(1)海绵状ITO[xIn2O3(1-x)SnO2]可作异佛尔酮二胺合成的催化剂,如图表示相同条件下,两种不同方法制得的催化剂催化异佛尔酮二胺的相对初始速率随x的变化曲线。真空蒸馏法的相对初始速率较大的原因可能是

(2)酸浸时,铟的浸出率随温度和硫酸浓度的关系如表,锡的浸出率小于20%。
| 30℃ | 50℃ | 70℃ | 90℃ | |
| 3 mol/L H2SO4 | 56% | 72% | 83% | 91% |
| 4 mol/L H2SO4 | 68% | 81% | 89% | 94% |
②由上表信息可得出规律:其他条件不变时,铟的浸出率随温度升高而
(3)现有一份In2(SO4)3和Sn2(SO4)2的混合溶液,向其中逐渐加入锌粉,测得析出固体的质量随加入锌粉的物质的量关系如图所示:

该混合溶液中,In3+和Sn4+的物质的量浓度之比为
(4)若“浸酸”后的溶液中In2(SO4)3的浓度为1 mol/L,取100 mL该溶液向其中滴加氨水,当Sn4+沉淀完全[设c(Sn4+)=1×10-6 mol/L]时,溶液的pH=
(5)“碱熔”时主要反应的离子方程式为
(6)以粗铟为阳极,纯铟为阴极,H2SO4、NaCl和InCl3混合液为电解液可提纯粗铟。写出阴极反应的电极方程式:
组卷网是一个信息分享及获取的平台,不能确保所有知识产权权属清晰,如您发现相关试题侵犯您的合法权益,请联系组卷网